D’après Charpentier C et al., abstr. PS09.3 / Palich R et al., abstr. eP101, actualisés
L’échec virologique était défini comme 2 charges virales (CV) consécutives ≥ 50 copies/mL, et l’absence de réponse virologique correspondait à une diminution de charge viraleCharge virale La charge virale plasmatique est le nombre de particules virales contenues dans un échantillon de sang ou autre contenant (salive, LCR, sperme..). Pour le VIH, la charge virale est utilisée comme marqueur afin de suivre la progression de la maladie et mesurer l’efficacité des traitements. Le niveau de charge virale, mais plus encore le taux de CD4, participent à la décision de traitement par les antirétroviraux. < 1 log10 copie/mL ou à une CV restant > 50 copies/mL à la semaine 24. Les tests génotypiques de résistance cumulés de l’ensemble des participants étaient réinterprétés selon l’algorithme de l’ANRS-MIE.
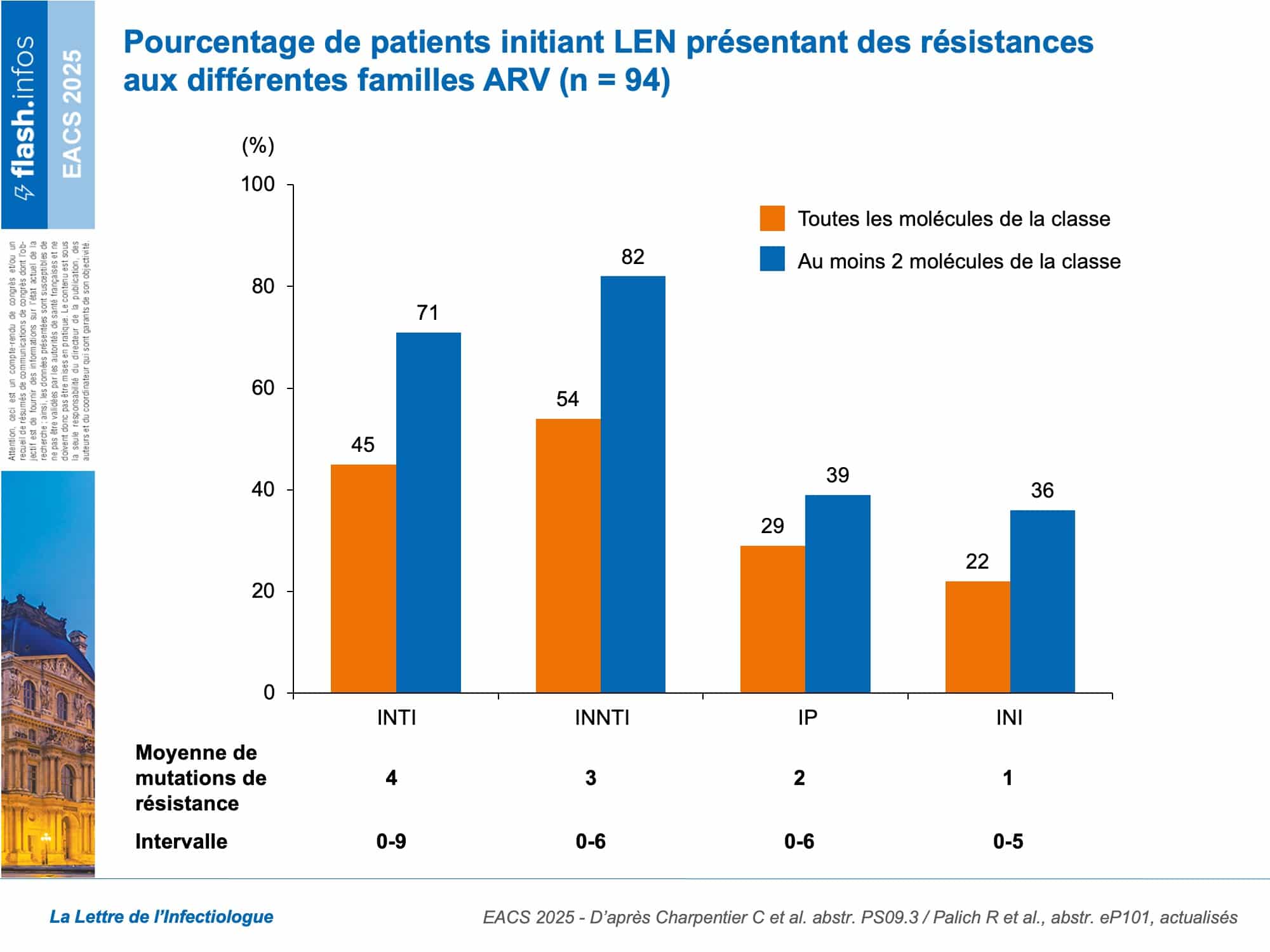
Au total, 94 PVVIHPVVIH Personne vivant avec le VIH ont été incluses dans l’analyse, dont 49 (52 %) étaient en suppression virologique au moment de l’initiation du LEN et du traitement ARV associé. En miroir, 45 (48 %) avaient une CV détectable, avec une CV médiane à 2,5 log10 copies/mL. Les participants étaient porteurs de virus présentant une résistance cumulée à de nombreux ARV, dans plusieurs classes thérapeutiques, limitant les options thérapeutiques (figure 1). La durée médiane de suivi sous LEN était de 14 mois. Le score de sensibilité génotypique (genotypic susceptibility score, GSS) des ARV associés au LEN était inférieur à 1 chez 51 participants (65 %). 12 participants (13 %) ont interrompu le traitement à base de LEN : 3 étant perdus de vue, 4 en raison d’un échec virologique, 1 en raison d’effets indésirables cutanés, 1 sur décision du patient, et 3 en raison d’un décès sans lien avec le traitement. L’échec virologique tel que défini dans cette étude observationnelle est survenu chez 7 participants (7 %) : 3 qui étaient en succès virologique à l’initiation du LEN, et 4 déjà en échec au moment de l’initiation du LEN. Une absence de réponse virologique (CV médiane : 164 copies/mL) a été observée chez 12 participants (13 %), tous en échec virologique au moment du début du LEN. Une séquence de la capside au moment de l’échec était disponible pour 8 participants, révélant l’émergence de la mutation N74D chez un seul d’entre eux. Aucune mutation de résistance émergente n’a été observée pour les autres ARV du traitement de fond, à l’exception d’un passage vers un tropisme X4 chez une personne recevant du maraviroc. Les concentrations plasmatiques de LEN étaient disponibles pour 11 des 19 personnes en échec virologique, avec des taux considérés comme adéquats (> 15 ng/mL) dans 27/35 (68 %) échantillons analysés.
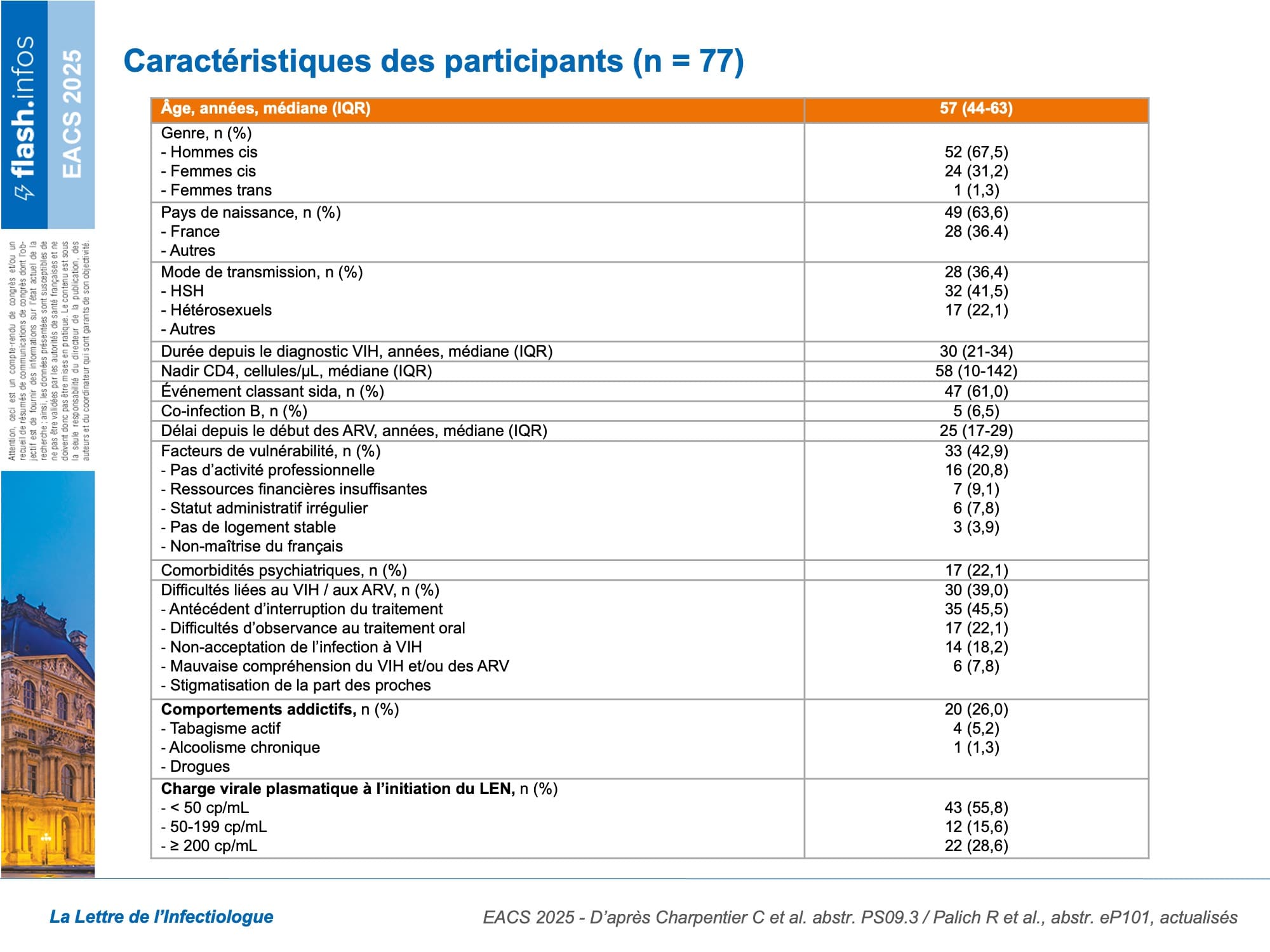
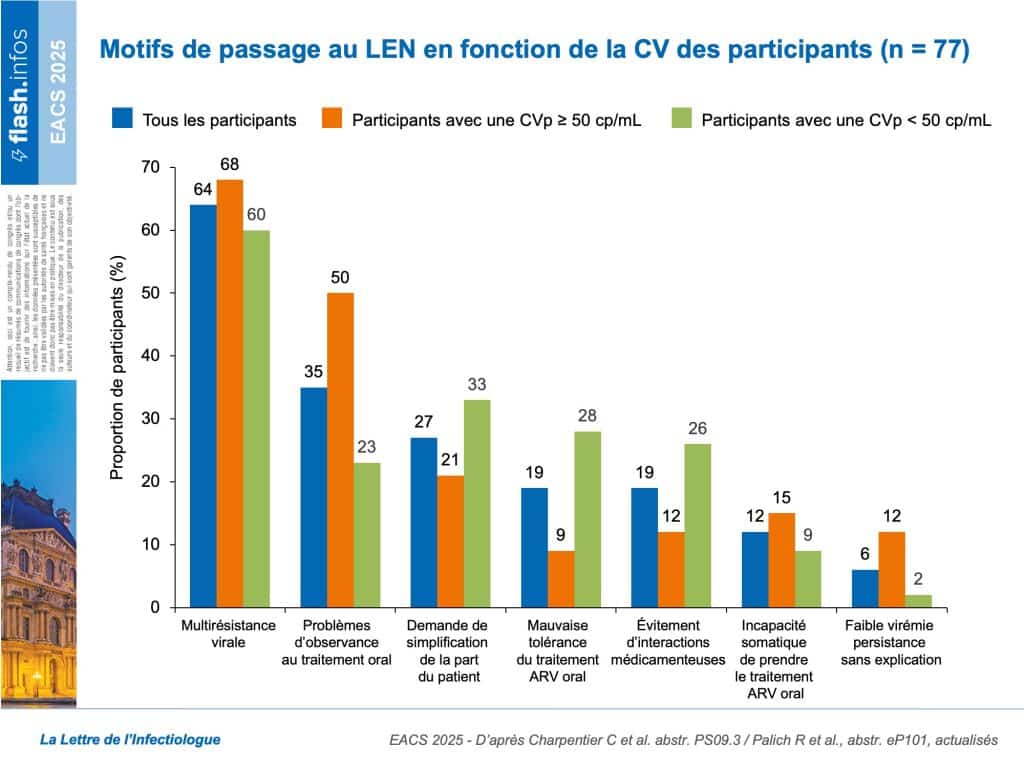
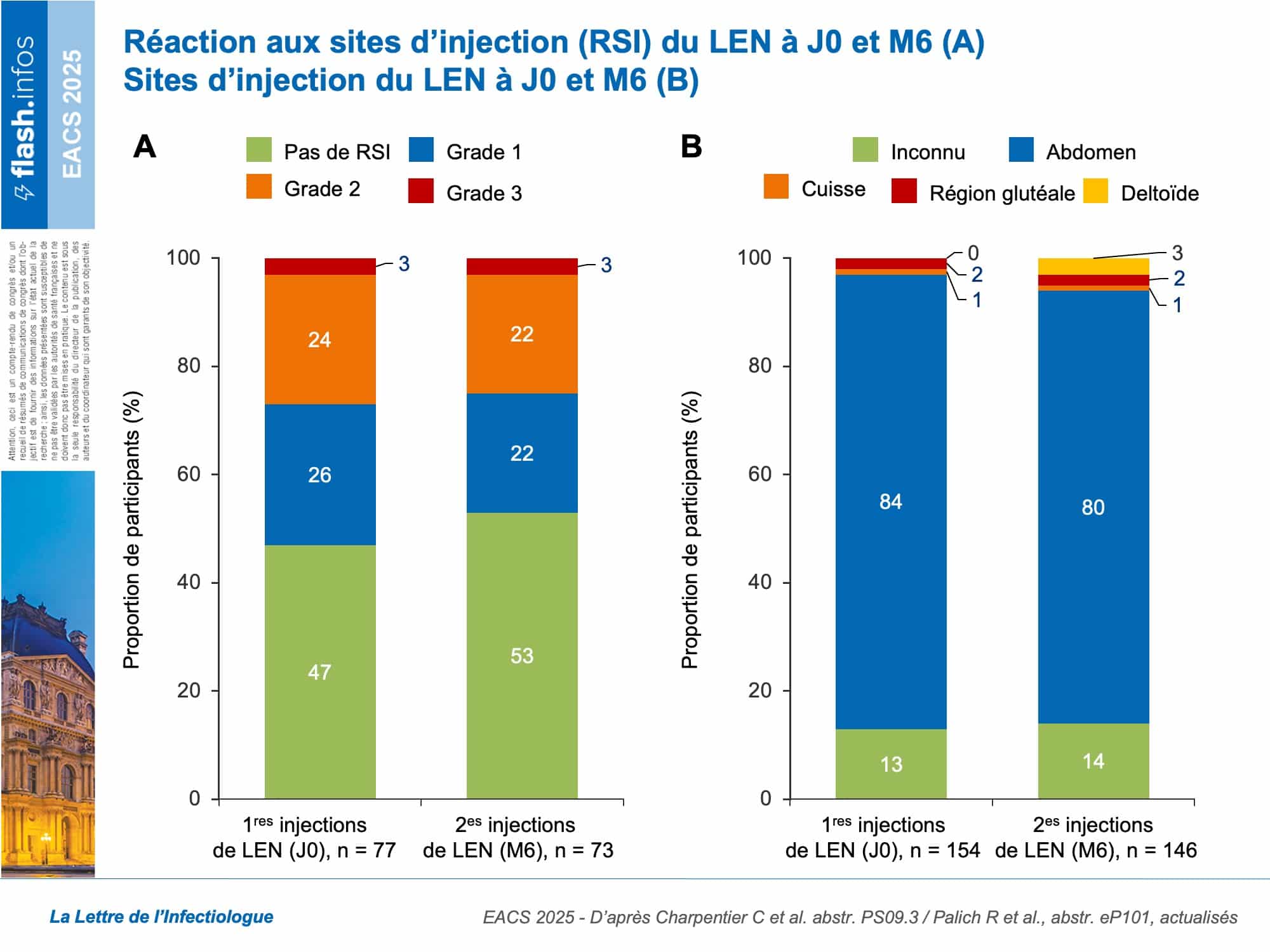
Une autre étude, conduite auprès d’une population d’étude sensiblement identique, permet de connaître les caractéristiques cliniques des PVVIH recevant du LEN durant cette période. Cette deuxième analyse portait sur 77 participants, présentant de nombreux facteurs de vulnérabilité et des difficultés d’observance (tableau). Les principales raisons mentionnées pour passer à un traitement par LEN (en association à d’autres ARV) étaient la multirésistance virale (64 %), les difficultés d’observance (35 %), une demande de simplification du traitement ARV demandée par le patient (27 %), une mauvaise tolérance du traitement ARV oral (20 %) et l’éviction d’interactions médicamenteuses (20 %) (figure 2). Des réactions au site d’injection (RSI) ont été rapportées chez 41/77 participants (53 %) au moment des premières injections (J0) et chez 34/73 (47 %) au moment des deuxièmes injections (M6). 96 % (129/134) des injections à J0 et 93 % (117/126) des injections à M6 ont été administrées dans l’abdomen (figure 3). À M6, les injections ont été effectuées “dans les temps” pour 81 % des participants, en avance pour 15 %, et en retard pour 4,1 %.
En conclusion, ces deux études françaises montrent que les PVVIH recevant du LEN depuis sa commercialisation présentent un profil distinct de celui des participants des essais cliniques pivots, incluant de nombreuses personnes en succès virologique bénéficiant, pour certaines d’entre elles, d’un traitement “tout injectable” par l’association du LEN avec le cabotégravir et/ou la rilpivirine injectable.
Cet article a été précédemment publié dans le Flash-Infos de la Lettre de l’infectiologue d’Edimark consacré à l’EACS. Nous le reproduisons ici avec leur aimable autorisation.
