Pendant près de deux ans, le tecovirimat a incarné l’espoir thérapeutique face au mpox. Utilisé dans de nombreux pays via des dispositifs d’accès compassionnel, recommandé dans certaines situations à risque, il représentait la seule option antivirale disponible à grande échelle contre cette infection à orthopoxvirusOrthopoxvirus Famille de virus à laquelle appartiennent la variole, la vaccine et le monkeypox (mpox). Mais les résultats de l’essai international STOMP/A5418, publiés dans le The New England Journal of Medicine, rebattent les cartes : chez les adultes atteints d’un mpox à cladeClade Les clades désignent les variations d’un même virus qui ont divergé au gré des mutations génétiques. II, le médicament ne raccourcit ni le temps de guérison des lésions, ni l’intensité de la douleur, ni la durée de la détection virale.
Cette démonstration, issue d’un essai randomisé en double aveugleDouble aveugle L'étude avec répartition aléatoire, randomisé ou en double insu (ou en double aveugle) est une démarche expérimentale utilisée en recherche médicale et pharmaceutique faisant que ni le patient ni le médecin ne sait quel traitement est pris : traitement A ou B, traitement A ou placébo. contrôlé par placeboPlacebo Substance inerte, sans activité pharmacologique, ayant la même apparence que le produit auquel on souhaite le comparer. (NDR rien à voir avec le groupe de rock alternatif formé en 1994 à Londres par Brian Molko et Stefan Olsdal.) marque un tournant. Elle rappelle, une fois encore, qu’une plausibilité biologique et des données animales solides ne suffisent pas à garantir un bénéfice clinique chez l’humain.
Un antiviral avec des résultats négatifs dans deux études : quelle place en 2026 ?
Le tecovirimat (TPOXX) avait été autorisé initialement contre la variole selon la procédure réglementaire dite “Animal Rule”, qui permet une approbation sur la base de modèles animaux lorsqu’il serait impossible ou non éthique de réaliser des essais d’efficacité chez l’humain. Son mécanisme d’action cible la protéine virale p37, indispensable à la formation des particules virales enveloppées capables de disséminer dans l’organisme. Cette cible étant conservée parmi les orthopoxvirus, l’hypothèse d’une efficacité contre le virus mpox paraissait cohérente.
Les données in vitro et chez le primate non humain montraient une réduction de la mortalité, de la charge viraleCharge virale La charge virale plasmatique est le nombre de particules virales contenues dans un échantillon de sang ou autre contenant (salive, LCR, sperme..). Pour le VIH, la charge virale est utilisée comme marqueur afin de suivre la progression de la maladie et mesurer l’efficacité des traitements. Le niveau de charge virale, mais plus encore le taux de CD4, participent à la décision de traitement par les antirétroviraux. et du nombre de lésions. Lorsque l’épidémie mondiale de mpox a émergé en 2022, le repositionnement du tecovirimat s’est donc imposé comme une évidence. Pourtant, jusqu’à présent, aucune étude randomisée d’ampleur n’avait confirmé son efficacité chez l’humain.
L’essai STOMP : une méthodologie robuste
L’étude STOMP/A5418 a été menée dans 49 centres répartis dans sept pays. Les investigateurs ont inclus des adultes présentant un mpox symptomatique confirmé biologiquement, avec au moins une lésion cutanée ou muqueuse active et un début des symptômes datant de moins de 14 jours.
Les participants ont été randomisés selon un ratio 2:1 pour recevoir soit du tecovirimat oral, soit un placebo pendant 14 jours. L’essai était conduit en double aveugle, garantissant que ni les patients ni les cliniciens ne connaissaient l’assignation. Le critère principal était le délai jusqu’à la résolution clinique complète : toutes les lésions cutanées devaient être croûtées ou cicatrisées, et toutes les lésions muqueuses visibles guéries.
Les chercheurs ont également analysé l’évolution de la douleur à l’aide d’une échelle numérique standardisée, la cinétique de cicatrisation complète (réépithélialisation) ainsi que la disparition de l’ADN viral dans différents prélèvements. Un sous-groupe a bénéficié d’analyses pharmacocinétiques détaillées pour vérifier l’exposition au médicament.
Parmi les 412 participants initialement randomisés, 344 présentaient une infection confirmée biologiquement et ont été inclus dans les analyses d’efficacité. Le profil des patients reflétait fidèlement l’épidémie observée en Europe et en Amérique du Nord : âge médian de 34 ans, très grande majorité d’hommes, près de la moitié d’origine hispanique ou latino, et plus d’un tiers infecté par le VIHVIH Virus de l’immunodéficience humaine. En anglais : HIV (Human Immunodeficiency Virus). Isolé en 1983 à l’institut pasteur de paris; découverte récemment (2008) récompensée par le prix Nobel de médecine décerné à Luc montagnier et à Françoise Barré-Sinoussi.
Un point mérite toutefois attention : le délai médian entre le début des symptômes et l’inclusion était de huit jours. Trois quarts des participants avaient déjà dépassé cinq jours d’évolution au moment de l’initiation du traitement, ce qui pourrait théoriquement réduire l’impact d’un antiviral.
Résultats : aucun bénéfice sur la guérison des lésions
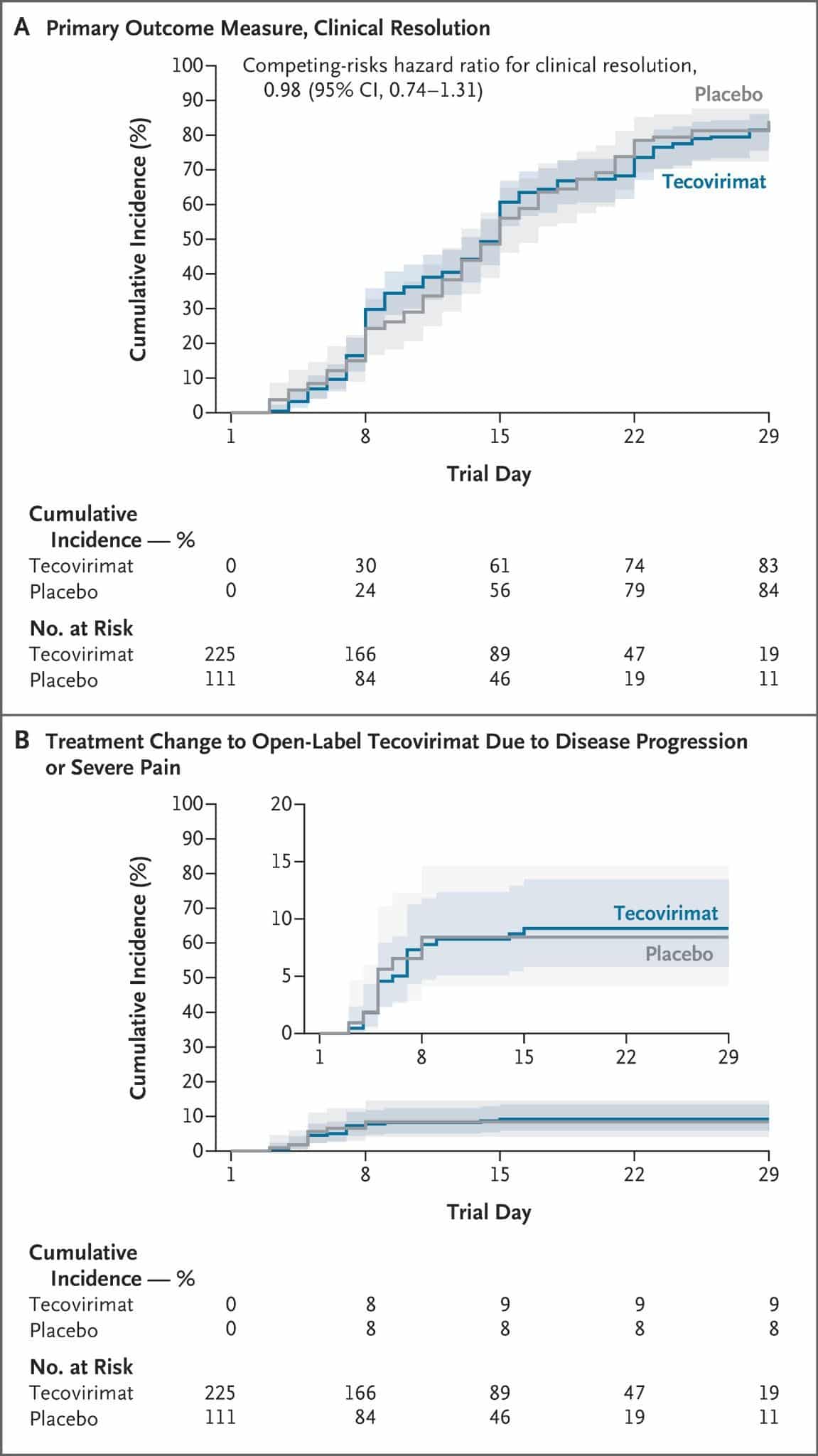
Les résultats sont sans ambiguïté. À 29 jours, 83% des patients du groupe tecovirimat contre 84% de ceux du groupe placebo ont vu leurs lésions cutanées guéries. L’analyse statistique ne montre aucune différence significative entre les deux groupes.
Les analyses en sous-groupes n’ont révélé aucun signal en faveur du médicament, qu’il s’agisse des patients traités précocement (dans les trois ou cinq premiers jours), des personnes vivant avec le VIH, de celles ayant reçu une vaccination antivariolique antérieure ou encore de celles présentant une charge lésionnelle élevée.
Une évolution de la douleur similaire
La douleur constitue l’un des symptômes les plus invalidants du mpox, en particulier en cas de proctite (inflammation de la muqueuse du rectum) ou de lésions génitales. Dans l’essai, environ un tiers des participants présentaient une douleur sévère à l’inclusion.
L’intensité douloureuse a diminué progressivement dans les deux groupes, mais la trajectoire était strictement parallèle. Chez les patients initialement très douloureux, la réduction moyenne sur les cinq premiers jours de traitement était pratiquement identique sous tecovirimat et sous placebo. Aucun avantage clinique n’a été démontré.
Une clairance virale comparable
L’analyse virologique apporte un éclairage intéressant. À J8, un pourcentage légèrement plus élevé de patients traités par tecovirimat présentait une disparition de l’ADN viral dans la lésion index (48% vs 37%). Toutefois, l’intervalle de confiance incluait l’absence d’effet et, surtout, cette différence disparaissait totalement à J15. Les prélèvements oraux, rectaux et sanguins n’ont montré aucune différence significative à aucun moment.
Autrement dit, même si un signal précoce semblait possible, il ne se traduisait pas par un bénéfice clinique mesurable ni durable.
L’hypothèse d’un sous-dosage écartée
Les analyses pharmacocinétiques indiquent que les concentrations plasmatiques atteintes dépassaient largement le seuil considéré comme efficace dans les modèles animaux. Le niveau mesuré à 12 heures post-dose était environ 2,8 fois supérieur au seuil cible extrapolé des études précliniques. Le manque d’efficacité ne semble donc pas lié à une exposition insuffisante.
Sur le plan de la sécurité, le tecovirimat confirme son bon profil de tolérance. Les événements indésirables graves étaient rares et comparables entre les deux groupes. Aucun décès n’a été rapporté.
Notons que plus d’un tiers des participants vivaient avec le VIH. Aucun bénéfice spécifique n’a été observé dans ce sous-groupe. Les patients présentant une immunodépression sévère étaient toutefois inclus dans un bras ouvert, ce qui empêche une comparaison formelle. Les formes graves observées chez certaines personnes très immunodéprimées restent donc un enjeu clinique distinct.
Un tournant pour la stratégie thérapeutique du mpox
Selon les dernières actualisations des recommandation du CDC, “les résultats de ces essais cliniques suggèrent que la plupart des patients atteints de variole du singe qui ne présentent pas de maladie grave ou de facteurs de risque de maladie grave (par exemple, une immunodéficience sévère) guériront grâce à des soins de soutien et à la gestion de la douleur. Le rôle du tecovirimat dans le traitement de la variole du singe chez les patients présentant une immunodéficience sévère, notamment un VIH avancé, n’a pas été déterminé et nécessite des essais cliniques supplémentaires.”
Ensemble, ces données fragilisent l’idée que cet antiviral puisse modifier l’évolution naturelle du mpox non grave chez l’adulte immunocompétent. Il existe d’autres études randomisées comme l’essai Unity.
Dans un contexte où plus de 100 000 cas et 220 décès ont été signalés à l’échelle mondiale depuis 2022 selon l’Organisation mondiale de la santé, ces résultats rappellent l’importance des essais randomisés même en situation d’urgence sanitaire. Ils soulignent également la nécessité d’explorer d’autres stratégies : nouvelles molécules, associations antivirales, inclusion spécifique des personnes immunodéprimées dans des protocoles contrôlés.
En attendant, la prise en charge du mpox repose principalement sur le traitement symptomatique, l’isolement des cas, la vaccination ciblée, l’identification précoce des complications et une approche One Health comme actuellement étudiée par l’ANRS-MIE. Récemment, le Comité des Médicaments à usage humain de l’EMA a recommandé de “ne plus utiliser Tecovirimat SIGA pour le traitement du mpox”. Cette recommandation, qui reposent sur 4 études (PALM007, STOMP, UNITY et PLATINUM-UK), n’affecte pas les autres indications autorisées de Tecovirimat SIGA, notamment le traitement de la variole, de la vaccine bovine et des complications liées à la vaccination antivariolique.
Selon les auteurs de l’étude publiée dans le NEJM, la démonstration rigoureuse de l’absence d’efficacité du tecovirimat dans les populations et les conditions de prescription des deux études constitue, paradoxalement, une avancée essentielle pour orienter la recherche vers des approches plus bénéfiques. Une autre piste avec des données in vitro et in vivo suggère le recours à des associations antivirales incluant le tecovirimat avec le brincidofovir, le cidofovir, la trifluridine, et les immunoglobulines (VIGIV), ou encore l’adjonction de la lactoferrin. Il est néanmoins utile de rappeler que le tecovirinat a été utilisé avec succès (non randomisé) dans des formes graves, y compris chez les PVVIHPVVIH Personne vivant avec le VIH immunodéprimés, populations exclues des deux études sus-citées.
Référence
- Jason Zucker et al. Tecovirimat for the Treatment of Mpox. New England Journal of Medicine Volume 394 • Number 9 • February 26, 2026 Pages: 884-895 https://www.cdc.gov/monkeypox/hcp/clinical-care/tecovirimat.html
- Tian L, Qin H, Li S, Zhang M, Zhuang L, Hong B, Liu K, Li M, Li S, Wang Y, Song L, Liu Y, Wang Y, Liu H, Tong Y, Fan H.Lactoferrin blocks orthopoxvirus entry via heparan sulphate and regulates host antiviral pathways. Emerg Microbes Infect. 2026 Dec;15(1):2631205. doi: 10.1080/22221751.2026.2631205. Epub 2026 Mar 6.
- Zargar AA. Mpox and the one health approach. Dialogues Health. 2026 Mar 17;8:100293. doi: 10.1016/j.dialog.2026.100293. eCollection 2026 Jun. https://pubmed.ncbi.nlm.nih.gov/41908519/
- Promer, Katherine; Brenner, Sara BT; Ostrer, Lily; Bortner, Adam C.; Wilkin, Timothy J. A. Mpox therapeutics in the post-STOMP/PALM era. Current Opinion in HIV and AIDS 21(2):p 103-109, March 2026. | DOI: 10.1097/COH.0000000000001015
- Calin R, Périllaud-Dubois C, Marot S, Kerrou K, Peytavin G, Bachir M, Kirch AL, Lassel L, Fallet V, Gozlan J, Pain JB, Senet P, Ferraris O, Bine S, Hubert M, Schwartz O, Morand-Joubert L, Pialoux G. Mpox Hepatic and Pulmonary Lesions in HIV/Hepatitis B Virus Co-Infected Patient, France. Emerg Infect Dis. 2024 Nov;30(11):2445-2447. doi: 10.3201/eid3011.241331.
- Mitjà O, Alemany A, Marks M, Lezama Mora JI, Rodríguez-Aldama JC, Torres Silva MS, Corral Herrera EA, Crabtree-Ramirez B, Blanco JL, Girometti N, Mazzotta V, Hazra A, Silva M, Montenegro-Idrogo JJ, Gebo K, Ghosn J, Peña Vázquez MF, Matos Prado E, Unigwe U, Villar-García J, Wald-Dickler N, Zucker J, Paredes R, Calmy A, Waters L, Galvan-Casas C, Walmsley S, Orkin CM; SHARE-NET writing group. Mpox in people with advanced HIV infection: a global case serie. Lancet. 2023 Mar 18;401(10380):939-949. doi: 10.1016/S0140-6736(23)00273-8. Epub 2023 Feb 21.PMID: 36828001
