«Le titre de notre symposium est un clin d’œil à la chanson des Beatles When I’m 64», explique Shibani S. Mukerji (Massachusetts General Hospital, Boston) en introduction de sa présentation, la 3e d’une session dense consacrée au vieillissement cérébral des personnes vivant avec le VIHVIH Virus de l’immunodéficience humaine. En anglais : HIV (Human Immunodeficiency Virus). Isolé en 1983 à l’institut pasteur de paris; découverte récemment (2008) récompensée par le prix Nobel de médecine décerné à Luc montagnier et à Françoise Barré-Sinoussi. «L’idée, quand Paul McCartney l’a écrite adolescent, c’était que 64 ans, c’était très vieux. Or, pour la première fois dans l’histoire, des centaines de milliers de personnes vivant avec le VIH dépassent cet âge grâce au traitement antirétroviral». Face à ce progrès, la question au cœur de cette session de la CROICROI «Conference on Retroviruses and Opportunistic Infections», la Conférence sur les rétrovirus et les infections opportunistes annuelle où sont présentés les dernières et plus importantes décision scientifiques dans le champs de la recherche sur le VIH. 2026 sera donc: comment s’assurer que ces années gagnées s’accompagnent d’une bonne santé cérébrale?

À l’heure de l’indétectabilité, le VIH affecte-t-il encore les fonctions cognitives ?
Neurodégénérescence et risque de démence chez les adultes âgés vivant avec le VIH: biomarqueurs et épidémiologie, Alan Winston, Imperial College London, Londres, Royaume-Uni, Session 18, CROI 2026
C’est la première des deux questions qu’Alan Winston (Imperial College London) a choisi de traiter, reprenant celles posées que le réseau communautaire britannique UK-CAB a posées aux personnes vieillissant avec le VIH. La réponse est nuancée. Dans les années 1980-1990, en l’absence de traitement, le complexe démentiel lié au sidaSida Syndrome d’immunodéficience acquise. En anglais, AIDS, acquired immuno-deficiency syndrome. était fréquent et relativement facile à diagnostiquer. Avec l’arrivée du traitement antirétroviral, ces formes sévères ont considérablement reculé. Mais des plaintes cognitives persistent chez certaines personnes sous traitement efficace, ce qui a conduit, il y a une vingtaine d’années, à l’élaboration des critères de Frascati (HAND, pour HIV-associated neurocognitive disorders).
Le problème, souligne Alan Winston, c’est que ces critères classifient mécaniquement 30 à 40% des personnes comme ayant un trouble cognitif. Le neurologue Sam Nightingale (université du Cap) a montré que, selon la définition retenue, on peut classer de 20% à 97% d’une cohorte comme présentant un problème neuro-cognitif. Les données de la cohorte britannique POPPY (Pharmacokinetic and Clinical Observations in People Over Fifty) montrent quant à elles des scores cognitifs moyens assez comparables entre personnes vivant avec le VIH et personnes séronégatives au mode de vie similaire, même si une plus grande dispersion vers les scores bas est observée dans le premier groupe.
Ces critères ont eu par ailleurs des conséquences concrètes non souhaitées: en Afrique du Sud, où une étude a suggéré que les chauffeurs routiers longue distance vivant avec le VIH ne devraient pas exercer sans évaluations supplémentaires; et au Royaume-Uni, les pilotes vivant avec le VIH se sont longtemps vu refuser des licences sans restriction par l’Autorité de l’aviation civile.
Et la maladie d’Alzheimer ?
Au-delà des troubles cognitifs directement liés au VIH, la maladie d’Alzheimer est-elle plus fréquente chez les personnes vivant avec le VIH? «Le verdict actuel est probablement que non», résume Alan Winston, tout en appelant à la prudence : les cohortes suivies sont peut-être encore trop jeunes pour observer un signal significatif, l’incidence de la maladie d’Alzheimer n’augmentant fortement que dans les dernières décennies de vie.
Les biomarqueurs Alzheimer ne fonctionnent pas de la même manière chez les personnes vivant avec le VIH : le signal, s’il existe, est bien moins marqué que chez les personnes séronégatives. Une étude thaïlandaise publiée récemment montre toutefois que les personnes dans le quartile supérieur de P-tau étaient plus susceptibles de voir leur score au test MoCA se détériorer au fil du temps — avec la réserve que seul ce test a été utilisé. Enfin, une large étude de cohorte américaine confirme que les personnes diagnostiquées tardivement pour le VIH, avec un taux de CD4 bas au diagnostic ou ne remontant pas sous traitement, ont un risque accru de démence au cours du temps.
Le message d’Alan Winston est clair : le VIH peut encore affecter le cerveau, en particulier chez les personnes diagnostiquées tardivement, et les effets «hérités» du passé persistent.
Le cerveau vieillit-il plus vite avec le VIH ?
C’est la seconde question que se posait la communauté des PvVIHPVVIH Personne vivant avec le VIH interrogée, et sans doute la plus anxiogène. La réponse, là encore, appelle à la nuance. Les données longitudinales de la cohorte COBRA (collaboration entre les cohortes POPPY au Royaume-Uni et AGEhIV aux Pays-Bas) montrent une légère réduction du volume cérébral à l’inclusion chez les personnes vivant avec le VIH, probablement liée à des effets hérités de la période non ou mal traitée. Mais en longitudinal, les trajectoires sont identiques à celles des personnes séronégatives : le volume de matière grise diminue à la même vitesse, les hypersignaux de la substance blanche augmentent au même rythme, et les courbes de performance cognitive se superposent.
En revanche, une étude récente du même groupe apporte une nuance capitale : les personnes dont la charge viraleCharge virale La charge virale plasmatique est le nombre de particules virales contenues dans un échantillon de sang ou autre contenant (salive, LCR, sperme..). Pour le VIH, la charge virale est utilisée comme marqueur afin de suivre la progression de la maladie et mesurer l’efficacité des traitements. Le niveau de charge virale, mais plus encore le taux de CD4, participent à la décision de traitement par les antirétroviraux. n’est pas contrôlée présentent une trajectoire nettement différente. La virémie persistante semble néfaste pour la santé cérébrale et pourrait faire basculer vers un profil de vieillissement accéléré.
Plusieurs données convergent pour souligner l’importance du traitement. Des résultats thaïlandais montrent que chez les personnes débutant un traitement très tôt après l’acquisition du VIH, de nombreux marqueurs de santé cérébrale reviennent à des niveaux comparables à ceux attendus chez les participants de l’essai.
L’étude Connect, menée dans le township de Gugulethu au Cap par l’équipe de Sam Nightingale, apporte un éclairage complémentaire. Elle a comparé la fonction cognitive de personnes vivant avec le VIH et de personnes séronégatives, avant et après un changement de traitement (passage de l’éfavirenz au dolutégravir). Sous éfavirenz, la fonction cognitive était légèrement inférieure chez les personnes vivant avec le VIH. Sous dolutégravirDolutégravir Le dolutégravir, nom de marque de Tivicay® et présent dans Juluca® et Triumeq®, appartient à la une classe de médicaments antirétroviraux appelés inhibiteurs de l'intégrase. Il est utilisé en combinaison avec d'autres médicaments anti-VIH. les performances étaient pratiquement indistinguables entre les deux groupes. «Ce sont des données très solides», commente Alan Winston.
Mesurer le vieillissement biologique : les horloges épigénétiques
Vieillissement épigénétique du cerveau et VIH : horloges de méthylation et modifications liées aux antirétroviraux, Michael J. Corley, University of California San Diego Medical Center, La Jolla, CA, États-Unis, session 19, CROI 2026
Comment savoir si le corps d’une personne vieillit plus vite que ne le laisse supposer son âge civil? C’est la question à laquelle Michael J. Corley (université de Californie San Diego) tente de répondre à l’aide d’un outil en plein essor : les horloges épigénétiques.
Le principe repose sur un mécanisme bien connu : la méthylation de l’ADN, c’est-à-dire l’ajout de petits groupes chimiques sur certains sites du génome. Ce marquage varie avec l’âge de façon prévisible. En analysant ces marques dans un large échantillon, on peut construire un modèle statistique capable d’estimer l’âge biologique d’un individu (voir encadré). L’écart entre cet âge biologique et l’âge civil indique si l’organisme vieillit plus vite ou plus lentement que la moyenne.
Les premières horloges, dites de première génération, prédisaient simplement l’âge chronologique. Celles de deuxième et troisième génération sont plus ambitieuses : elles intègrent des données cliniques comme le risque de mortalité, la multimorbidité ou des caractéristiques propres à certains organes, dont le cerveau. «Chaque horloge donne un résultat significativement différent selon ce pour quoi elle a été conçue», souligne Michael Corley.
Âge chronologique et âge biologique
L’âge chronologique mesure le temps écoulé depuis la naissance. L’âge biologique est un reflet composite de la physiologie et de l’état moléculaire, qui capture la résilience, les expositions cumulées et les risques de maladie. La durée de vie (lifespan), le nombre d’années vécues, peut ainsi être séparée de la durée de vie en bonne santé (healthspan), le nombre d’années vécues en bonne santé. Cet écart varie considérablement à travers le monde, comme l’illustrent les données comparant les Amériques et l’Afrique.
Ce que les horloges révèlent chez les personnes vivant avec le VIH
Appliquées aux personnes vivant avec le VIH (cohortes américaines NNTC et CHARTER), ces horloges détectent un vieillissement accéléré. Les données de la cohorte thaïlandaise RV254 montrent que ces modifications apparaissent très tôt, dès l’infection aiguë, et qu’elles ne sont pas complètement corrigées par l’initiation rapide du traitement antirétroviral.
Le cerveau n’est pas épargné. Des travaux sur les tissus cérébraux de donneurs décédés (cohorte NNTC) retrouvent un signal de vieillissement épigénétique dans le cortex et le cervelet. Un poster présenté à cette même CROI (n°456) montre que l’horloge GrimAge, conçue pour prédire la mortalité, est associée à un vieillissement cérébral accéléré en imagerie et à une dysfonction exécutive.
Ces horloges commencent aussi à servir d’outil de tri pour évaluer des interventions. L’exercice physique et le régime alimentaire montrent un impact sur l’âge cérébral épigénétique. Les agonistes du récepteur GLP-1, testés dans un essai en double aveugleDouble aveugle L'étude avec répartition aléatoire, randomisé ou en double insu (ou en double aveugle) est une démarche expérimentale utilisée en recherche médicale et pharmaceutique faisant que ni le patient ni le médecin ne sait quel traitement est pris : traitement A ou B, traitement A ou placébo. contre placeboPlacebo Substance inerte, sans activité pharmacologique, ayant la même apparence que le produit auquel on souhaite le comparer. (NDR rien à voir avec le groupe de rock alternatif formé en 1994 à Londres par Brian Molko et Stefan Olsdal.) ont montré un signal dans plusieurs systèmes dont le système nerveux central, un résultat préliminaire mais prometteur.
Michael Corley appelle toutefois à la prudence : ces outils ne sont pas encore prêts pour un usage clinique de routine. Leur interprétation dépend fortement de la population étudiée et de l’horloge choisie. «Il faut savoir sur quoi elles ont été entraînées et comment on les utilise dans ses études», résume-t-il.
Agir : vers une santé cérébrale proactive
Vieillissement cognitif chez les personnes vivant avec le VIH : évaluation et prise en charge cliniques, Shibani S. Mukerji, Massachusetts General Hospital, Boston, MA, États-Unis, Session 20, CROI 2026
Face à ces constats, la troisième intervenante, Shibani S. Mukerji, a centré son propos sur la traduction de ces résultats de recherche en pratique clinique. Son point de départ : les personnes vivant avec le VIH ne forment pas un groupe homogène et elle distingue trois générations dans cette population. Les survivants de très longue date, qui ont traversé le pire de la crise du sida sans traitement efficace, avec des années d’immunosuppression et d’exposition à des médicaments neurotoxiques; Les survivants de longue date, qui ont été infectés par le VIH après l’arrivée des traitements efficaces, mais qui présentent des multimorbidités; et les survivants «à vie», parfois plus jeunes, qui ont grandi avec le VIH et chez qui le développement cérébral s’est fait parallèlement à l’infection.
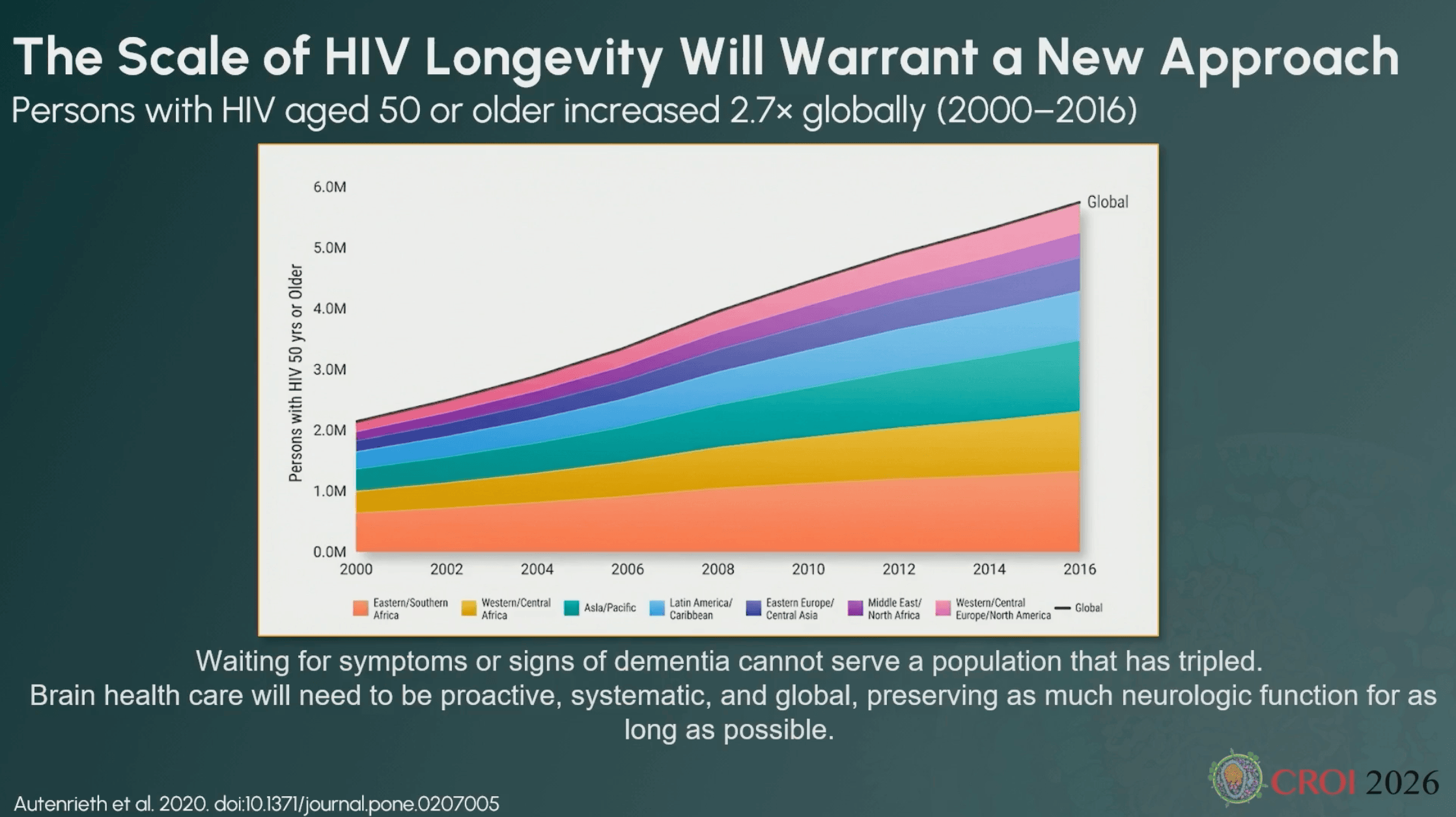
«Si nous utilisons l’âge chronologique seul, en dépistant tout le monde à 60 ans par exemple, nous risquons une inefficience médicale, un gaspillage économique et un échec envers les personnes qui ont besoin de soins personnalisés», prévient-elle. Entre 2000 et 2016, le nombre de personnes vivant avec le VIH âgées de 50 ans ou plus a été multiplié par 2,7 au niveau mondial. Simplement «attendre les symptômes de démence ne peut pas permettre de servir efficacement une population qui a triplé.»
Le sexe, la géographie, l’origine ethnique, l’accès aux soins, les comorbidités et les déterminants structurels créent autant de trajectoires distinctes. «Face à une population hétérogène, les soins réactifs ne peuvent pas passer à l’échelle», explique Shibani Mukerji.
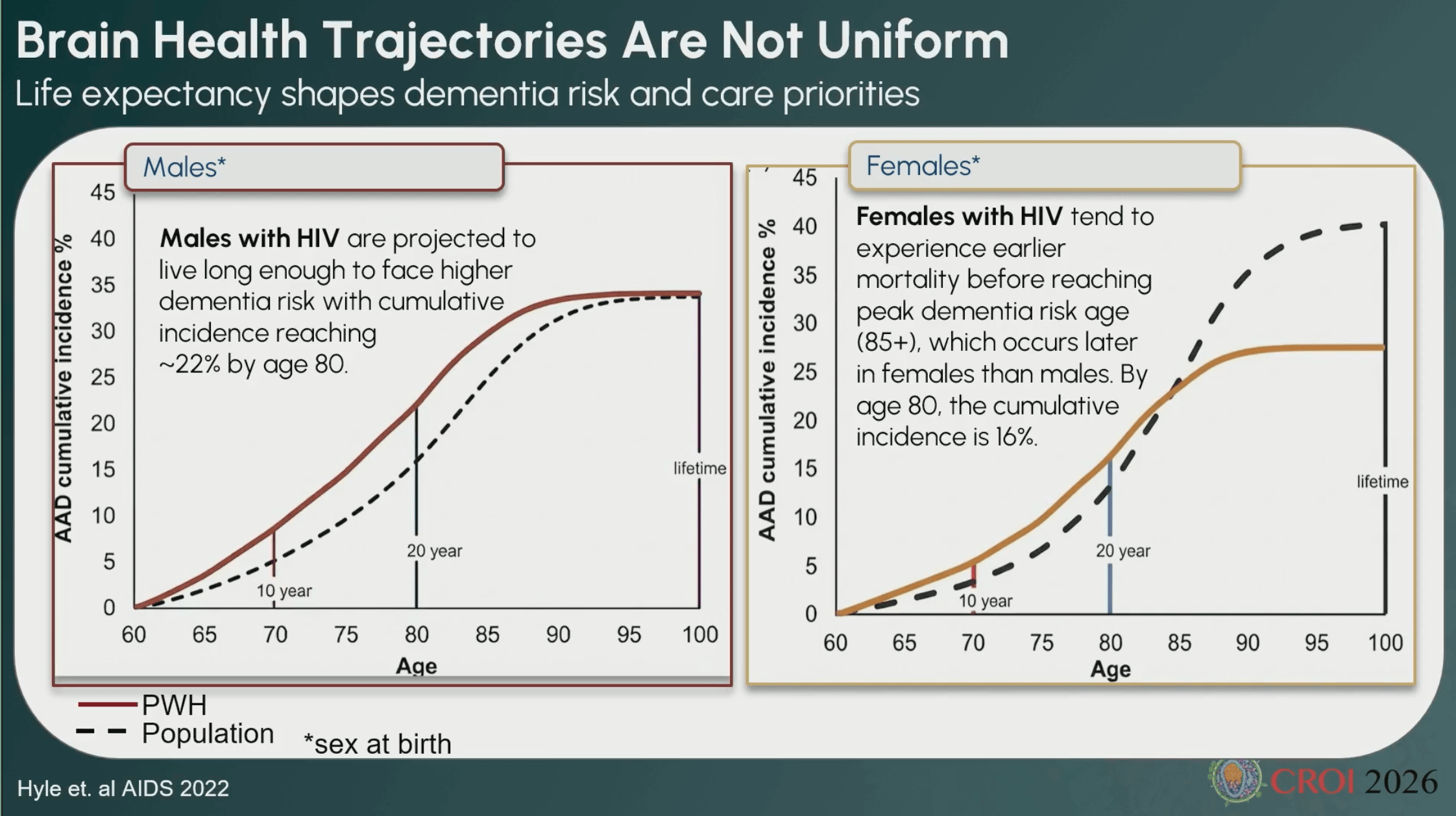
Des données de projection d’Emily Hyle (Hyle et. al AIDS 2022) et ses collègues montrent que les hommes vivant avec le VIH, aux États-Unis, font face à des risques cumulés de démence similaires à ceux de la population générale, quoique légèrement supérieurs, soit autour de 22 % vers 80 ans. Les femmes vivant avec le VIH ont une trajectoire différente en raison d’autres risques : si elles meurent plus tôt de maladies cardiovasculaires ou d’autres pathologies, elles n’atteindront pas l’âge de pic de démence observé chez les femmes séronégatives (85 ans et plus).
La santé cérébrale selon l’OMS
L’Organisation mondiale de la santé définit la santé cérébrale comme un état continu d’atteinte et de maintien d’un fonctionnement neurologique optimal soutenant le bien-être physique, mental et social tout au long de la vie. Le National Institute on Aging identifie cinq piliers : le mouvement (marcher, utiliser ses mains), les sens (voir, entendre, toucher, l’équilibre), la cognition (mémoire, attention, fonctions exécutives), et la santé émotionnelle (humeur, lien social). Au niveau mondial, une personne fait un AVC toutes les trois secondes.
La santé cérébrale dans le parcours de soin des VIH.
Face à ces données, comment expliquer que la santé cérébrale n’est pas encore prise en compte systématiquement en consultation ? Shibani Mukerji identifie trois freins principaux. Tout d’abord, les patients hésitent, même s’ils souhaiteraient que leur médecin aborde la question, à cause de l’âgisme, de la stigmatisation, du sentiment qu’on ne peut rien y faire. Les médecins, eux aussi, hésitent, au cause du manque de temps en consultation, de priorités concurrentes, de la complexité diagnostique perçue ou de l’absence de traitement curatif. Enfin, les différentes communautés ont des manières différentes d’aborder la santé cérébrale. Certaines n’utilisent pas le mot «démence», par exemple. «Si nous pouvons demander la charge virale et discuter de sexualité, nous pouvons avoir des discussions non menaçantes sur la santé cérébrale», argue Shibani Mukerji.
Pourtant, le besoin, et surtout le bénéfice possible, est là : jusqu’à 45 % de la démence serait attribuable à des facteurs de risque modifiables. Citons les plus importants de la vie adulte : la perte auditive (une perte de 10 décibels est associée à une augmentation d’environ 16 % du risque de démence), l’hypercholestérolémie, l’isolement social, la dépression, l’inactivité physique, le tabagisme et le diabète.

Shibani Mukerji met en avant des données de l’essai REPRIEVE (statines chez les personnes vivant avec le VIH) dans un poster également présenté à la CROI 2026 : 31 % des participants avaient une pression artérielle élevée sans diagnostic d’hypertension, 12 % une hypertension non diagnostiquée, et parmi ceux traités, seuls 64 % des hommes et 56 % des femmes avaient une pression artérielle contrôlée. Le défaut de contrôle au milieu de la vie fait perdre la réserve vasculaire cérébrale et compromet la capacité du cerveau à encaisser les agressions à un âge plus avancé.
Pour l’intervenante, l’isolement social mérite une attention particulière: «On peut envisager de prescrire le lien social. C’est une intervention médicale. Ce n’est pas si différent de dire « vous pouvez prendre votre atorvastatine 40 mg par jour »», défend-elle
Shibani Mukerji alerte également sur les médicaments à action centrale souvent prescrits sans suivi cognitif: les anticholinergiques, qui bloquent l’acétylcholine et altèrent mémoire et attention ; les gabapentinoïdes, qui provoquent un brouillard cognitif ; et les benzodiazépines en usage chronique, qui sont associées à un risque de démence. Des protocoles de de prescription existent, et un essai est en cours pour déterminer si la prescription des anticholinergiques améliore les capacités cognitives.
Enfin, la comorbidité la plus sous-estimée en termes d’impact cérébral est probablement la santé mentale, avec des taux élevés de troubles dans tous les groupes d’âge, toutes les origines ethniques et tous les genres, selon l’enquête britannique Positive Voices citée par Alan Winston en première partie. La stigmatisation joue également un rôle direct : des données longitudinales de la cohorte WIHS (Women’s Interagency HIV Study) montrent qu’un niveau plus élevé de stigmatisation internalisée à l’inclusion est associé à une moins bonne performance cognitive globale.
Un modèle à trois niveaux
Shibani Mukerji propose un modèle par paliers. Le premier niveau serait un kit de santé cérébrale régionalisé, ciblant précocement les facteurs de risque, complété par des dosages simples (B12, thyroïde, glucose, sérologieSérologie Étude des sérums pour déterminer la présence d’anticorps dirigés contre des antigènes. syphilis). Le deuxième niveau, un système d’escalade avec ponction lombaire et imagerie en cas de déclin rapide ou de signes focaux. Le troisième niveau, une orientation vers un neurologue pour les situations inexpliquées. Le tout adossé à un modèle en réseau («hub and spoke»), avec des centres de référence accessibles avant que les personnes n’aient besoin d’aide en urgence. Comme le résume Shibani Mukerji: «Nous pouvons renforcer la durée de vie cérébrale (brain span) en étudiant les soins groupés (bundled care).»
Parallèlement, la formation des soignants est un levier d’action qui peut se faire à faible coût et qui a beaucoup d’impact. «Si l’IAS peut former des membres à travers le monde, nous pouvons former les gens à réaliser des évaluations cognitives au lit du patient», affirme-t-elle, citant les neurologues en Zambie, en Afrique du Sud, en Thaïlande, au Pérou, au Brésil et en Équateur qui forment activement les équipes locales.
Un optimisme à nuancer pour la France
Les messages de cette session convergent, comme le souligne une revue récente publiée dans The Lancet HIV : les effets délétères de l’infection sur le cerveau peuvent être atténués. Un traitement antirétroviral précoce et efficace protège largement l’organe. Les horloges épigénétiques offrent des outils prometteurs pour mesurer le vieillissement biologique et évaluer les interventions, même si elles ne sont pas encore prêtes pour un usage de routine. Près de la moitié des démences pourrait être prévenue en agissant sur des facteurs modifiables, à condition d’intégrer la santé cérébrale dans les soins courants des personnes vivant avec le VIH, de manière proactive et personnalisée.
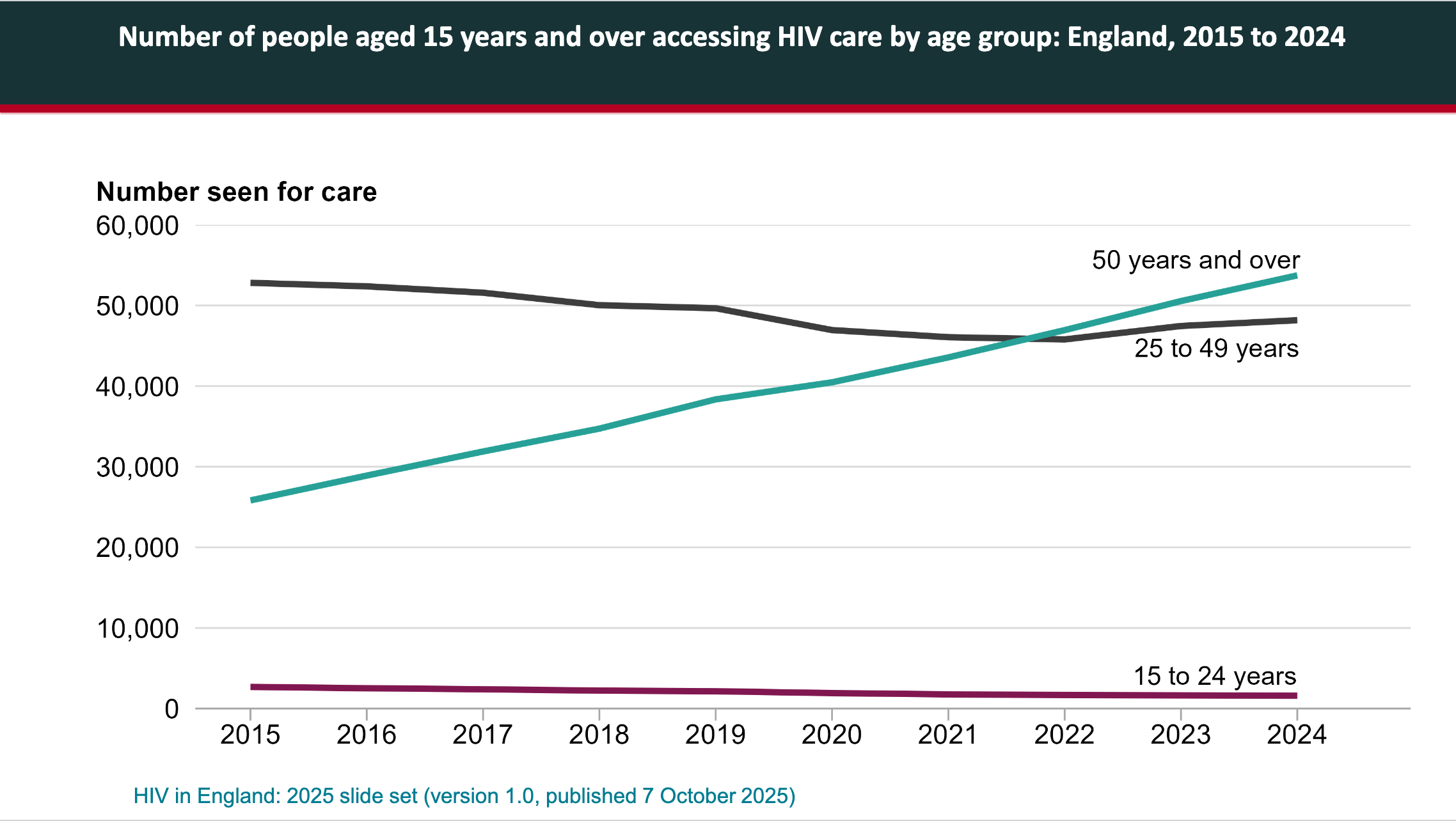
Ces résultats sont rassurants pour les personnes diagnostiquées et traitées rapidement aujourd’hui. Mais en France, la réalité de la file active invite à la prudence. Les données de l’enquête VESPA 3 (2023), dont les premiers résultats ont été présentés au congrès de la SFLS, montrent que la médiane d’ancienneté du diagnostic est de 19 ans : la moitié des personnes suivies ont été diagnostiquées avant 2004, c’est-à-dire avant la généralisation du traitement immédiat, et un quart avant 1994, avant l’arrivée des trithérapies. Les CD4 au diagnostic restent par ailleurs bas : selon le rapport des indicateurs de prise en charge des PVVIH dans les COREVIH (FHDH et AQUIVIH, 2022), 30% des personnes avaient moins de 200 CD4/mm3 ou un stade sida à la prise en charge, 20% entre 200 et 350, et seulement un tiers dépassait les 500. Une grande partie des personnes vivant avec le VIH en France ont donc été exposées, pendant des années, aux effets d’une infection non traitée sur le cerveau et l’organisme.
Ce constat soulève une question de fond. La tendance actuelle est d’intégrer le suivi VIH dans les médecine de ville, en sortant des services spécialisés. Or les données présentées à cette session plaident pour un suivi coordonné incluant des compétences neurologiques, un accès à l’imagerie et des évaluations cognitives structurées. Les neurologues sont déjà peu disponibles dans les pays à hauts revenus; ils le sont encore moins dans les pays où les systèmes de santé sont sous-dimensionnés. Le modèle en réseau proposé par Shibani Mukerji, avec des centres de référence et une formation des soignants de première ligne aux évaluations de base, offre sans doute la voie la plus réaliste pour concilier ces deux exigences.
