Récemment, la société pharmaceutique sud-coréenne SK bioscience a annoncé que le vaccin pan-sarbécovirus GBP511 allait entrer en phase 1 en Australie (https://www.ipd.uw.edu/2026/02/gbp511-vaccine-clinical-trial-begins/). Ce vaccin mis au point par des chercheurs de l’Université de Washington est destiné à protéger contre l’infection par le Sars-CoV-2 mais également les autres coronavirus apparentés, y compris ceux qui pourraient apparaître dans le futur1. C’est l’occasion de faire le point sur ce type d’approche.
Pourquoi développer un vaccin pan-sarbécovirus ?
Au cours des vingt dernières années, le monde a assisté à trois émergences d’infections par des coronavirus: le Sars-CoV en 2003, le MERS-CoV en 2012, puis le Sars-CoV-2 en 2019 à l’origine de la pandémie de CovidCovid-19 Une maladie à coronavirus, parfois désignée covid (d'après l'acronyme anglais de coronavirus disease) est une maladie causée par un coronavirus (CoV). L'expression peut faire référence aux maladies suivantes : le syndrome respiratoire aigu sévère (SRAS) causé par le virus SARS-CoV, le syndrome respiratoire du Moyen-Orient (MERS) causé par le virus MERS-CoV, la maladie à coronavirus 2019 (Covid-19) causée par le virus SARS-CoV-2. À ces événements s’ajoute la circulation continue de coronavirus saisonniers humains, dont l’identification est également assez récente, responsables d’une part non négligeable des infections respiratoires. Cette succession d’émergences reflète une dynamique biologique propre aux coronavirus, caractérisée par une grande diversité génétique dans les réservoirs animaux, notamment chez les chauves-souris, et une capacité élevée d’adaptation et de franchissement de la barrière d’espèce.
Les données actuelles convergent vers l’idée que l’émergence de nouveaux coronavirus est un phénomène attendu qu’il convient d’anticiper2. La circulation simultanée de nombreux coronavirus chez l’animal, les phénomènes de recombinaison et l’augmentation des interactions entre humains et réservoirs animaux créent un environnement propice à l’apparition de nouveaux virus capables d’infecter l’homme. De plus, l’expérience récente du Sars-CoV-2 a montré que même après l’émergence initiale, la diversification virale peut conduire à l’apparition de variants échappant partiellement à l’immunité, limitant l’efficacité des vaccins de première génération3.
Dans ce contexte, le développement de vaccins pan-sarbécovirus s’inscrit dans une logique de prévention anticipatrice. Il ne s’agit plus seulement de répondre à une épidémie en cours, mais de se préparer à celles qui surviendront inévitablement. Cette approche vise à dépasser les limites des vaccins actuels, qui restent largement spécifiques d’une souche ou d’un variant, pour induire une immunité capable de reconnaître un ensemble plus large de virus apparentés.
Quels virus cible-t-on avec un vaccin pan-sarbécovirus ?
Les Coronaviridae constituent une grande famille de virus à ARN simple brin de polarité positive. Au sein de cette famille, la sous-famille des Orthocoronavirinae regroupe les coronavirus d’intérêt pour la pathologie humaine. Cette sous-famille est elle-même divisée en quatre genres: les alphacoronavirus, les bêtacoronavirus, les gammacoronavirus et les deltacoronavirus. Les coronavirus humains connus se répartissent principalement entre les alphacoronavirus, avec notamment 229E et NL63, et les bêtacoronavirus, qui comprennent OC43, HKU1, le Sars-CoV-1, le Sars-CoV-2 et le MERS-CoV. Cette organisation phylogénétique est essentielle, car elle conditionne l’ambition et la définition même des vaccins à large spectre.
À partir de cette classification, plusieurs niveaux d’objectif de couverture vaccinale peuvent être théoriquement distingués.
- Vaccins dits « pan-variant » dirigés contre une seule espèce virale, en pratique le Sars-CoV-2, mais avec l’objectif de maintenir une efficacité contre l’ensemble de ses variants.
- Vaccins « pan-sous-genre », par exemple les vaccins pan-sarbécovirus, qui visent à protéger contre les virus du sous-genre Sarbecovirus, incluant le Sars-CoV-1, le Sars-CoV-2 et des coronavirus animaux proches susceptibles d’émerger chez l’homme.
- Vaccins « pan-genre » cherchant à couvrir un genre entier, par exemple l’ensemble des bêtacoronavirus, ce qui inclurait non seulement les sarbécovirus, mais aussi d’autres bêtacoronavirus humains comme le MERS-CoV, OC43 et HKU1.
- Vaccins « pan-sous-famille », visant l’ensemble des Orthocoronavirinae, donc à la fois les alpha- et les bêtacoronavirus humains.
- Vaccin « pan-coronavirus » au sens strict, capable de couvrir l’ensemble de la famille des Coronaviridae.
Cette classification reflète des niveaux croissants de difficultés biologiques et immunologiques. Plus on élargit le spectre visé, plus il devient nécessaire d’identifier des régions antigéniques conservées entre virus phylogénétiquement éloignés, tout en conservant une immunogénicitéImmunogénicité Capacité à produire une réponse immunitaire. suffisante. En pratique, les approches actuellement les plus avancées se concentrent souvent sur des objectifs intermédiaires, notamment les vaccins pan-sarbécovirus, plutôt que sur un véritable vaccin universel couvrant tous les coronavirus.
Quel type d’immunité doit-on induire avec un vaccin pan-sarbécovirus ? Les leçons du Covid… et des infections par les coronavirus banals
Les vaccins contre le Sars-CoV-2, presque tous fondés sur la protéine Spike, ont démontré de manière très nette que les anticorps neutralisants constituent un déterminant majeur de la protection, en particulier vis-à-vis de l’infection symptomatique. L’évolution de la pandémie s’est toutefois accompagnée de l’apparition de variants, associée à une perte d’efficacité plus ou moins importante des vaccins initiaux. Cette vulnérabilité tient au fait que la majorité des anticorps neutralisants les plus puissants ciblent des régions fortement exposées mais relativement variables de la protéine Spike, en particulier le domaine de liaison au récepteur, le RBD. Autrement dit, l’expérience du Covid a confirmé qu’une stratégie vaccinale reposant principalement sur les régions immunodominantes et variables du virus est très performante à court terme, mais insuffisante pour construire une protection large et durable contre des sarbécovirus divergents.
Ceci ne signifie pas pour autant qu’il faille renoncer à cibler la réponse humorale. En effet, des anticorps à large spectre ont pu être identifiés chez l’homme (4). Des travaux ont montré que certaines réponses dirigées contre la sous-unité S2 de la protéine Spike, notamment la région du peptide de fusion, conservent une reconnaissance large au sein des coronavirus4. Dacon et al. ont décrit des anticorps neutralisants capables de reconnaître un motif conservé du peptide de fusion chez les 7 coronavirus infectant l’homme5. Ces anticorps sont rares et dirigés contre S2. Ils sont moins puissants en termes de neutralisation que les anticorps anti-RBD. Un vaccin visant à induire de tels anticorps doit par ailleurs surmonter l’immunodominance naturelle des régions variables de Spike, c’est-à-dire la capacité naturelle de la réponse anticorps à cibler le RBD au détriment de régions plus conservées comme S2.
Une autre observation importante réalisée au cours de la pandémie a été l’impact bénéfique sur la réponse anticorps de l’exposition du système immunitaire à des antigènes apparentés mais distincts. L’exemple le plus marquant est celui des survivants du Sars-CoV-1 vaccinés ensuite par BNT162b26. Les auteurs ont montré chez ces sujets ayant eu des stimulations séquentielles par des antigènes viraux proches mais quand même distants, l’induction d’anticorps neutralisants pan-sarbécovirus, capables de neutraliser non seulement le Sars-CoV-2 et ses variants, mais aussi plusieurs sarbécovirus animaux à potentiel zoonotique.
L’étude de la réponse lymphocytaire T aux coronavirus a été également riche d’enseignements. On a tout d’abord pu étudier l’impact des réponses T croisées préexistantes, dirigées contre des coronavirus banals sur l’infection par le Sars-CoV-2. Swadling et al. ont montré chez des soignants fortement exposés mais demeurés séronégatifs, la présence de réponses T préexistantes dirigées contre le complexe de réplication-transcription, notamment NSP12, capables de s’amplifier rapidement in vivo, suggérant un contrôle abortif de l’infection avant séroconversionSéroconversion Période d'apparition, dans le sang, d'anticorps spécifiques en réponse au virus. Par ailleurs les réponses T induites par la souche ancestrale Wuhan, après infection ou vaccination, reconnaissent largement le variant Omicron avec une conservation d’environ 70-80 % de leur activité fonctionnelle malgré l’échappement des anticorps, contribuant ainsi au maintien de la protection contre les formes sévères de Covid7. Contrairement aux anticorps, les lymphocytes T reconnaissent de courts peptides présentés par le CMH, ce qui leur permet de cibler des régions internes — comme celle de la nucléoprotéine — beaucoup plus conservées du virus. Certaines des protéines les plus conservées à l’échelle des coronavirus, en particulier NSP12 et NSP13 du complexe de réplication-transcription, induisent dans l’infection naturelle des réponses sous-dominantes.
Cette question des réponses immunitaires dominantes et sous-dominantes conduit directement à la question de l’empreinte immunologique, particulièrement importante pour la réponse anticorps. Le Sars-CoV-2 a illustré de manière particulièrement claire la façon dont une première exposition au virus par infection ou vaccination peut modeler durablement les réponses ultérieures. L' »immunological imprinting », proche du concept d’original antigenic sin décrit pour la grippe, correspond au fait que le système immunitaire tend à rappeler préférentiellement les clones mémoires induits par la première rencontre antigénique, même lorsque l’antigène a évolué (https://college-immunologie.fr/focus-on/article/5-PECHE-ANTIGENIQUE-ORIGINEL). Dans le contexte du Sars-CoV-2, plusieurs travaux ont montré que l’infection ou la vaccination par des souches précoces pouvait orienter les réponses de rappel vers des épitopesEpitope Partie d’une molécule capable de stimuler la production d’un anticorps. ancestraux, parfois au détriment de la génération de réponses optimales contre de nouveaux variants8. Ce phénomène n’interdit pas l’élargissement de la réponse, mais il complique la tâche. Ainsi un vaccin pan-sarbécovirus devra composer avec un paysage immunitaire préimprimé par les infections et vaccinations antérieures.
Quelles stratégies vaccinales pour un vaccin pan-sarbécovirus ?
Le développement de vaccins à large spectre contre les sarbécovirus ne constitue pas un concept nouveau mais s’inscrit dans une recherche déjà engagée pour d’autres virus à forte variabilité antigénique ou à potentiel d’émergence, notamment le VIHVIH Virus de l’immunodéficience humaine. En anglais : HIV (Human Immunodeficiency Virus). Isolé en 1983 à l’institut pasteur de paris; découverte récemment (2008) récompensée par le prix Nobel de médecine décerné à Luc montagnier et à Françoise Barré-Sinoussi. les virus influenza ou encore les henipavirus9.
Dans le contexte du développement d’un vaccin pan-sarbécovirus, on retrouve deux grands types de stratégies selon qu’elles ciblent la réponse humorale ou cellulaire.
Stratégies visant à élargir la réponse anticorps: agir sur la nature et la séquence des antigènes
Plusieurs approches complémentaires sont aujourd’hui explorées pour dépasser la focalisation naturelle de la réponse anticorps sur les régions variables de la Spike.
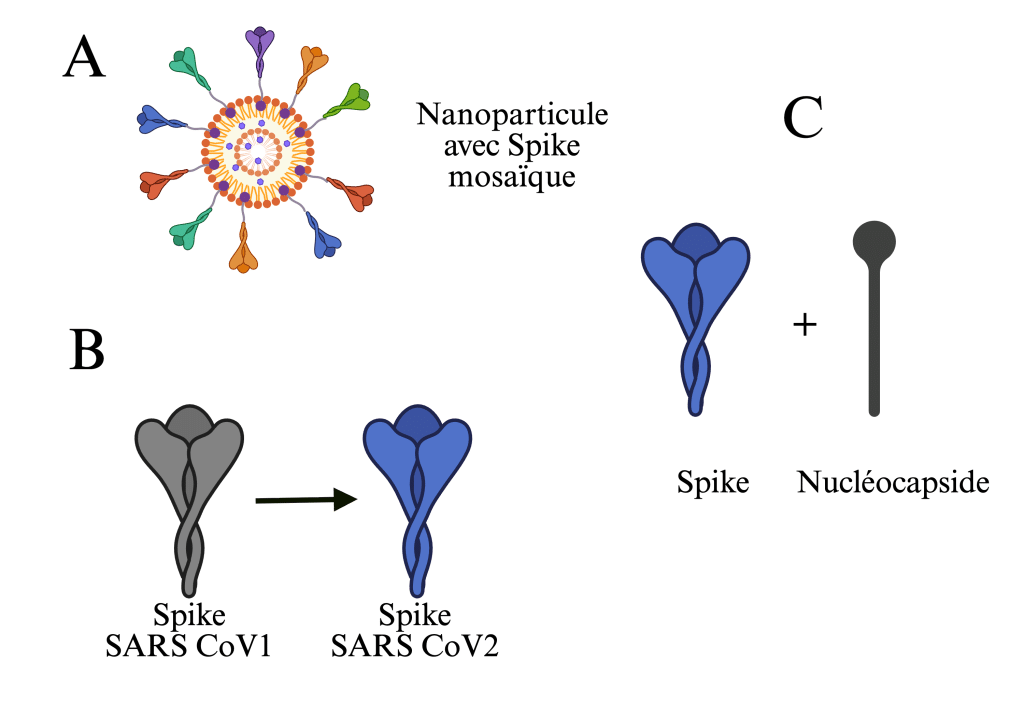
La première repose sur la manière dont l’antigène est présenté au système immunitaire. Les plateformes nanoparticulaires permettent une présentation multivalente hautement ordonnée des antigènes, favorisant l’activation de clones B rares. Deux stratégies principales ont été développées: l’utilisation de nanoparticules homotypiques, qui présentent un même antigène de manière répétée10, et surtout celle de nanoparticules mosaïques, qui co-expriment plusieurs RBD issus de sarbécovirus distincts11. Cette dernière approche est particulièrement intéressante car elle impose une contrainte de reconnaissance commune entre antigènes, favorisant la sélection de clones B dirigés contre des épitopes conservés plutôt que spécifiques d’une seule souche, la co-présentation antigénique constituant un levier majeur pour induire des réponses croisées9.
Une deuxième approche consiste à modifier la séquence même de l’antigène afin d’augmenter sa représentativité de la diversité virale. Les antigènes consensus ou optimisés par des approches computationnelles, largement développés dans le domaine de la grippe, visent à reconstruire un immunogène capable de couvrir un ensemble de variants13.
D’autres enfin, s’appuyant sur les observations effectuées chez les survivants du Sars-CoV-1 vaccinés contre le Sars-CoV-2 (cf. plus haut), ont développé des stratégies de vaccination séquentielle, reposant sur l’administration successive d’antigènes apparentés mais distincts afin de guider la maturation des lymphocytes B vers des épitopes conservés14.
Ces différentes approches poursuivent un objectif commun: dépasser l’immunodominance naturelle du RBD variable pour favoriser l’émergence d’anticorps dirigés contre des structures conservées.
Associer réponses humorales et cellulaires
Les stratégies centrées exclusivement sur les anticorps pourraient s’avérer cependant insuffisantes pour répondre à la diversité des coronavirus. Dans cette perspective, une seconde orientation majeure consiste à concevoir des vaccins capables d’induire simultanément des réponses humorales larges et des réponses T dirigées contre des régions conservées14. Dans le domaine de la grippe, des vaccins ciblant des protéines internes comme NP ou M1 ont été développés précisément pour induire des réponses T conservées. Dans le cas des coronavirus, cette complémentarité apparaît particulièrement pertinente. Les anticorps peuvent limiter l’infection en amont, tandis que les réponses T interviennent pour contrôler la réplication virale et limiter la progression vers des formes sévères. L’intégration de ces deux dimensions dans un même vaccin apparaît donc particulièrement pertinente.
Conclusion
La mise au point d’un vaccin pan-sarbécovirus constitue aujourd’hui un véritable graal de la vaccinologie, dans un contexte où l’émergence de nouveaux coronavirus apparaît hautement probable. Parmi les stratégies explorées, l’approche dite « mosaïque », à l’origine du vaccin GBP511 (CTG: NCT07280858), illustre parfaitement ce changement de paradigme. En présentant simultanément au système immunitaire plusieurs RBD issus de coronavirus distincts sur une nanoparticule, elle vise à orienter la réponse vers des déterminants conservés communs à l’ensemble des sarbécovirus plutôt que vers une souche unique. Cette stratégie, très intéressante sur le plan conceptuel, n’est toutefois qu’une des voies ayant atteint un développement clinique. D’autres approches cherchant à optimiser les immunogènes, notamment à partir de RBD modifiés ou consensus, et à les associer à des plateformes capables d’induire conjointement des réponses humorales et cellulaires robustes, sont arrivées à maturation comme le montre la mise en place en 2025 de l’essai ANRS0640s LKV-PAN-01 (PanCoV) (CTG: NCT07113106). Bien que des avancées significatives aient été réalisées depuis les premières tentatives de développement de vaccins à large spectre, notamment contre des virus hautement évolutifs comme la grippe, le chemin vers un vaccin capable de couvrir l’ensemble des coronavirus actuels et futurs risque toutefois d’être encore long.
Conflit d’intérêt
Le Pr Lelièvre JD est le coordonnateur de l’essai ANRS0640s LKV-PAN-01 (PanCoV).
Références
- Maringe C, Spicer J, Morris M, Purushotham A, Nolte E, Sullivan R, et al. The impact of the COVID-19Covid-19 Une maladie à coronavirus, parfois désignée covid (d'après l'acronyme anglais de coronavirus disease) est une maladie causée par un coronavirus (CoV). L'expression peut faire référence aux maladies suivantes : le syndrome respiratoire aigu sévère (SRAS) causé par le virus SARS-CoV, le syndrome respiratoire du Moyen-Orient (MERS) causé par le virus MERS-CoV, la maladie à coronavirus 2019 (Covid-19) causée par le virus SARS-CoV-2. pandemic on cancer deaths due to delays in diagnosis in England, UK: a national, population-based, modelling study. Lancet Oncol. août 2020;21(8):1023-34. doi:10.1016/S1470-2045(20)30388-0 ↩︎
- Balloux F, Tan C, Swadling L, Richard D, Jenner C, Maini M, et al. The past, current and future epidemiological dynamic of SARS-CoV-2. Oxf Open Immunol. 11 juin 2022;3(1):iqac003. doi:10.1093/oxfimm/iqac003 ↩︎
- Harvey WT, Carabelli AM, Jackson B, Gupta RK, Thomson EC, Harrison EM, et al. SARS-CoV-2 variants, spike mutations and immune escape. Nat Rev Microbiol. juill 2021;19(7):409-24. doi:10.1038/s41579-021-00573-0 ↩︎
- Chen Y, Zhao X, Zhou H, Zhu H, Jiang S, Wang P. Broadly neutralizing antibodies to SARS-CoV-2 and other human coronaviruses. Nat Rev Immunol. mars 2023;23(3):189-99. doi:10.1038/s41577-022-00784-3 ↩︎
- Dacon C, Tucker C, Peng L, Lee CCD, Lin TH, Yuan M, et al. Broadly neutralizing antibodies target the coronavirus fusion peptide. Science. 12 août 2022;377(6607):728-35. doi:10.1126/science.abq3773 ↩︎
- Tan CW, Chia WN, Young BE, Zhu F, Lim BL, Sia WR, et al. Pan-Sarbecovirus Neutralizing Antibodies in BNT162b2-Immunized SARS-CoV-1 Survivors. N Engl J Med. 7 oct 2021;385(15):1401-6. doi:10.1056/NEJMoa2108453 ↩︎
- Keeton R, Tincho MB, Ngomti A, Baguma R, Benede N, Suzuki A, et al. T cell responses to SARS-CoV-2 spike cross-recognize Omicron. Nature. 17 mars 2022;603(7901):488-92. doi:10.1038/s41586-022-04460-3 ↩︎
- Suryawanshi R, Ott M. SARS-CoV-2 hybrid immunity: silver bullet or silver lining? Nat Rev Immunol. oct 2022;22(10):591-2. doi:10.1038/s41577-022-00771-8 ↩︎
- Tan CW, Valkenburg SA, Poon LLM, Wang LF. Broad-spectrum pan-genus and pan-family virus vaccines. Cell Host Microbe. juin 2023;31(6):902-16. doi:10.1016/j.chom.2023.05.017 ↩︎
- Vu MN, Kelly HG, Kent SJ, Wheatley AK. Current and future nanoparticle vaccines for COVID-19. eBioMedicine. déc 2021;74:103699. doi:10.1016/j.ebiom.2021.103699 ↩︎
- Cohen AA, Gnanapragasam PNP, Lee YE, Hoffman PR, Ou S, Kakutani LM, et al. Mosaic nanoparticles elicit cross-reactive immune responses to zoonotic coronaviruses in mice. Science. 12 févr 2021;371(6530):735-41. doi:10.1126/science.abf6840 ↩︎
- Tan CW, Valkenburg SA, Poon LLM, Wang LF. Broad-spectrum pan-genus and pan-family virus vaccines. Cell Host Microbe. juin 2023;31(6):902-16. doi:10.1016/j.chom.2023.05.017 ↩︎
- Vishwanath S, Carnell GW, Ferrari M, Asbach B, Billmeier M, George C, et al. A computationally designed antigen eliciting broad humoral responses against SARS-CoV-2 and related sarbecoviruses. Nat Biomed Eng. 25 sept 2023;9(2):153-66. doi:10.1038/s41551-023-01094-2 ↩︎
- Peng L, Renauer PA, Ökten A, Fang Z, Park JJ, Zhou X, et al. Variant-specific vaccination induces systems immune responses and potent in vivo protection against SARS-CoV-2. Cell Rep Med. mai 2022;3(5):100634. doi:10.1016/j.xcrm.2022.100634 ↩︎
- Peng L, Renauer PA, Ökten A, Fang Z, Park JJ, Zhou X, et al. Variant-specific vaccination induces systems immune responses and potent in vivo protection against SARS-CoV-2. Cell Rep Med. mai 2022;3(5):100634. doi:10.1016/j.xcrm.2022.100634 ↩︎
