Le lénacapavir est un inhibiteur de capside du VIH-1 à longue durée d’action, administré par voie sous-cutanée tous les six mois, actuellement en développement en prophylaxie pré-exposition (PrEP). Trois communications présentées à la CROICROI «Conference on Retroviruses and Opportunistic Infections», la Conférence sur les rétrovirus et les infections opportunistes annuelle où sont présentés les dernières et plus importantes décision scientifiques dans le champs de la recherche sur le VIH. 2026 fournissent les résultats des essais PURPOSE 1 et PURPOSE 2 à la fin de leur phase randomisée en double aveugleDouble aveugle L'étude avec répartition aléatoire, randomisé ou en double insu (ou en double aveugle) est une démarche expérimentale utilisée en recherche médicale et pharmaceutique faisant que ni le patient ni le médecin ne sait quel traitement est pris : traitement A ou B, traitement A ou placébo. au-delà des analyses intermédiaires publiées jusqu’ici. Au total, cinq infections par le VIHVIH Virus de l’immunodéficience humaine. En anglais : HIV (Human Immunodeficiency Virus). Isolé en 1983 à l’institut pasteur de paris; découverte récemment (2008) récompensée par le prix Nobel de médecine décerné à Luc montagnier et à Françoise Barré-Sinoussi. ont été documentées dans les bras lénacapavir des deux essais.
Parmi ces échecs, deux sont survenus alors que les concentrations plasmatiques de lénacapavir se situaient dans les valeurs attendues pour une protection et que le calendrier d’injections avait été respecté. Un troisième cas est, en revanche, expliqué par une injection manquée et des concentrations très inférieures au seuil protecteur. L’analyse génotypique montre que trois des cinq virus portent la mutation de capside N74D, spécifique du lénacapavir, et que la mutation M184V est présente chez tous, reflétant sa fréquence dans la population virale circulante.
Lénacapavir (LEN) en PrEPPrEP Prophylaxie Pré-Exposition. La PrEP est une stratégie qui permet à une personne séronégative exposée au VIH d'éliminer le risque d'infection, en prenant, de manière continue ou «à la demande», un traitement anti-rétroviral à base de Truvada®. : incidence du VIH-1 et tolérance dans l’étude PURPOSE 2 à la fin de la phase randomisée en double aveugle
D’après Cantos Lucio VD et al. Abstr. 129 actualisé
Parmi les 3 265 participants séronégatifs au VIH à l’inclusion, 2 179 ont été randomisés dans le groupe LEN et 1 086 dans le groupe F/TDF. Après l’analyse principale, 1 infection supplémentaire par le VIH a été observée dans le groupe LEN et 3 infections supplémentaires dans le groupe F/TDF, portant le total à 15 infections incidentes par le VIH jusqu’à la fin de la phase randomisée en double aveugle : 3 dans le groupe LEN et 12 dans le groupe F/TDF. Cela correspond à une incidence actualisée du VIH de : 0,11/100 personnes-années (PA) (IC à 95 % : 0,02–0,33) dans le groupe LEN et 0,93/100 PA (IC à 95 % : 0,48–1,62) dans le groupe F/TDF (figure).
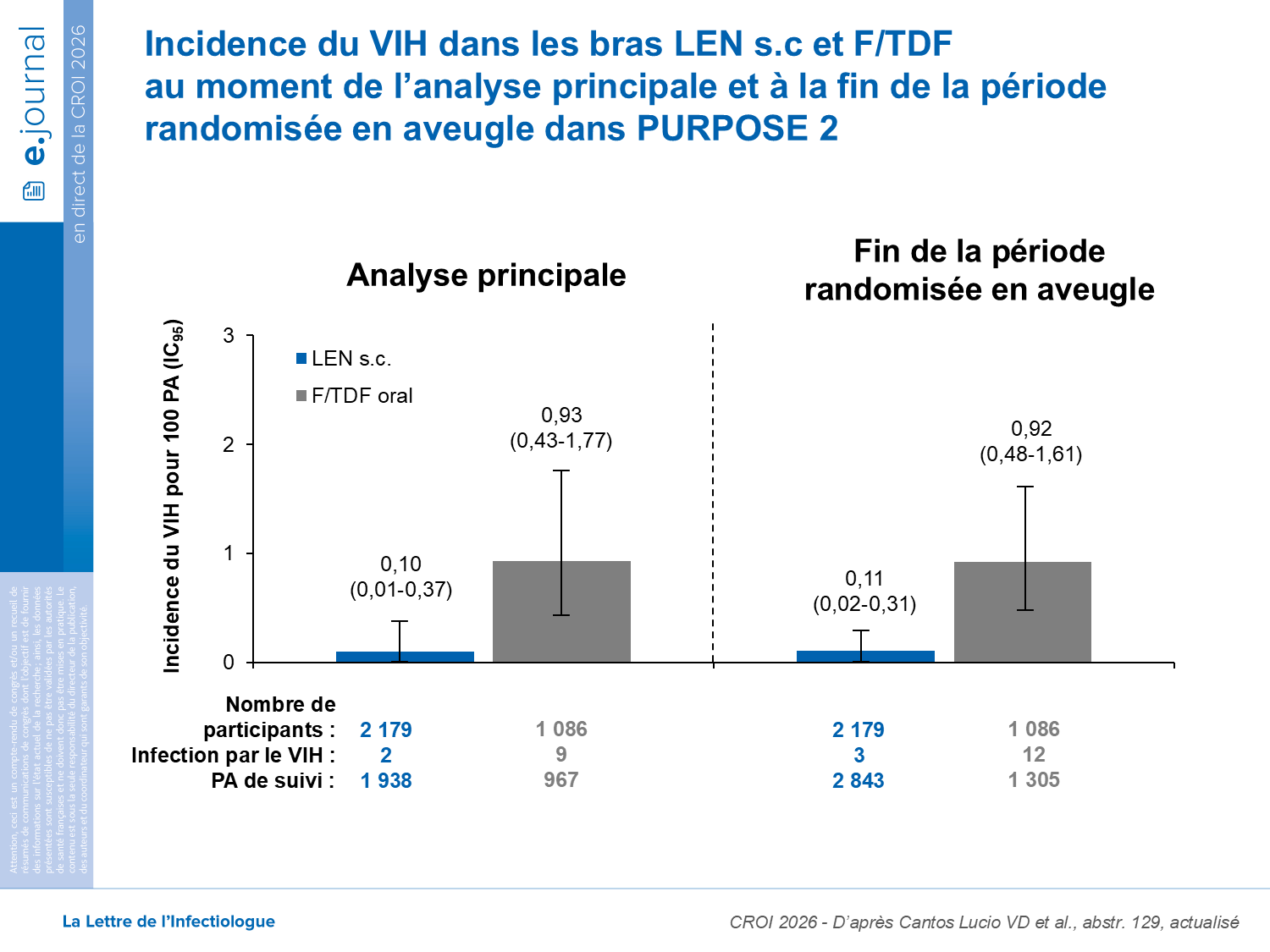
Le participant diagnostiqué avec le VIH dans le groupe LEN avait reçu sa dernière injection de LEN environ 25 semaines auparavant (toutes injections réalisées dans les temps) et présentait une concentration plasmatique de LEN de 14,2 ng/mL, légèrement inférieure à la concentration cible correspondant au quotient inhibiteur 4 (IQ4). Il avait des antécédents d’infection rectale à Chlamydiae et à gonocoque à S26. Aucun nouveau problème de tolérance significatif lié au LEN n’a été observé.
Parmi les participants recevant le LEN : 84,5 % ont rapporté des réactions au site d’injection (RSI) vs 70,4 % dans le groupe F/TDF + injection placeboPlacebo Substance inerte, sans activité pharmacologique, ayant la même apparence que le produit auquel on souhaite le comparer. (NDR rien à voir avec le groupe de rock alternatif formé en 1994 à Londres par Brian Molko et Stefan Olsdal.) La majorité des participants (83,9 %) ont rapporté des RSI de grade 1 ou 2, et les arrêts de traitement dus aux RSI sont restés faibles (1,2 %) jusqu’à la fin de la phase randomisée en double aveugle.
Au total, dans cette analyse incluant des données à plus long terme, le LEN administré par voie sous-cutanée (SC) deux fois par an est resté sûr et hautement efficace pour la prophylaxie pré-exposition (PrEP) contre le VIH chez les hommes cisgenres et les personnes de genre divers ayant des rapports sexuels avec des hommes.
Dr Jean-Philippe Madiou
Analyse de la résistance au lénacapavir dans les essais PURPOSE 1 et 2
D’après Cox S et al. Abstr. 130 actualisé
Le lénacapavir (LEN), inhibiteur de capside, administré deux fois par an en sous-cutanée a démontré en stratégie de PrEP, son efficacité et sa tolérance dans les essais randomisés, en aveugle de phase 3 (PURPOSE 1 et 2).
Le dépistage de l’infection a été effectué à l’inclusion par un test de charge viraleCharge virale La charge virale plasmatique est le nombre de particules virales contenues dans un échantillon de sang ou autre contenant (salive, LCR, sperme..). Pour le VIH, la charge virale est utilisée comme marqueur afin de suivre la progression de la maladie et mesurer l’efficacité des traitements. Le niveau de charge virale, mais plus encore le taux de CD4, participent à la décision de traitement par les antirétroviraux. et des tests rapides de dépistage puis au cours du suivi par des tests de dépistage. L’analyse de la résistance génotypique a été réalisée chez tous les participants ayant été infectés par le VIH-1 pendant la phase randomisée et en aveugle des 2 études et avec une charge virale supérieure à 200 copies/mL.
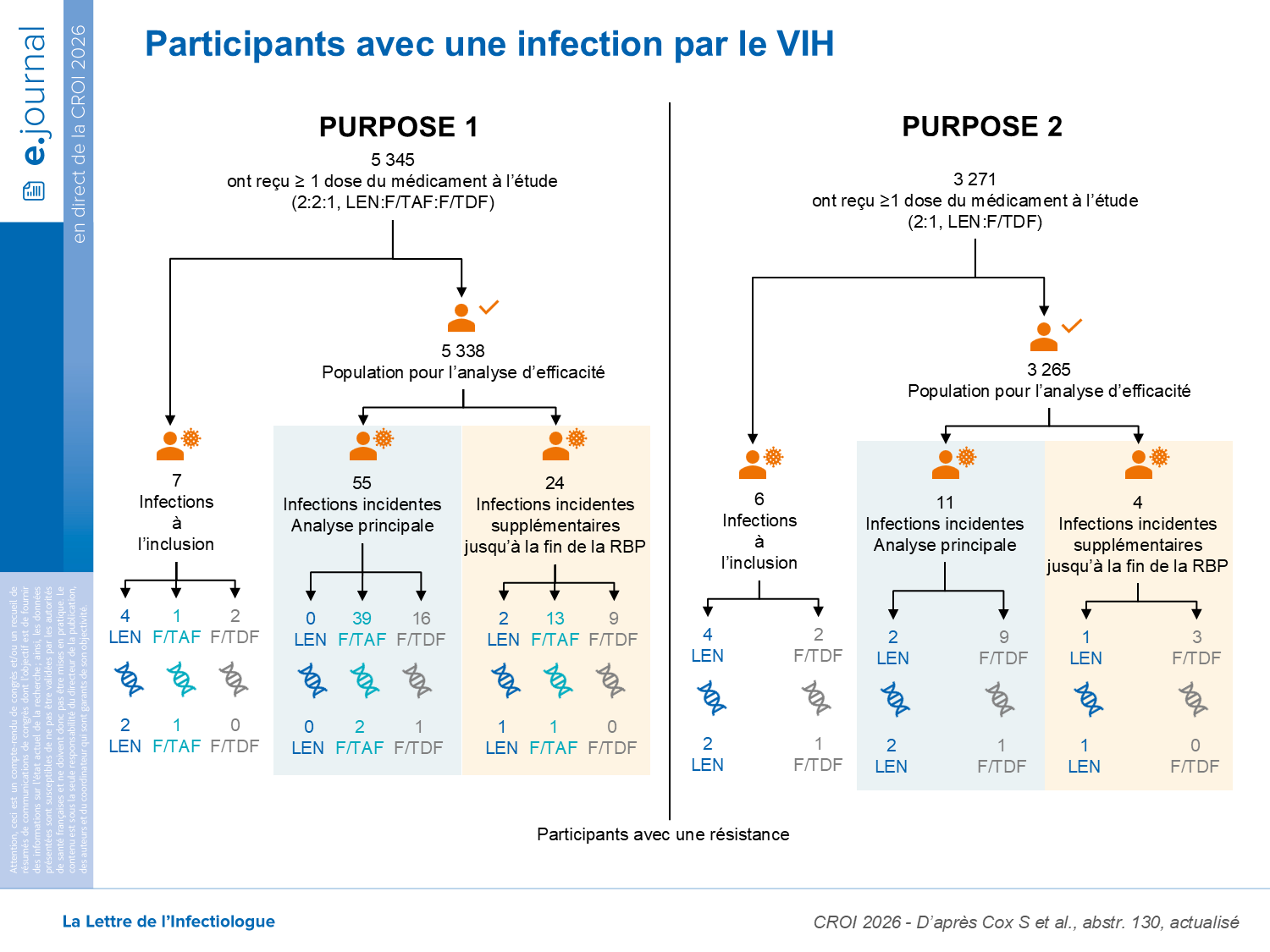
Depuis les analyses primaires d’efficacité de PURPOSE 1 et 2, l’infection par le VIH-1 dans le bras LEN a été diagnostiquée chez deux participants dans PURPOSE 1 (à S52 et à S95) et chez un autre dans l’étude PURPOSE 2 (à S52); ce qui donne au total 5 infections sous LEN : 2 dans PURPOSE 1 et 3 dans PURPOSE 2. L’analyse génotypique de la capside a montré la présence de la mutation N47D associée à la résistance au LEN dans 3 infections et l’association Q67H, K70R dans une autre infection. Ces mutations ont été acquises sous la monothérapie du LEN. Chez les patients jamais traités par LEN, la mutation N47D est rarement retrouvée quel que soit le sous-type, permettant d’écarter un risque de résistance transmise pour le futur.
Sur les 89 infections acquises sous F/TAF ou F/TDF, la résistance a été observée chez 5 cas avec la M184V/I identifiée chez 4 participants (3 F/TAF ; 1 F/TDF), et l’association K65R et M184I chez 1 participant.
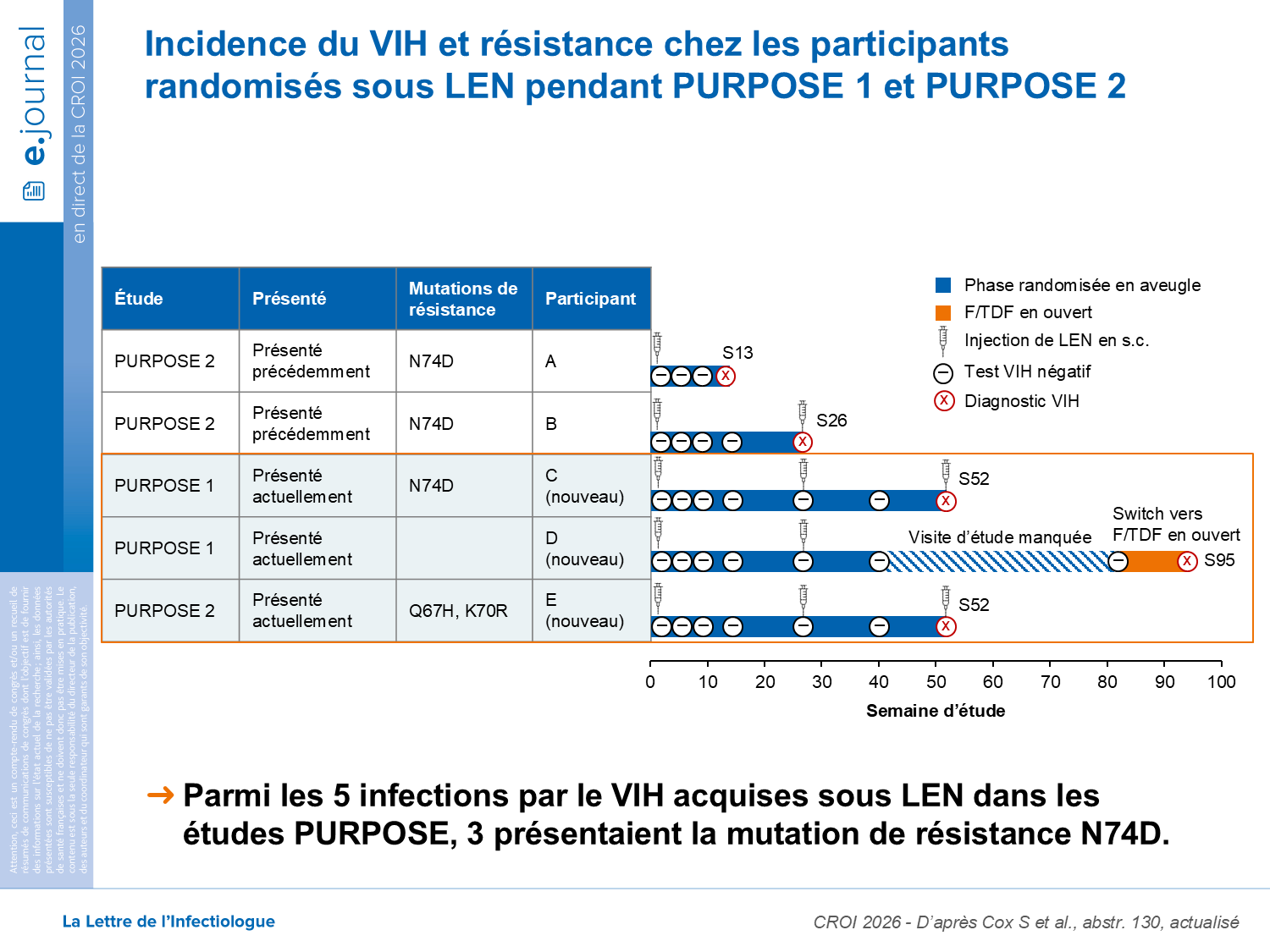
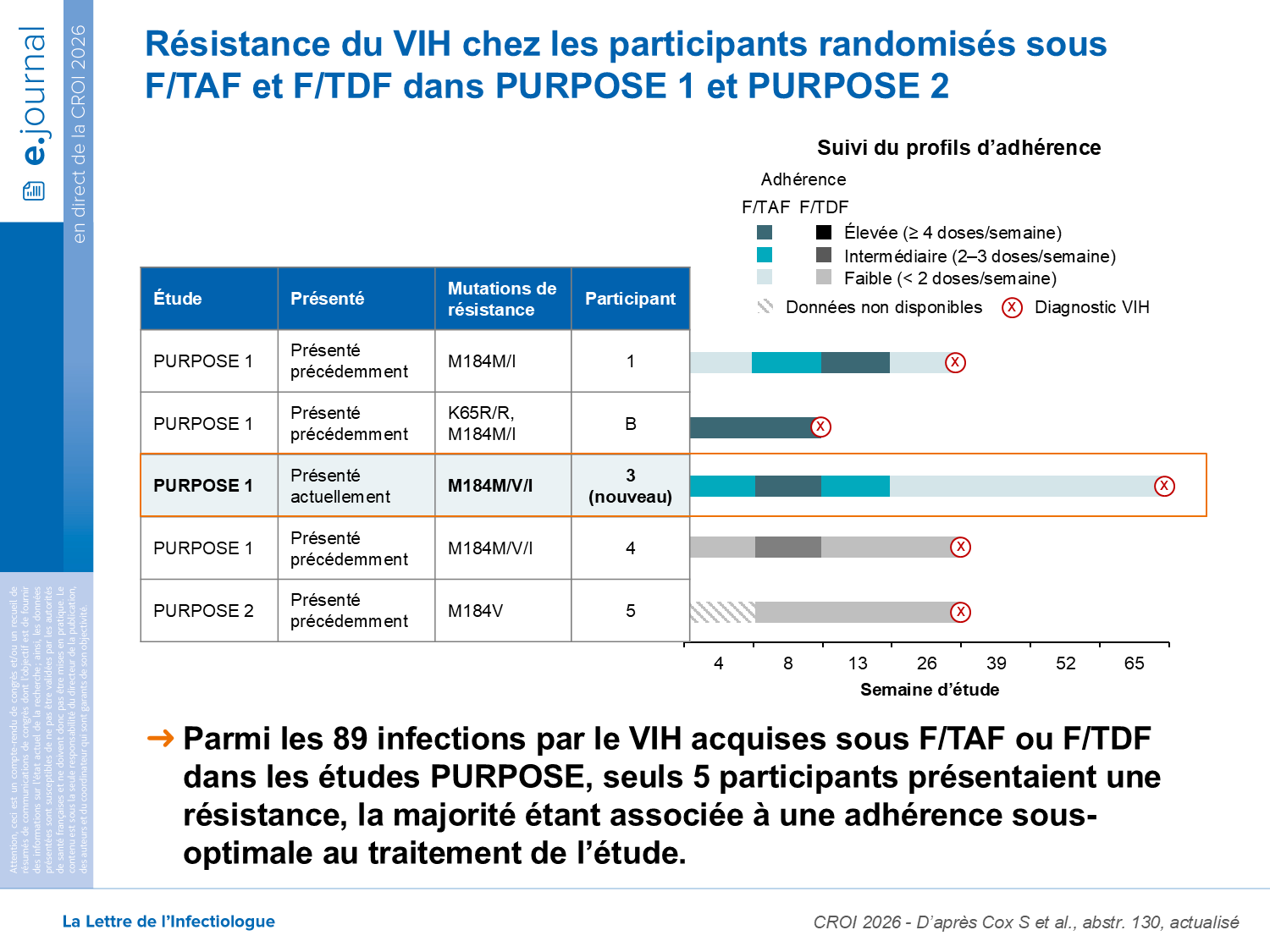
La résistance au LEN est observée dans le contexte d’une monothérapie fonctionnelle, un schéma retrouvé sous cabotégravir en PreP.
Pr Laurence Morand-Joubert
PURPOSE-1 : actualisation des données d’incidence du VIH et de tolérance
D’après Ndlovu N et al. Abstr. 128 actualisé
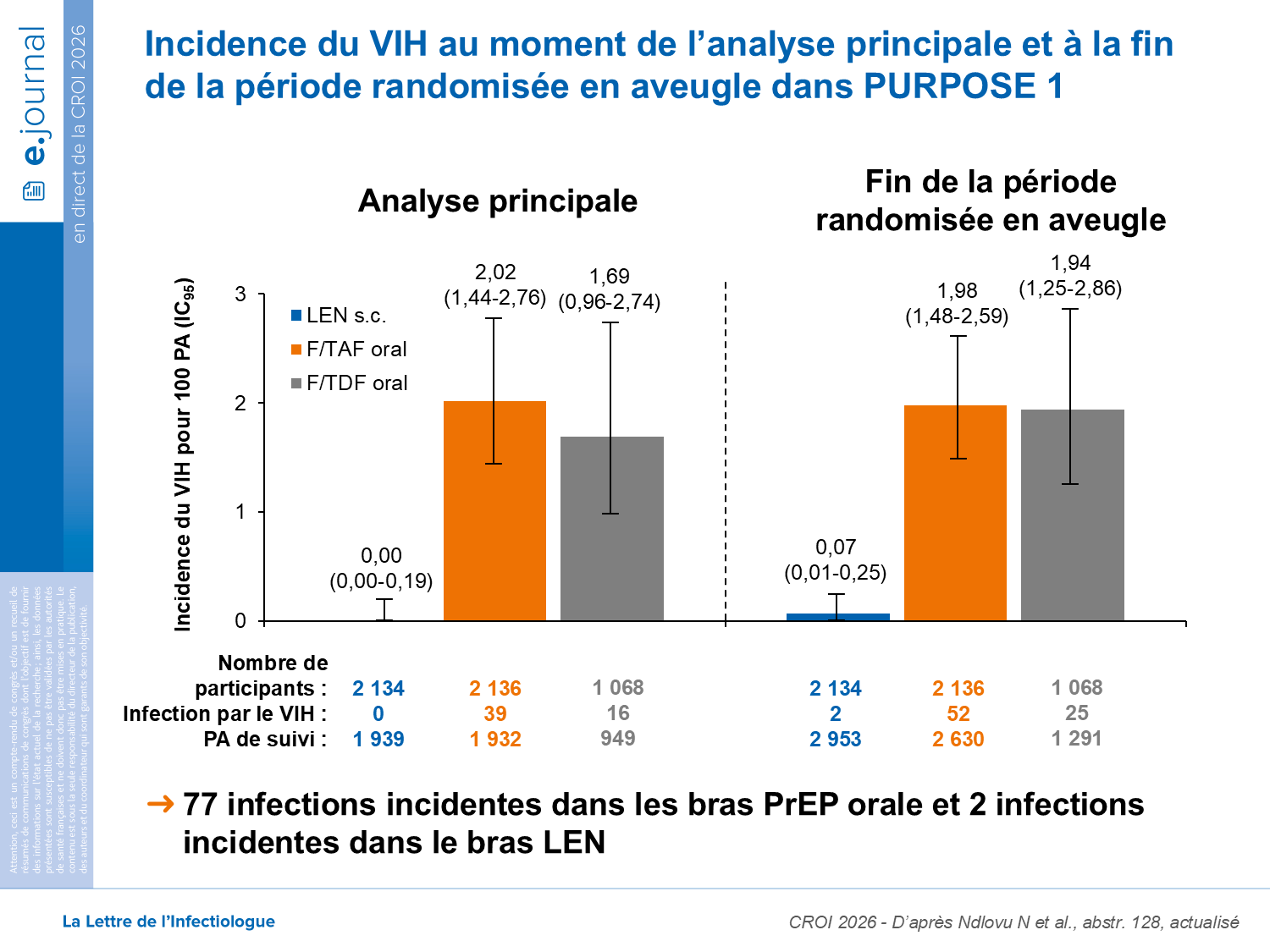
Parmi les 5338 participantes, femmes cis, initialement séronégatives pour le VIH et participant à l’essai de PrEP par le lénacapavir PURPOSE-1, 23 infections supplémentaires par le VIH ont été observées après l’analyse principale. Parmi celles-ci : 2 dans le groupe LEN, 13 dans le groupe F/TAF et 8 dans le groupe F/TDF. Au total, 79 infections incidentes par le VIH ont été observées jusqu’à la fin de la phase randomisée en double aveugle – correspondant à 2 054 Personnes/Années supplémentaires de suivi.
Parmi les deux participantes assignées au groupe LEN ayant présenté une infection incidente par le VIH :
- La participante C :
- A reçu toutes les injections de LEN dans les délais
- Dernière dose administrée 182 jours avant le diagnostic
- Concentration plasmatique de LEN au moment du diagnostic : 44,6 ng/mL
- Supérieure au quotient inhibiteur cible 4 (IQ4)
- La participante D :
- A reçu sa dernière injection de LEN 487 jours avant le diagnostic
- Concentration plasmatique de LEN au diagnostic : 0,65 ng/mL
- Inférieure à l’IQ4 cible
Aucun nouveau signal de sécurité concernant le LEN n’a été rapporté. L’incidence des réactions au site d’injection (RSI) dans le groupe LEN était similaire à celle observée lors de l’analyse principale, sans nouveaux arrêts de traitement dus aux RSI. En conclusion, Dans cette analyse actualisée avec un suivi plus long, le LEN administré par voie sous-cutanée (SC) deux fois par an est resté sûr, bien toléré et hautement efficace pour la prophylaxie pré-exposition (PrEP) contre le VIH chez les femmes cisgenres.
Dr Jean-Philippe Madiou
Conclusion
Avec un suivi prolongé couvrant la totalité de la phase randomisée en aveugle, l’incidence du VIH sous lénacapavir reste très faible dans les deux essais : 0,07/100 personnes-années dans PURPOSE 1 (femmes cisgenres) et 0,11/100 personnes-années dans PURPOSE 2 (hommes cisgenres et personnes de genre divers ayant des rapports sexuels avec des hommes), nettement en dessous des bras PrEP orale. Le profil de tolérance est inchangé, sans nouveau signal de sécurité. L’émergence de la mutation N74D dans trois des cinq infections percées sous lénacapavir illustre le risque de sélection de résistance inhérent à une monothérapie fonctionnelle, un phénomène déjà décrit avec le cabotégravir en PrEP. La rareté de cette mutation dans la population virale naïve de traitement limite pour l’heure le risque de résistance transmise. Les phases d’extension en ouvert et le suivi en vie réelle permettront de préciser ces données.
Ces trois articles ont été publiés dans le e-journal de la lettre de l’infectiologue d’Edimark, nous les reproduisons avec leur aimable autorisation.
Références
Twice-Yearly Subcutaneous Lenacapavir for PrEP: Updated HIV-1. Incidence and Safety Data in PURPOSE 1, Nkosiphile Ndlovu et al.
Lenacapavir for PrEP: HIV-1 Incidence and Safety From PURPOSE 2 at End of Randomized Blinded Phase, Valeria D. Cantos Lucio et al.
Resistance Analyses of the PURPOSE Studies Through the End of the Randomized Blinded Phase, Stephanie Cox et al.
Kelley CF et al. N Engl J Med 2025 ;392 :1261-76
Bekker LG et al. N Engl J Med 2024 ;391 :1179-92
