«Le lénacapavir, premier inhibiteur de capside du VIH-1, est désormais indiqué (aux États-Unis) en prophylaxie préexposition (PrEP) pour réduire le risque d’infection par le VIH-1 par voie sexuelle chez les adultes et les adolescents pesant au moins 35 kg à risque de contamination. Les personnes doivent avoir un test VIH-1 négatif avant de commencer le traitement par le lénacapavir», annonce le laboratoire Gilead.
Le lénacapavir en prévention du VIHVIH Virus de l’immunodéficience humaine. En anglais : HIV (Human Immunodeficiency Virus). Isolé en 1983 à l’institut pasteur de paris; découverte récemment (2008) récompensée par le prix Nobel de médecine décerné à Luc montagnier et à Françoise Barré-Sinoussi. est disponible aux États-Unis après le feu vert de la FDA en PrEPPrEP Prophylaxie Pré-Exposition. La PrEP est une stratégie qui permet à une personne séronégative exposée au VIH d'éliminer le risque d'infection, en prenant, de manière continue ou «à la demande», un traitement anti-rétroviral à base de Truvada®. sous le nom de Yeztugo® au prix, comme en thérapeutique, de 28 218 dollars annuels, pour les deux injections sous-cutanées (SC) semestrielles. Comme pour d’autres molécules, cet accès va creuser un peu plus les inégalités d’accès à la PrEP aux États-Unis, à commencer par la population afro-américaine.
Le lénacapavir est en cours d’évaluation accélérée à l’EMA, l’agence européenne du médicament, depuis février 2025. Cette molécule antirétrovirale à longue durée d’action, le lénacapavir, est déjà autorisée dans plusieurs pays pour le traitement du VIH multirésistant chez les adultes, en association avec d’autres antirétroviraux; donc une niche concernant quelques centaines de PVVIHPVVIH Personne vivant avec le VIH en France. Par exemple, à l’échelon d’un service comme celui de l’hôpital Tenon (où travaille Gilles Pialoux), c’est moins de dix PVVIH sur 3000.
Son mécanisme d’action en plusieurs étapes se distingue des autres classes d’agents antiviraux actuellement approuvées. Le lénacapavir est conçu pour inhiber le VIH à plusieurs étapes de son cycle et n’a pas de résistance croisée connue avec d’autres classes de médicaments existantes. Il est d’ailleurs certains experts pour réclamer, sans que cela soit industriellement audible, que le lénacapavir soit réservé à la PrEP pour ne pas induire de résistances dans cette nouvelle classe thérapeutique.
Le prix, un obstacle majeur aujourd’hui
Des négociations sont en cours depuis des mois pour fixer un prix acceptable dans les pays à revenu faible ou intermédiaire (voir notre article).
Gilead a d’ores et déjà négocié avec plusieurs génériqueurs et il est possible que ce médicament préventif soit disponible dans les pays émergents, en Afrique notamment, à un prix très inférieur (50 dollars ?!), et ce bien avant qu’il le soit en Europe. Ce qui serait un juste pied de nez à l’histoire du sidaSida Syndrome d’immunodéficience acquise. En anglais, AIDS, acquired immuno-deficiency syndrome. vu le temps qu’ont mis les molécules anti-VIH à descendre au-delà du détroit de Gibraltar.
Reste à savoir quel sera l’impact négatif du gel du Pepfar et de Usaid sur le plan de mise à disposition prévu par le laboratoire, avant le retour au pouvoir de Donald Trump avec la politique sanitaire que l’on sait (voir notre article). Le prix reste un obstacle majeur à son utilisation comme à celle du cabotégravir injectable en PrEP dans les pays qui ont une assurance maladie universelle comme la France ou un système comparable. Sachant que, en France, le générique de Truvada® se négocie autour des 150-180 euros la boite de 28 comprimés. Parfois moins, dans les achats hospitaliers.
Nous ne savons pas jusqu’où iront les négociations de prix en France pour qu’il soit soutenable par l’assurance maladie. Ce d’autant que le prix du cabotégravir, l’autre PrEP injectable de ViiV Healthcare qui a déjà son autorisation de mise sur le marché (AMM) en France (1 injection Intramusculaire tous les deux mois) et a reçu l’avis favorable de la Haute Autorité de Santé, n’a toujours pas été fixé, dans les négociations entre les autorités de santé (via le comité économique des produits de santé) et le laboratoire.
L’intérêt d’une offre de PrEp élargie
La France devrait disposer à terme de trois possibilités de PrEP: l’association Tenofovir/FTC (Truvada génériqué) en comprimé tous les jours ou à la demande, le cabotégravir IM bimensuel, puis un peu plus tard le lénacapavir SC semestriel. Sauf si les autorités ministérielles considèrent – c’est une éventualité – qu’il n’y a pas assez de demande pour une telle offre plurielle en France.
Le but évident de cette diversification de l’offre de PrEP n’est pas tant d’offrir un choix aux HSHHSH Homme ayant des rapports sexuels avec d'autres hommes. sous PrEP que d’augmenter considérablement les populations en prévention au-delà du HSH trente- ou quarantenaire, blanc, urbain et informé. Cible qui d’ailleurs est elle-même insuffisamment couverte eu égard au niveau d’exposition. On pense notamment aux femmes (5,7 % des initiations de PrEP et 34 % des nouveaux diagnostics), aux hétérosexuels multipartenaires, aux jeunes migrant·es, aux travailleur·euses du sexe, aux jeunes HSH.
Or, l’ouverture de la prescription de la PrEP en ville a indiscutablement permis d’augmenter le nombre de prescripteurs et de PrEpeurs mais pas de diversifier la cible. Comme l’a démontré une récente publication d’Epiphare basée sur le système national des données de santé (SNDS) dans Lancet Public Health sur l’impact de la décision d’autoriser l’initiation de PrEP en médecine de ville à partir du 1er juin 2021 (voir notre article). Pour autant, réduire le débat à la seule question du coût de la PrEP est pour le moins réducteur.
Le prix de la santé publique
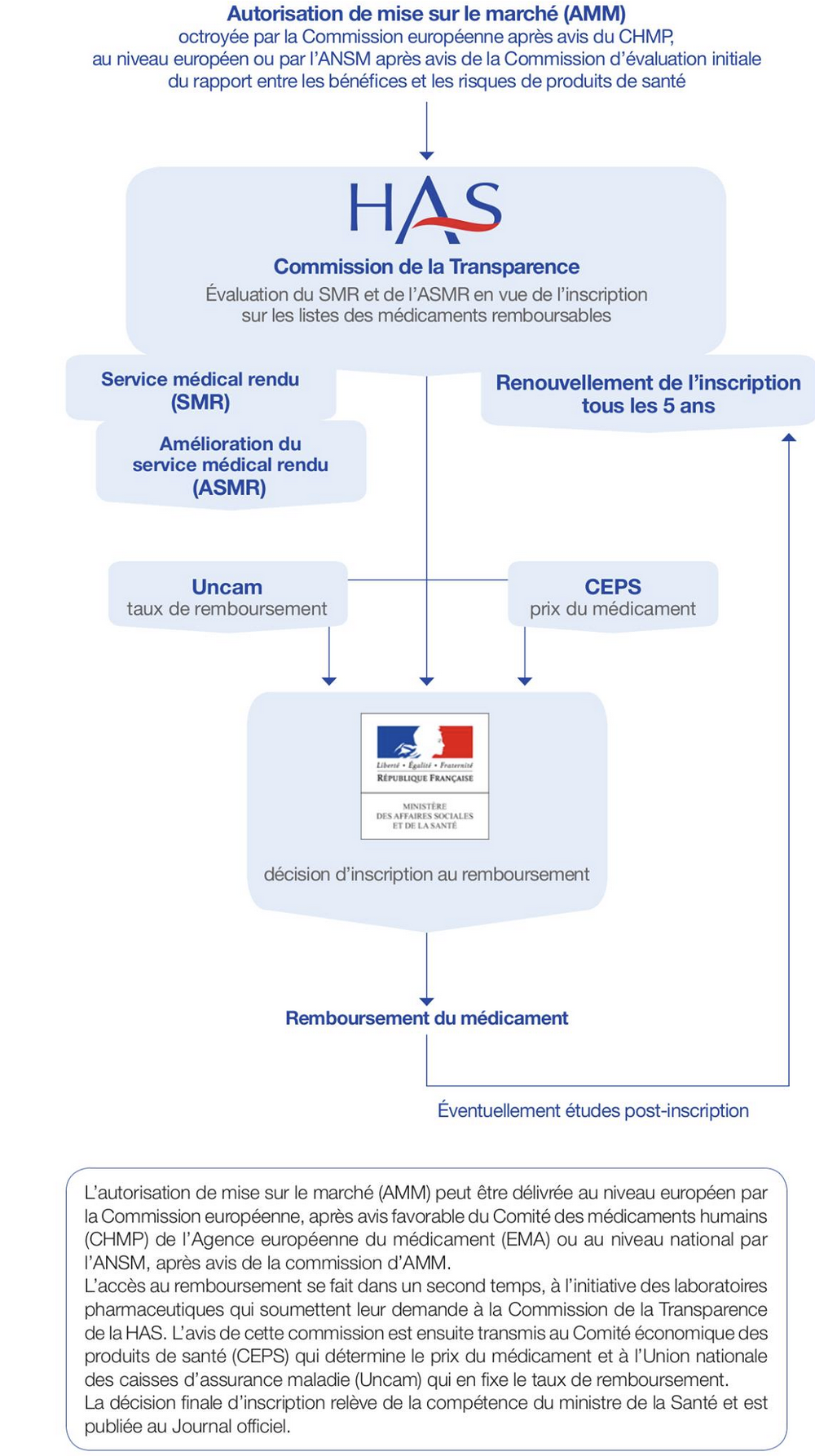
Le prix d’un médicament préventif ou thérapeutique est fixé par le comité économique des produits de santé (CEPS), en général par négociation avec l’entreprise exploitant le médicament (à défaut, par décision du comité), sur la base notamment de l’ASMR (amélioration du service médical rendu), du prix des médicaments à même visée thérapeutique (le Truvada ici), des volumes de vente envisagés – ce que l’on nomme la balance prix-volume – de la population cible et des prix pratiqués à l’étranger. Et cette balance prix-volume comme la taille de la population-cible sont au centre des négociations sur le prix de la PrEP dans les pays qui disposent d’une sécurité sociale.
La logique de santé publique en PrEP est d’accroitre le poids de la PrEP dans la prévention combinée et d’atteindre les objectifs 2030 de l’OMS ou de l’Onusida (95-95-95 et moins de 50 nouvelles contaminations par an en 2030, on est à 3650 en France pour 2023). Le prix n’est donc pas la seule clé au regard de l’aller-vers, de l’offre diversifiée, des campagnes de promotion de la PrEP hors HSH…
En France, nous savons selon les études ERAS que la moitié des HSH exposés sont sous PrEP orale, dont la moitié à la demande, et avec une excellente efficacité. Ceux qui ne prennent pas la PrEP dans cette population très exposée sont des hommes plus éloignés des codes communautaires (voir notre article) et ont peut-être des traits particuliers, notamment en littératie en santé.
Les autres populations exposées, notamment en termes populationnels, les migrants, hommes et femmes, hétérosexuels, n’en bénéficient encore que très marginalement. La situation est en train de changer avec des programmes dans des centres municipaux de santé et des centres de santé sexuelle s’adressant aux femmes (anciennement CePF). En tout état de cause, ces groupes ont un taux de nouvelles infections plus bas que les populations aujourd’hui sous PrEP, ce qui affecte aussi l’efficacité en termes de nombre de cas évités.
Dans cette période où l’objectif est l’élimination de la transmission en 2030, il n’est pas entendable de passer à côté d’une telle innovation majeure. La mesure de son impact épidémiologique ne peut venir que d’une étude d’implantation large, simple et robuste pour documenter dans la vraie vie les paramètres majeurs de sa contribution à l’objectif d’élimination.
