Safety, Pharmacokinetics, and Antiviral Activity of GS-3242, a Novel Long-Acting Injectable InSTI
Samir Gupta et al. (Gilead)
Le GS-3242 est un nouvel inhibiteur de l’intégrase conçu pour une formulation injectable à longue durée d’action. Deux études de phase 1 ont exploré sa tolérance, sa pharmacocinétique et son activité antivirale.
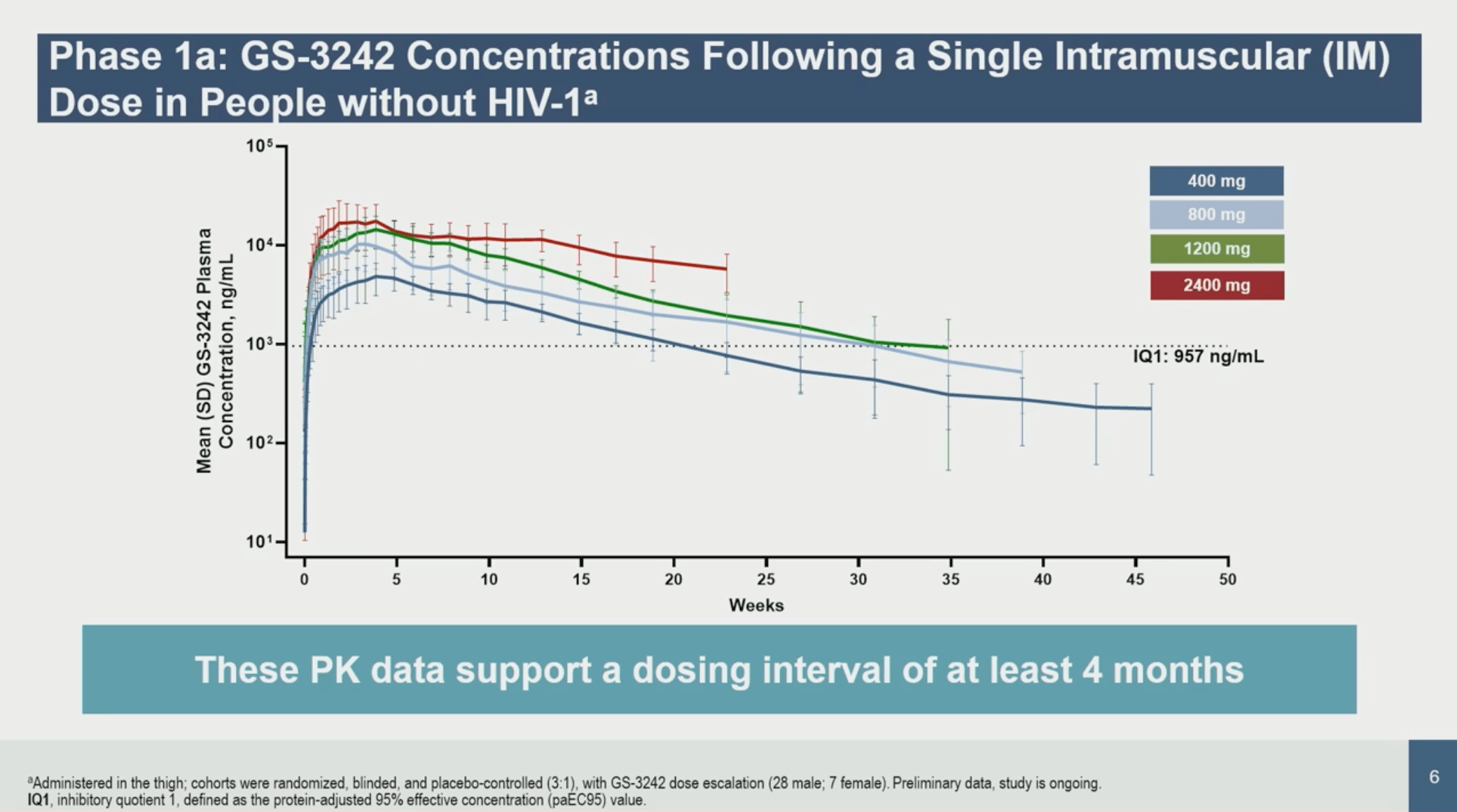
En phase 1a, une injection intramusculaire unique (doses de 400 à 2400 mg, en deux injections pour les volumes élevés) chez des volontaires séronégatifs a été globalement bien toléré, les effets secondaires rapportés étant dominés par la douleur au point d’injection, sans anomalie biologique notable.
Les profils pharmacocinétiques montrent un pic tardif (environ 3–5 semaines) et une demi-vie terminale longue(47–56 jours), avec une exposition proportionnelle à la dose. En phase 1b, une courte administration orale chez six personnes vivant avec le VIHVIH Virus de l’immunodéficience humaine. En anglais : HIV (Human Immunodeficiency Virus). Isolé en 1983 à l’institut pasteur de paris; découverte récemment (2008) récompensée par le prix Nobel de médecine décerné à Luc montagnier et à Françoise Barré-Sinoussi. (PVVIH) naïfs de traitement a été réalisée pour tester l’effet anti-viral sans avoir à les exposer sur le long terme. Cette administration a induit une baisse rapide et importante de la charge viraleCharge virale La charge virale plasmatique est le nombre de particules virales contenues dans un échantillon de sang ou autre contenant (salive, LCR, sperme..). Pour le VIH, la charge virale est utilisée comme marqueur afin de suivre la progression de la maladie et mesurer l’efficacité des traitements. Le niveau de charge virale, mais plus encore le taux de CD4, participent à la décision de traitement par les antirétroviraux. (−2,31 log10 à J11, équivalent aux autres anti-intégrases «historiques»), sans signal sur la tolérance.
Les modélisations issues de la pharmacocinétique (PK) suggèrent qu’une administration trimestrielle, voire plus espacée, pourrait être envisageable en formulation longue action.
L’étude de phase 1b se poursuit pour préciser la relation dose — réponse. L’objectif final est d’intégrer GS-3242 dans un schéma complet à longue durée d’action, en association avec un autre agent du même type.
NDR : trop tôt pour envisager une utilisation en PrEPPrEP Prophylaxie Pré-Exposition. La PrEP est une stratégie qui permet à une personne séronégative exposée au VIH d'éliminer le risque d'infection, en prenant, de manière continue ou «à la demande», un traitement anti-rétroviral à base de Truvada®.
Injectable HIV-1 Capsid Inhibitor VH4011499 (VH-499) Formulation Supports Ultra-Long- Acting Dosing
Nilay Thakkar et al. (ViiV)
Le VH-499 est un inhibiteur de la capside du VIH-1 en développement pour une formulation injectable à très longue durée d’action. Cette première étude de phase 1 chez l’humain explore sa tolérance et sa pharmacocinétique après une dose unique intramusculaire ou sous-cutanée, chez des volontaires séronégatifs.
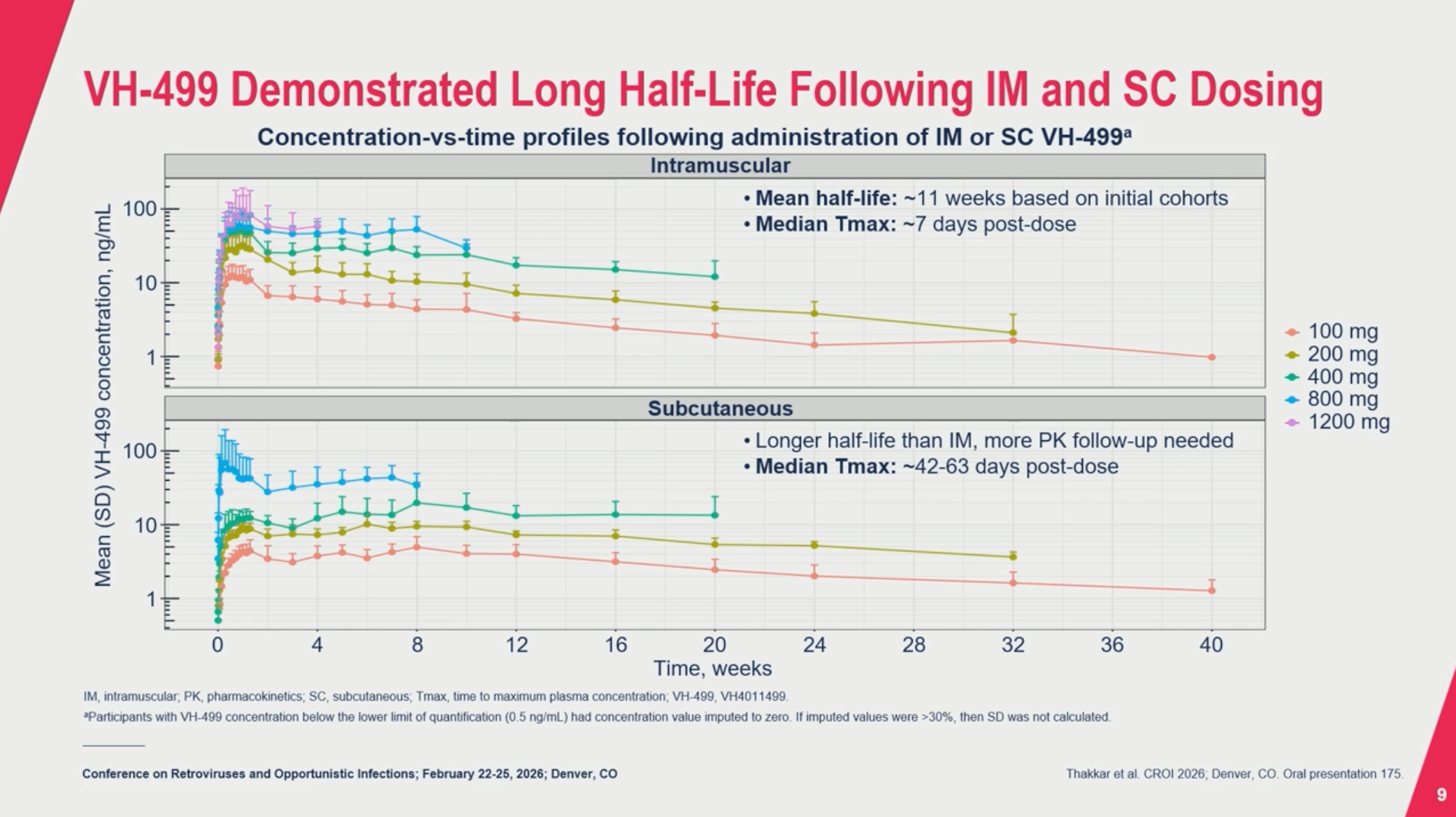
Quarante-huit participants ont reçu 100 à 800 mg de VH-499 ou un placeboPlacebo Substance inerte, sans activité pharmacologique, ayant la même apparence que le produit auquel on souhaite le comparer. (NDR rien à voir avec le groupe de rock alternatif formé en 1994 à Londres par Brian Molko et Stefan Olsdal.) La tolérance apparaît correcte, avec des effets indésirables majoritairement légers à modérés, dominés par les réactions au site d’injection. Ces réactions, surtout la douleur, sont relativement brèves (1 à 3 jours) et nettement plus fréquentes en sous-cutané qu’en intramusculaire. Aucun événement indésirable grave ni arrêt pour motif de sécurité n’a été observé.
Sur le plan pharmacocinétique, l’absorption est nettement plus lente en sous-cutané, avec un Tmax autour de 112 jours, contre 7 à 18 jours en intramusculaire. Les pics de concentration sont plus faibles en sous-cutané, mais avec une élimination extrêmement lente, empêchant pour l’instant d’estimer la demi-vie terminale. Ces premiers résultats suggèrent un potentiel d’administrations très espacées, possiblement ≥4 mois. Les prochaines étapes reposeront sur des données PK avec plus de recul et une modélisation pour optimiser le schéma et la stratégie de développement. Le choix se fera alors pour les essais suivants sur la dose et les modalités d’administration.
Pharmacokinetics and Evaluation of Potential Dosing Regimens for Long-Acting VH4524184
Hyunmoon Backet al. (ViiV)
Le VH-184 est un nouvel inhibiteur de l’intégrase de troisième génération, conçu pour conserver une activité malgré certaines résistances, avec un développement en formulation injectable longue durée d’action.
Cette étude de phase 1, en double aveugleDouble aveugle L'étude avec répartition aléatoire, randomisé ou en double insu (ou en double aveugle) est une démarche expérimentale utilisée en recherche médicale et pharmaceutique faisant que ni le patient ni le médecin ne sait quel traitement est pris : traitement A ou B, traitement A ou placébo. contre placebo, évalue chez des volontaires séronégatifs la tolérance et la pharmacocinétique de deux formulations (A et B) et de de deux modes d’administration, SC et IM, avec un suivi jusqu’à 52 semaines…
La tolérance apparaît globalement bonne chez les 39 participants, avec des réactions au site d’injection le plus souvent légères, dominées par l’érythème, la douleur et des nodules, et seulement deux événements de grade 3. La formulation A atteint rapidement son pic (environ 3 jours) et présente une demi-vie terminale d’environ 7 semaines après injection SC. La formulation B, à absorption plus lente, montre un profil plasmatique très «plat» jusqu’au 7ème mois, empêchant encore d’estimer sa demi-vie terminale.
L’intégration des données dans un modèle de PK populationnel permet de simuler des schémas d’administration, avec des injections qui pourraient être mensuelles ou bimestrielles pour la formulation A, et potentiellement semestrielles pour la formulation B. L’ensemble du profil de sécurité ressemble à celui des INSTI déjà disponibles.
Ces résultats soutiennent le développement de VH-184 en longue action avec les essais de phase 2b (INOVATE)
DOR/ISL (100/0.25 mg) vs BIC/FTC/TAF for Initial HIV-1 Therapy: Week 48 Results of a Phase III Study
Juergen K. Rockstroh et al pour MSD
Cette étude de phase 3 en double aveugle évalue l’association doravirine/islatravir (DOR/ISL) comme traitement initial du VIH-1, comparée au schéma de référence BIC/FTC/TAF. Plus de 500 adultes naïfs d’antirétroviraux, ont été randomisés entre les deux stratégies.
À 48 semaines, DOR/ISL atteint un taux de suppression <50 copies/mL (91,8 %) comparable à BIC/FTC/TAF (90,6 %), démontrant la non-infériorité. Les résultats sont identiques chez les participants ayant une charge virale élevée, y compris > 500 000 copies/mL. Les échecs virologiques sont rares; sous DOR/ISL, deux cas ont sélectionné des mutations conférant une résistance à la doravirine tout en conservant la sensibilité à l’islatravir, sur fond de virémie initiale >1 million et de mutations préexistantes non excluantes (dans un des deux cas, il semble qu’il y ait eu des problèmes d’observance avec des taux médicamenteux bas, mais les données n’ont pas été montrées ici).
Aucun signal de résistance émergente n’a été observé dans le bras BIC/FTC/TAF parmi les participants testés. La restauration immunologique (CD4) et les paramètres hématologiques étaient similaires entre groupes. La tolérance est globalement comparable, avec peu d’arrêts pour effets indésirables. Une prise de poids modérée et non différente dans les deux bras.
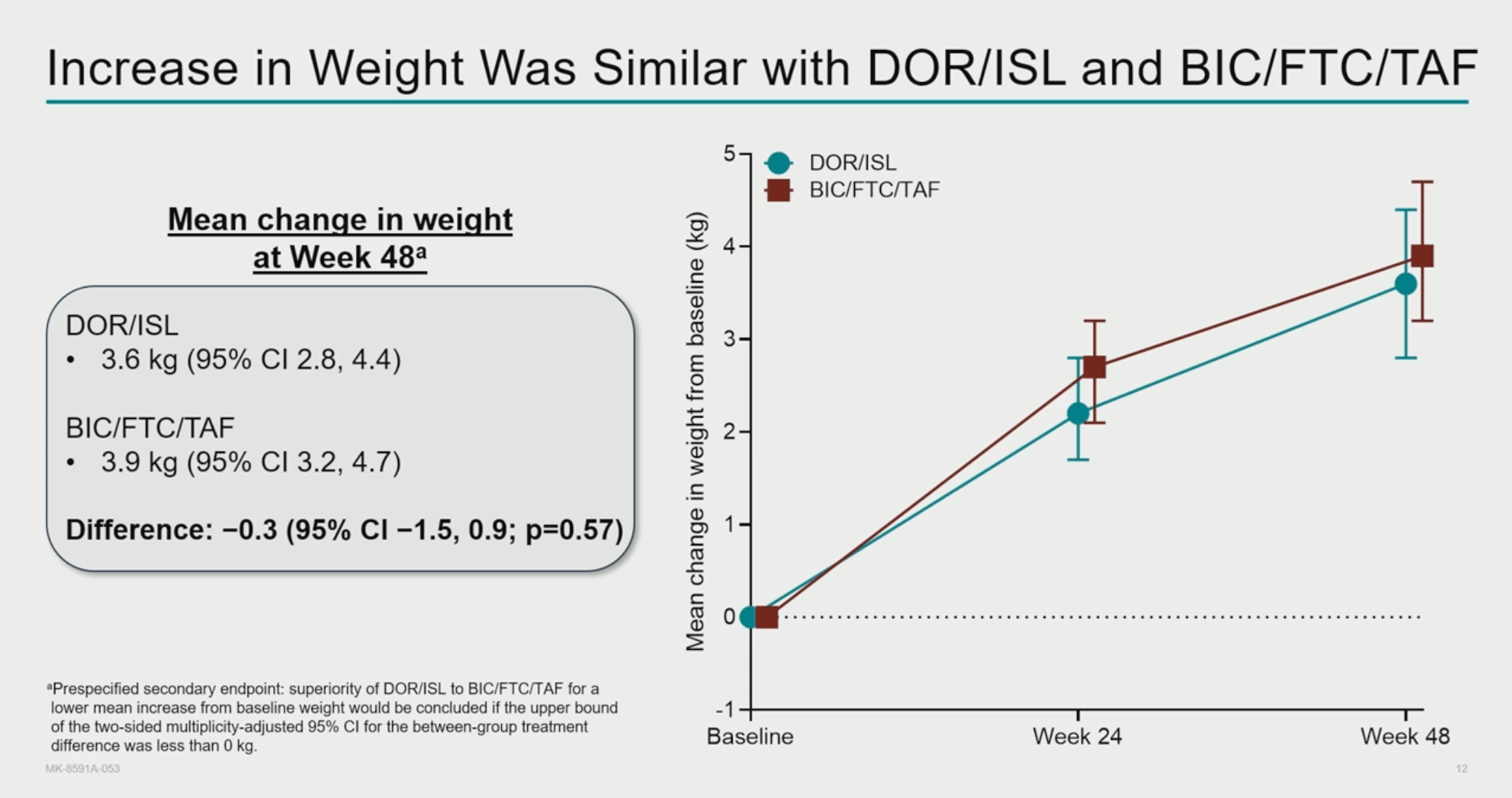
Au total, DOR/ISL apparaît comme une option efficace et bien tolérée en initiation, avec une vigilance particulière en cas de très forte charge virale et de résistances basales de la transcriptase inverse. Ces données confortent le potentiel de ce duo comme alternative aux trithérapies classiques à base d’intégrase.
NDR : les résultats sont encourageants avec une bonne alternative quand on ne souhaite pas utiliser d’anti-intégrase ou de TDF/TAF en initiation de traitement. On est un peu déçu par les courbes de prise de poids identiques dans les deux bras, il sera intéressant de voir les résultats à plus long terme, si au-delà de 12 mois la prise de poids se différencie dans la mesure où le suivi sera de 3 ans. On sait que le déficit immunitaire sévère est un facteur de risque de prise de poids et ici près de 20% des patients avaient des CD4<200. Mais avec une prise quotidienne, l’alternative DOR-3TC actuellement testée dans MODULO en traitement d’entretien sera certainement une option moins coûteuse que cette bithérapie, avec plus de recul avec la lamivudine qu’avec l’islatravir ! Par ailleurs, comme cela a été discuté plus tard dans la journée, la proposition d’un nouveau traitement en comprimé journalier n’est pas vraiment une révolution…
Maintenance of HIV Suppression at 12 Months With VH3810109 (N6LS) Q4M + CAB LA QM: The EMBRACE Study
Charlotte-Paige Rolle et al.
EMBRACE évalue une stratégie de maintenance ultra-longue action combinant l’anticorps neutralisant N6LS, administré tous les 4 mois, et le cabotégravir injectable mensuel.
L’étude inclut des adultes avec CV<50 cop/mL et sélectionnés sur une sensibilité phénotypique au N6LS. Les participants ont été randomisés vers N6LS IV + CAB LA, N6LS SC + CAB LA, ou la poursuite du traitement standard.
À 12 mois, la proportion de rebond virologique (≥50 copies/mL) reste faible, mais légèrement plus élevée avec N6LS SC (10 %) qu’avec N6LS IV (6 %), et proche de comparaisons historiques (4 %). Les échecs virologiques confirmés suivent la même tendance (4% IV, 6% SC, 4% SOC).
Sur le plan de la tolérance, les arrêts pour effets indésirables sont plus fréquents dans le bras SC, même si les événements attribués au N6LS restent rares. Les réactions sévères au site d’administration sont absentes en IV, mais touchent 16% des participants en SC, constituant la principale différence en termes de tolérance. Malgré cela, l’acceptabilité rapportée demeure élevée dans les deux bras. Globalement, N6LS IV apparaît comme la modalité la mieux tolérée pour une administration trimestrielle, tout en maintenant une suppression virologique élevée.
Ces résultats soutiennent la poursuite du développement d’approches combinées anticorps/anti-intégrase sous réserve d’une sélection préalable sur la sensibilité au bNAb.
La 2nde phase de l’essai comportera des injections IV de N6LS tous les six mois et de CAB IM tous les deux mois.
Safety and Antiviral Effect of 10E8.4/Ibalizumab in People With HIV: A Phase Ib Trial
T. Crowell for the RV584 Study Group. L’orateur Marco T. Missanga initialement prévu n’a pu se rendre au congrès du fait des limitations de visa.
Cet essai de phase 1b mené en Tanzanie évalue un anticorps bispécifique, 10E8.4/ibalizumab, conçu pour neutraliser le VIH en ciblant à la fois l’enveloppe virale (MPER) et le récepteur CD4.
Vingt adultes vivant avec le VIH, naïfs de TAR ou hors traitement depuis plusieurs mois, ont été répartis en cinq bras recevant soit un traitement oral standard, soit une dose unique de 10E8.4/iMab, à différentes doses et voies (IV ou IM), avec un bras combinant VRC07-523LS.
La tolérance est globalement satisfaisante, dominée par des événements légers à modérés de réactogénicité systémique. Deux événements sévères et deux événements graves (cytolyse) ont été observés dans un bras, mais jugés non liés et résolutifs sans intervention.
Un effet antiviral est constaté dans tous les groupes entre J0 et J14, sans différence statistiquement significative entre les bras. Les baisses de charge virale sont donc compatibles avec une activité rapide, mais la petite taille des groupes limite les comparaisons. Les concentrations sériques de l’anticorps culminent précocement puis décroissent sur deux semaines. Après J14, tous les participants des bras anticorps ont repris un TAR standard.
L’ensemble suggère que 10E8.4/iMab a une activité antivirale comparable à un traitement oral sur le court terme, et bien toléré, y compris en injection intramusculaire. Ces résultats soutiennent la poursuite du développement des bNAbs.
Sustained DNA-Encoded SARS-CoV-2 Antibody Expression and Safety Through 96 Weeks
Pablo Tebas et al.
Cette étude de phase 1 explore une approche innovante consistant à faire produire des anticorps neutralisants directement par l’organisme via l’injection de plasmides d’ADN (DMAb), délivrés par électroporation CELLECTRA™. Il s’agit de la première étude de ce type chez l’humain.
Des volontaires sains ont reçu, par voie intramusculaire et électroporation, de l’ADN codant deux anticorps anti-SARS-CoV-2 à demi-vie prolongée. Le suivi, prolongé jusqu’à 96 semaines, constitue le plus long rapporté pour cette technologie en clinique. La tolérance est favorable, avec principalement des réactions locales transitoires au point d’incorporation (douleur, érythème) et aucun événement indésirable grave attribué au produit. Les anticorps exprimés in vivo étaient détectables chez tous les participants évaluables et persistaient jusqu’à 96 semaines. Les concentrations maximales augmentaient lorsque l’administration se faisait sur plusieurs sites, dépassant parfois 1 μg/mL.
Fait marquant, l’expression reste stable entre les semaines 72 et 96, suggérant une durabilité exceptionnelle. Les anticorps produits conservent une activité fonctionnelle, avec liaison aux RBD de variants majeurs de SARS-COV2 et neutralisation de pseudovirus chez tous les participants évaluables.
Aucun anticorps anti-médicament n’a été confirmé malgré un grand nombre d’échantillons testés, ce qui renforce la faisabilité à long terme. L’ensemble soutient le potentiel des DMAb comme plateforme «synthétique» et non virale de délivrance prolongée d’anticorps, applicable au-delà des infections respiratoires.
Le papier est publié ce jour: Tebas et al. Nature Medicine 2026.
Phase III Efficacy and Safety of Switch From Complex Regimen to Single-Tablet BIC/LEN in ARTISTRY-1
Chloe M. Orkin et al.
ARTISTRY-1 évalue une nouvelle stratégie en un comprimé par jour associant bictégravir et lénacapavir pour simplifier le traitement de PVVIHPVVIH Personne vivant avec le VIH ayant un traitement avec un des schémas complexes.
L’essai inclut une population âgée et très prétraitée, souvent polymorbide, prenant plusieurs comprimés quotidiens et majoritairement sous inhibiteur de protéase. Les participants, tous en suppression virologique, ont été randomisés pour passer au STR BIC/LEN ou poursuivre leur traitement habituel. À 48 semaines, les rebonds virologiques étaient rares et comparables entre les 2 groupes, démontrant la non-infériorité de la stratégie de switch vers le comprimé de BIC/LEN. La proportion de charge virale indétectable restait très élevée, sans émergence de résistance.
Les effets indésirables attribués au traitement étaient plus fréquents après switch vers BIC/LEN, mais les événements sévères ou graves demeuraient exceptionnels. On note une amélioration des paramètres lipidiques.
Au-delà de l’efficacité, la simplification s’est traduite par une amélioration nette de la satisfaction des patients, ce qui est central dans une population exposée à la fatigue thérapeutique (la moyenne de traitement antivirale est proche de 30 ans). L’étude suggère ainsi qu’un schéma simplifié peut maintenir le contrôle virologique chez des patients dans des situations virologiques complexes et avec d’importantes comorbidités.
Le papier est publié ce jour également: Orkyn et al. Lancet HIV 2026.
NDR : L’essai BIC/LEN pour simplifier les traitements est un vrai progrès. Avec le point, tout de même, que pas mal de données montrent que l’on peut être efficace avec un régime de type TLD ou Biktarvy chez des personnes ayant un haut niveau de résistance au INTIINTI Les inhibiteurs nucléosidiques de la transcriptase inverse du VIH ou INTI, sont des composés de synthèse utilisés dans le traitement du VIH et des hépatites. sans l’aide du LEN… Mais pour les patients âgés et multimorbides, se passer du TDF/TAF est tout de même pas mal!.
Référence
Session de communications orales libres : Antiviraux à longue durée d’action, CROICROI «Conference on Retroviruses and Opportunistic Infections», la Conférence sur les rétrovirus et les infections opportunistes annuelle où sont présentés les dernières et plus importantes décision scientifiques dans le champs de la recherche sur le VIH. 2026.
Cet article a été publié sur le site du CoReSS Bretagne, nous le reproduisons ici avec l’aimable autorisation de son auteur.
