Implants Releasing NRTTI MK-8591 Fail to Protect Macaques Against SHIV Containing the M184V Mutation
Charles Dobard, et al.
Des implants du type de ceux utilisés en contraception ont été développés pour être chargés en islatravir, un inhibiteur non nucléosidique de la transcriptase du VIHVIH Virus de l’immunodéficience humaine. En anglais : HIV (Human Immunodeficiency Virus). Isolé en 1983 à l’institut pasteur de paris; découverte récemment (2008) récompensée par le prix Nobel de médecine décerné à Luc montagnier et à Françoise Barré-Sinoussi. L’étude cherche à répondre à trois questions: faisabilité, tolérance et efficacité. L’un des enjeux est que la sensibilité du VIH à l’ISL diminue d’un facteur 10 en présence de la mutation M184V, qui est l’une des plus courantes pour les virus circulant actuellement (NDR : cf. plus loin dans cette session les présentations sur le lénacapavir en PrEPPrEP Prophylaxie Pré-Exposition. La PrEP est une stratégie qui permet à une personne séronégative exposée au VIH d'éliminer le risque d'infection, en prenant, de manière continue ou «à la demande», un traitement anti-rétroviral à base de Truvada®. où tous les patients qui s’infectent sous lénacapavir ont un virus porteur de cette mutation).
Onze macaques ont bénéficié de la mise en place d’un implant d’ISL, six macaques ont été exposés (8 expositions sur 2 mois) par voie anale à un virus SHIV sauvage et cinq à un virus ayant une mutation M184V.
Du point de vue pharmacologique, si les taux plasmatiques sont assez faibles, les taux dans les PBMC restent élevés, et dans les concentrations attendues pour être efficace en prévention pendant toute la durée de l’exposition.
Du point de vue efficacité, l’implant d’ISL protège mal contre les virus porteurs de la mutation M184V: alors qu’aucun des six macaques exposés au virus sauvage ne s’infecte, trois/5 macaques surexposés au virus mutés s’infectent, après en moyenne 3 expositions.
MK-8527 Phase III Dose Selection for Monthly Oral HIV-1 Preexposure Prophylaxis
Yash Kapoor et al. (MSD)
Le MK-8527 est un INTI de nouvelle classe, inhibant la translocation, avec la caractéristique d’une demi-vie longue permettant une administration mensuelle. Les données de 408 participants à des études antérieures dont 37 PVVIHPVVIH Personne vivant avec le VIH ont été rassemblées afin d’alimenter un modèle permettant de déterminer la dose la plus adaptée aux essais de phase 3. Les différentes modélisations de doses, allant de 6 mg à 12 mg une fois par mois, ont permis de sélectionner la dose de 11mg pour les essais de phase III : cette dose permet de maintenir des concentrations de composés triphosphatés supérieures aux doses considérées comme efficaces en prévention tout au long du mois d’exposition. Deux études de PrEP de phase III sont en cours avec cette dose.
Final Results of the ANRS PREVENIR Study With Daily or On-Demand Oral PrEP With TDF/FTC in Paris
Jean-Michel Molina for the ANRS Prevenir Study Group
L’objectif de l’étude observationnelle PREVENIR était d’une part de mettre en évidence une diminution de l’incidence du VIH à Paris entre les périodes 2015/16 (juste avant la PrEP) et 2023/2024 (6 ans après l’implantation de la PrEP). PREVENIR ne concerne que la population HSH et femmes transgenres. Elle a essentiellement recruté des HSH nés en France (>80%). Les participants choisissaient leur mode de PrEP (continue ou discontinue) à l’entrée dans l’étude, mais avait la possibilité de changer, ce qui a été plébiscité par plus de 50% des participants (de façon assez équilibrée entre les deux groupes).
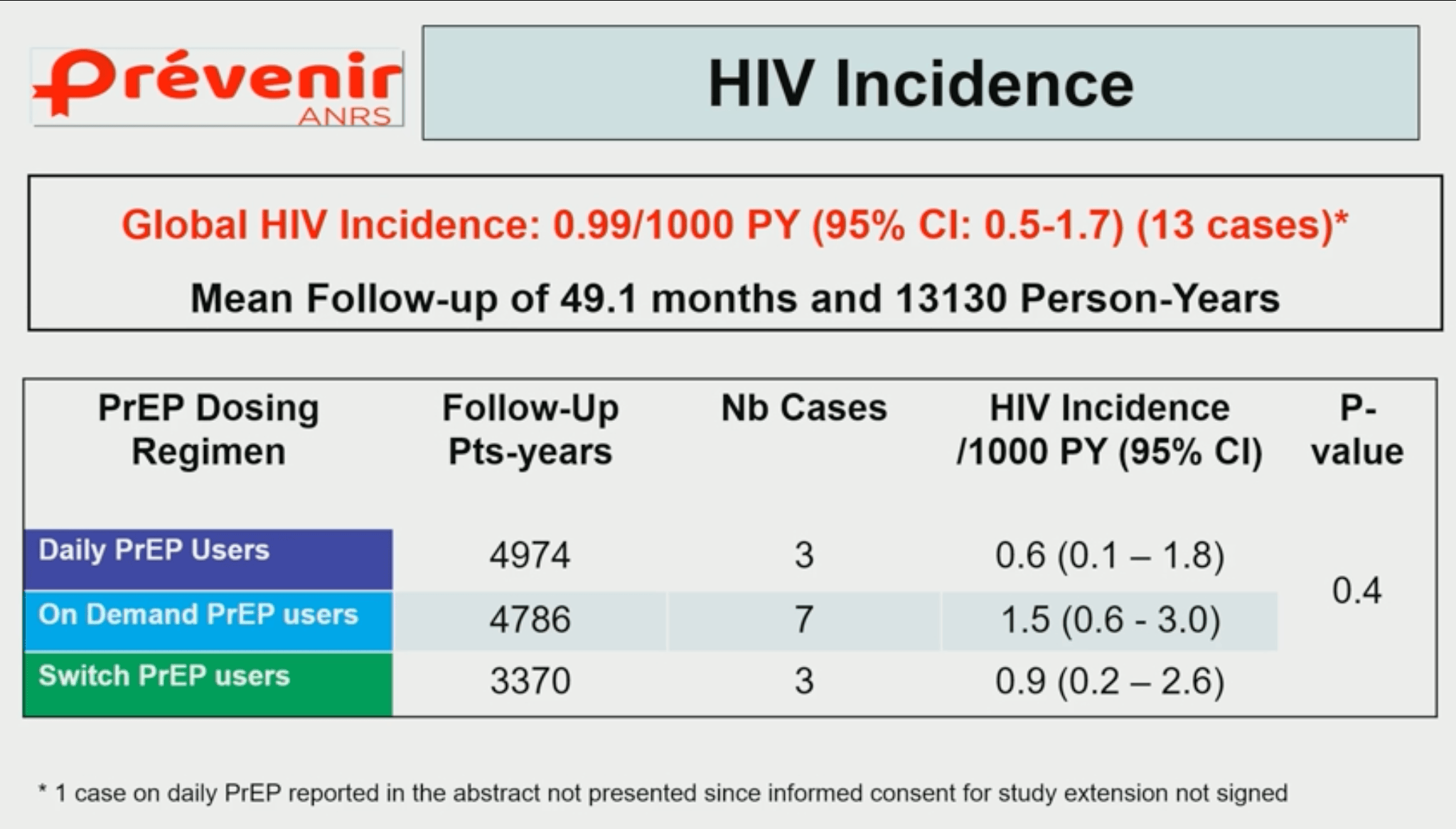
Dans PREVENIR, on retrouve une incidence globale un peu inférieure 1/1000 personnes/années, ce qui est un bon résultat global, mais en parallèle les données de Santé publique France ne montrent pas une réduction d’incidence importante à Paris entre les deux périodes prédéfinies. Cela est lié au fait que l’on observe actuellement une épidémie «biphasique», avec une nette diminution des nouveaux diagnostics chez les HSHHSH Homme ayant des rapports sexuels avec d'autres hommes. nés en France (-33%) et une forte augmentation chez ceux nés à l’étranger (+75%).
La plupart des infections diagnostiquées dans PREVENIR surviennent à distance de l’arrêt de la PrEP. (NDR: Ce qui signifie que l’on se retrouve dans une situation de persistance de l’exposition malgré l’arrêt de PrEP.)
Dernières données sur le lénacapavir en PrEP
Twice-Yearly Subcutaneous Lenacapavir for PrEP: Updated HIV-1. Incidence and Safety Data in PURPOSE 1
Nkosiphile Ndlovu et al.
Lenacapavir for PrEP: HIV-1 Incidence and Safety From PURPOSE 2 at End of Randomized Blinded Phase
Valeria D. Cantos Lucio et al.
Resistance Analyses of the PURPOSE Studies Through the End of the Randomized Blinded Phase
Stephanie Cox et al.
Les trois communications autour du Lénacapavir permettent de disposer des résultats à moyen terme des essais Purpose-1 (2134 participantes, en Afrique subsaharienne) et Purpose-2 (2179 participants, HSH), qui sont toujours en cours. Seules les données intermédiaires avaient été publiées jusqu’à maintenant.
Si l’on regroupe les résultats des deux essais, il y a maintenant cinq échecs de traitement sur la totalité des patients recrutés (près de 4400) dans les deux essais, le niveau d’efficacité reste donc très élevé avec un peu plus de recul.
Dans Purpose-1, l’une des transmissions se fait alors que les conditions de l’étude ont été bien respectées, la patiente ayant bien reçu les injections de lénacapavir dans les temps et l’étude des concentrations montrant que celles-ci sont dans les valeurs attendues pour une protection. Il n’y a donc pas d’explication par défaut d’observance à cet échec. Le second échec dans Purpose-1 concerne une patiente n’ayant pas réalisé son injection de 52 semaines, et s’étant contaminée à distance des premières injections, alors que les concentrations étaient très en dessous des valeurs attendues pour une protection. Ce cas est donc par contre bien expliqué.
Dans Purpose-2, On observe également une nouvelle transmission, diagnostiquée au moment où est réalisée la 2nde injection à S52. Et là aussi, les concentrations attendues sont respectées et le cas n’est donc pas « expliqué » par une mauvaise observanceObservance L’observance thérapeutique correspond au strict respect des prescriptions et des recommandations formulées par le médecin prescripteur tout au long d’un traitement, essentiel dans le cas du traitement anti-vih. (On parle aussi d'adhésion ou d'adhérence.) du rythme des injections. (NDR: Une des questions qui se pose est de savoir si une ISTIST Infections sexuellement transmissibles. peut être un facteur de risque d’échec ; sur les 5 échecs, un patient avait une infection à gono et un autre à Chlamydiae.)
On analyse la résistance virale de ces 5 échecs, 3/5 ont une mutation spécifique du lénacapavir (N74D), Mais tous les virus son porteur d’une mutation M184V et un d’une mutation K65R conférant une résistance à l’ensemble des inhibiteurs nucléosidiques de la transcriptase, soulignant la fréquence de la mutation M184V dans la population virale circulante.
À lire également sur Vih.org: PURPOSE 1 et 2 : données actualisées sur le lénacapavir en PrEP.
Randomized controlled trial of Dynamic Choice to Provide Oral PrEP to Postpartum South African Women
Dvora L. Joseph Davey et al.
Les femmes en post-partum présentent un risque accru d’acquisition du VIH, mais les données d’observance montrent en général une adhésion médiocre pendant cette période. L’idée de cet essai est de comparer, chez des femmes ayant eu une mauvaise observance de la PrEP en pré-partum, trois modalités de délivrance/soutien de la PrEP par TDF/FTC en post-partum: randomisation dans un groupe de choix dynamique (retrait rapide de la PrEP à la clinique, sur des sites communautaires, ou livraison à domicile, avec un suivi du statut VIH négatif par auto-tests VIH) ou dans un groupe contrôle renforcé (counseling PrEP en clinique avec biofeedback basé sur un test urinaire du ténofovir [TFV]).
Dans le bras intervention, 49% des femmes ont choisi le retrait rapide en centre de santé (n=65), 46 % la livraison à domicile (n=62) et 5% le retrait en communauté (n=7); par la suite, 45% (n=61) ont changé de modalité de retrait, principalement de la livraison à domicile vers le centre de santé (76%), et du centre de santé vers la livraison à domicile (35%). À la fin de l’étude, 58% dans le bras intervention avaient retiré la PrEP et rapportaient une utilisation au cours du dernier mois (contre 42 % dans le contrôle ; aOR=1,73 ; IC95% =1,05–2,87) mais il n’y avait pas de différence significative sur l’utilisation objective de la PrEP: 54 % avaient un TFV urinaire positif dans le bras intervention versus 46 % dans le bras contrôle (aOR=1,18 ; IC95% =0,58–2,41).
Effect of Different Pharmacy PrEP Delivery Models on Initiation and Continuation in Kenya: A cluster randomized controlled trial
Katrina F. Ortblad for the Pharm PrEP cRCT Team
Le modèle a été adapté du programme pilote d’une pharmacie de Seattle déjà présenté dans une conférence antérieure, et qui fait l’objet d’un programme dédié dans l’état de Washington. Le tissu de pharmacies au Kenya est assez dense, avec 7400 pharmacies enregistrées. L’idée est ici de comparer quatre façons de proposer la PrEP en pharmacie au Kenya.
En pratique, le modèle qui fonctionne le mieux est celui où il n’y a pas de reste à charge pour le client et qu’une partie des «tâches» PrEP du pharmacien est déléguée à un conseiller spécifiquement formé et payé par le programme. Mais le modèle sans soutien renforcé au pharmacien fonctionne bien également, tant pour la mise sous traitement que pour le suivi.
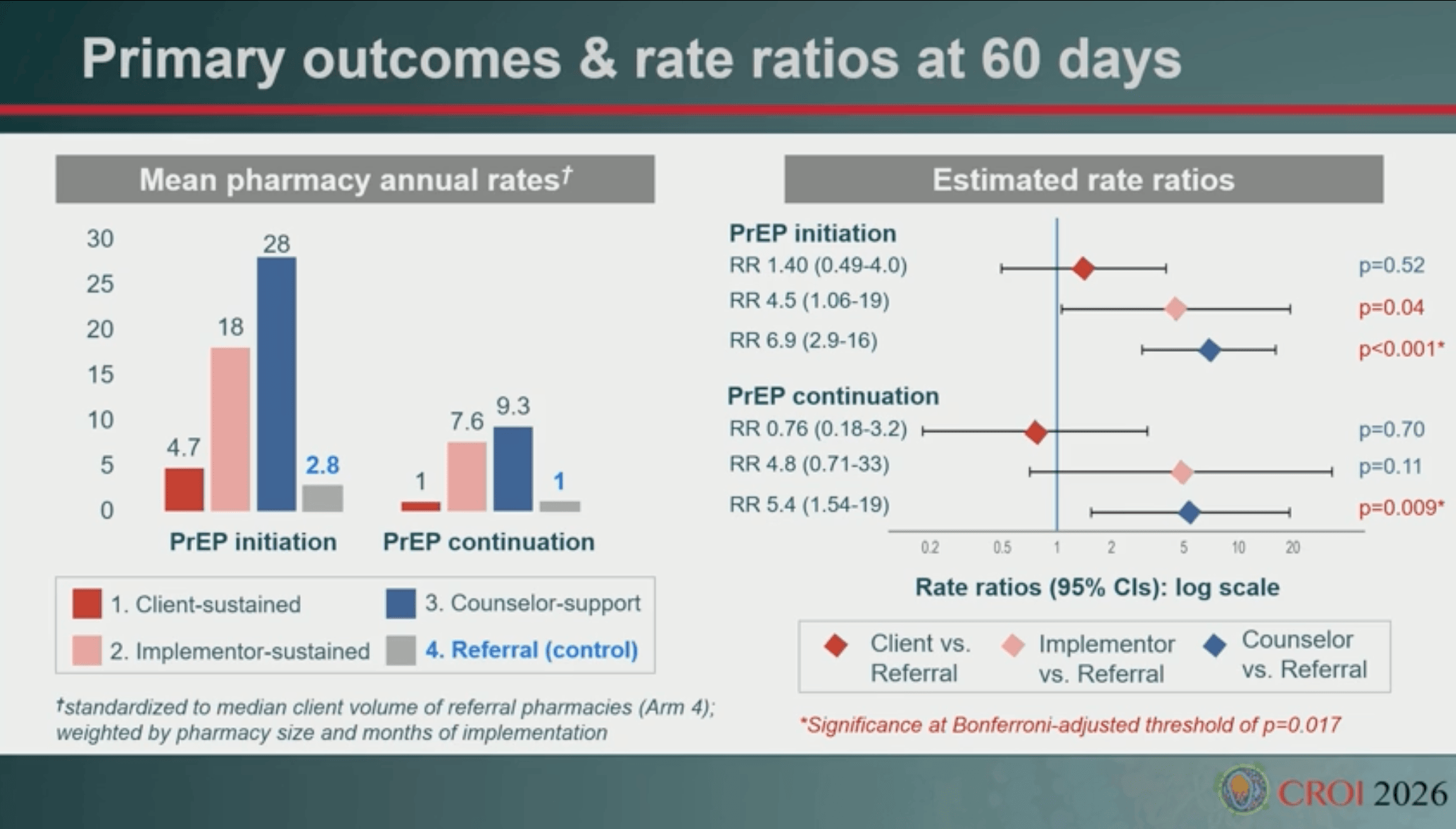
Finalement, les pharmacies qui acceptent de participer au programme arrivent à de bons résultats (sauf en cas de reste à charge pour le client) mais le problème vient surtout du goulot d’étranglement en amont: sur 411 pharmacies sélectionnées initialement, seulement 60 ont pu rejoindre l’étude. Les raisons de non-participation sont multiples, mais surtout liées à l’absence d’intérêt du pharmacien pour l’étude ou l’absence de pharmacien tout court. L’absence de pièce de confidentialité n’est une cause de non-participation que dans 29 cas.
Référence
Session de communication orales libres: «Evolution du paysage de la PrEP du VIH, piliers et avancées», CROICROI «Conference on Retroviruses and Opportunistic Infections», la Conférence sur les rétrovirus et les infections opportunistes annuelle où sont présentés les dernières et plus importantes décision scientifiques dans le champs de la recherche sur le VIH. 2026.
Cet article a été publié sur le site du CoReSS Bretagne, nous le reproduisons ici avec l’aimable autorisation de son auteur.
