RIO est une étude randomisée en double aveugleDouble aveugle L'étude avec répartition aléatoire, randomisé ou en double insu (ou en double aveugle) est une démarche expérimentale utilisée en recherche médicale et pharmaceutique faisant que ni le patient ni le médecin ne sait quel traitement est pris : traitement A ou B, traitement A ou placébo. contre placeboPlacebo Substance inerte, sans activité pharmacologique, ayant la même apparence que le produit auquel on souhaite le comparer. (NDR rien à voir avec le groupe de rock alternatif formé en 1994 à Londres par Brian Molko et Stefan Olsdal.) menée auprès de 68 patients (34 par groupe). Son objectif était d’évaluer l’efficacité de deux anticorps neutralisants à large spectre (LS-bNAbs), 3BNC117-LS et 10-1074-LS, administrés en deux perfusions intraveineuses espacées d’au moins 20 semaines, pour contrôler la charge viraleCharge virale La charge virale plasmatique est le nombre de particules virales contenues dans un échantillon de sang ou autre contenant (salive, LCR, sperme..). Pour le VIH, la charge virale est utilisée comme marqueur afin de suivre la progression de la maladie et mesurer l’efficacité des traitements. Le niveau de charge virale, mais plus encore le taux de CD4, participent à la décision de traitement par les antirétroviraux. après l’arrêt programmé du traitement antirétroviral.
Les patients inclus dans l’étude devaient répondre à plusieurs critères :
- Un traitement débuté lors de la primo-infection ou un taux de CD4 > 500/mm³;
- Un contrôle virologique stable d’au moins un an;
- Un taux de CD4 > 500/mm³ ou un rapport CD4/CD8 >1;
- Des mesures de prévention mises en place pour éviter la transmission du virus.
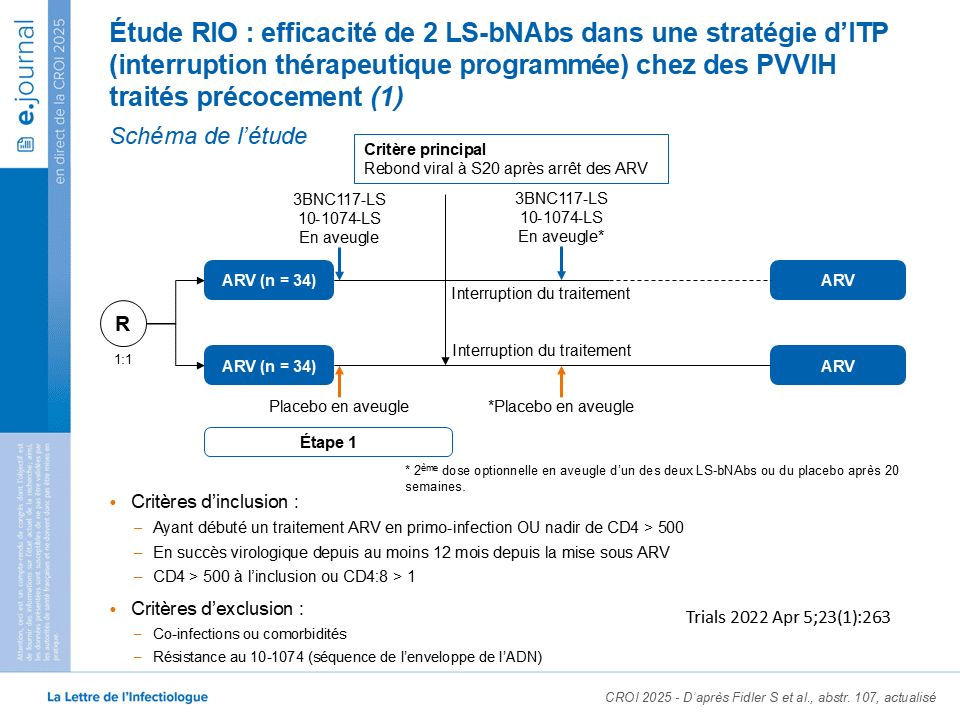
Le rebond viral était défini par six charges virales consécutives supérieures à 1000 copies/ml ou deux charges virales supérieures à 100000 copies/ml.
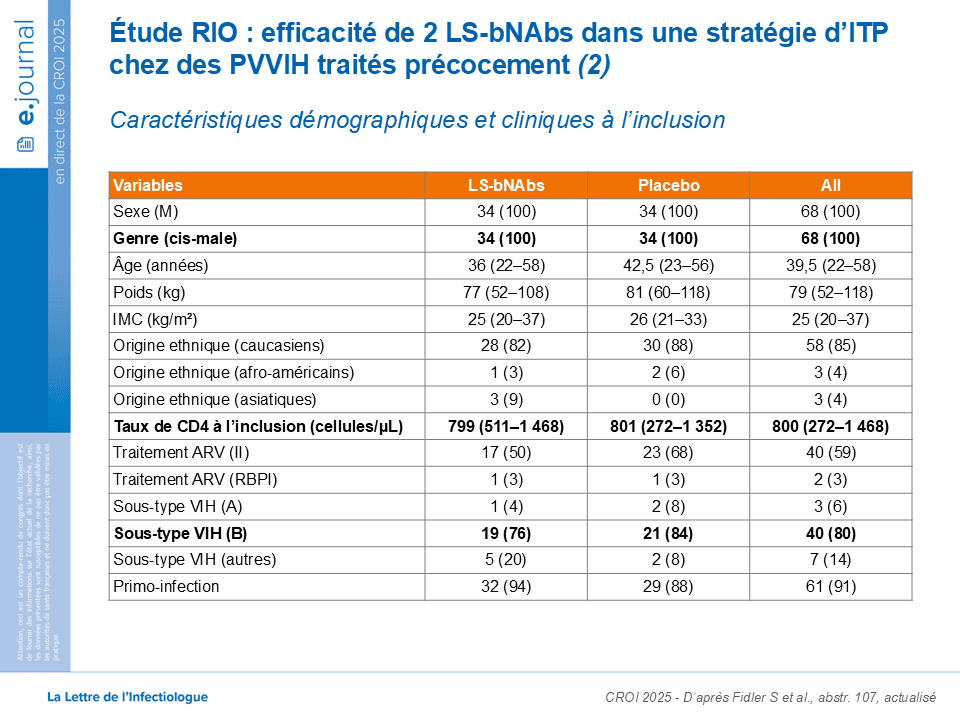
Des résultats encourageants
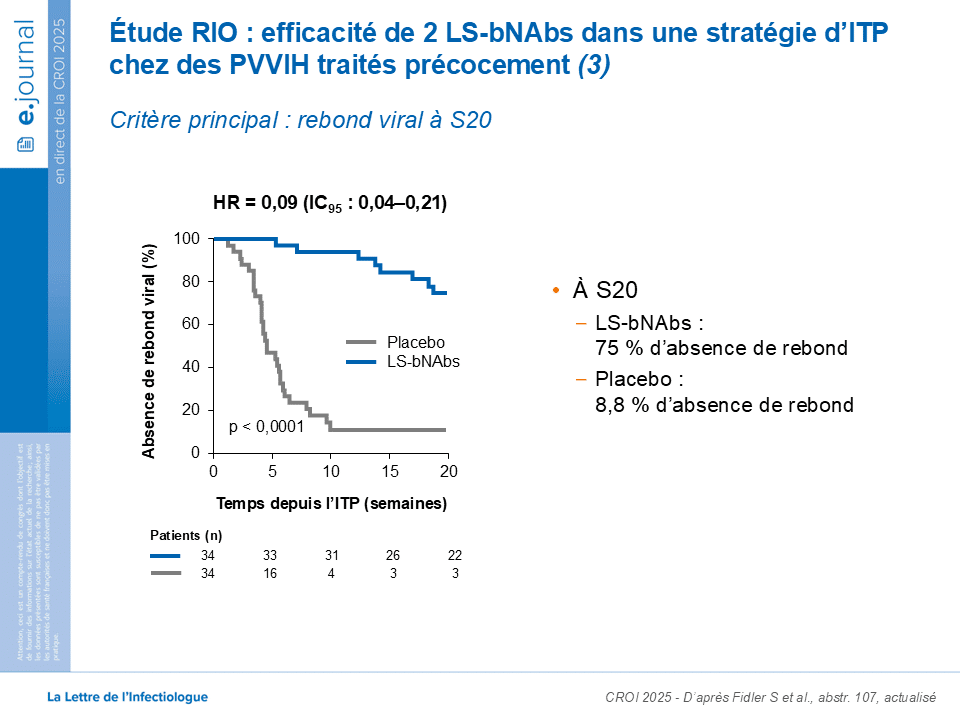
À la 20ᵉ semaine (objectif primaire), les chercheurs ont observé une différence significative entre les patients traités avec les anticorps et ceux sous placebo: 75 % des patients sous 3BNC117-LS et 10-1074-LS n’ont pas présenté de rebond virologique, contre seulement 8,8 % dans le groupe placebo (HR: 0,09; 95% IC: 0,04; 0,21, p<0.0001).
Après la 20ᵉ semaine, la durée médiane de contrôle virologique sous LS-bNAbs était de 62,3 semaines et 57% des patients étaient toujours en contrôle virologique à la 48ᵉ semaine et 39% à la 72ᵉ semaine.
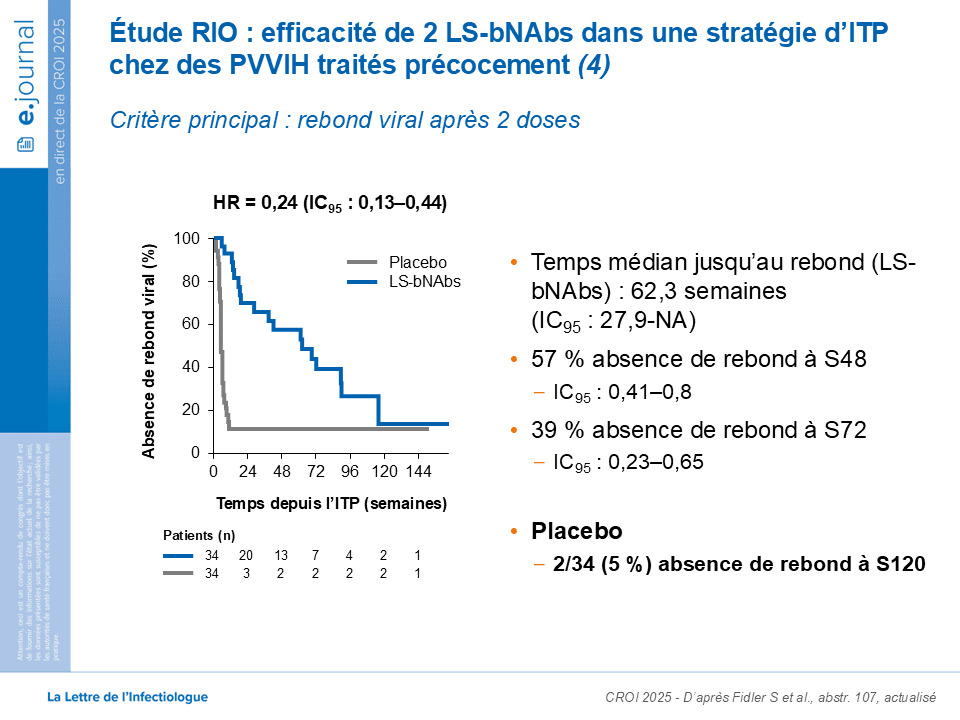
Trois profils de réponse virologique ont émergé:
- Un profil de rebond virologique rapide (8 patients sur 34) avant la 20ᵉ semaine, avec pour la moitié d’entre eux une sélection de résistance au 10-1074-LS.
- Un profil de rebond virologique retardé (14 patients sur 29) après la 72ᵉ semaine.
- Un profil de contrôle virologique (7 patients sur 29) au-delà de 72 semaines.
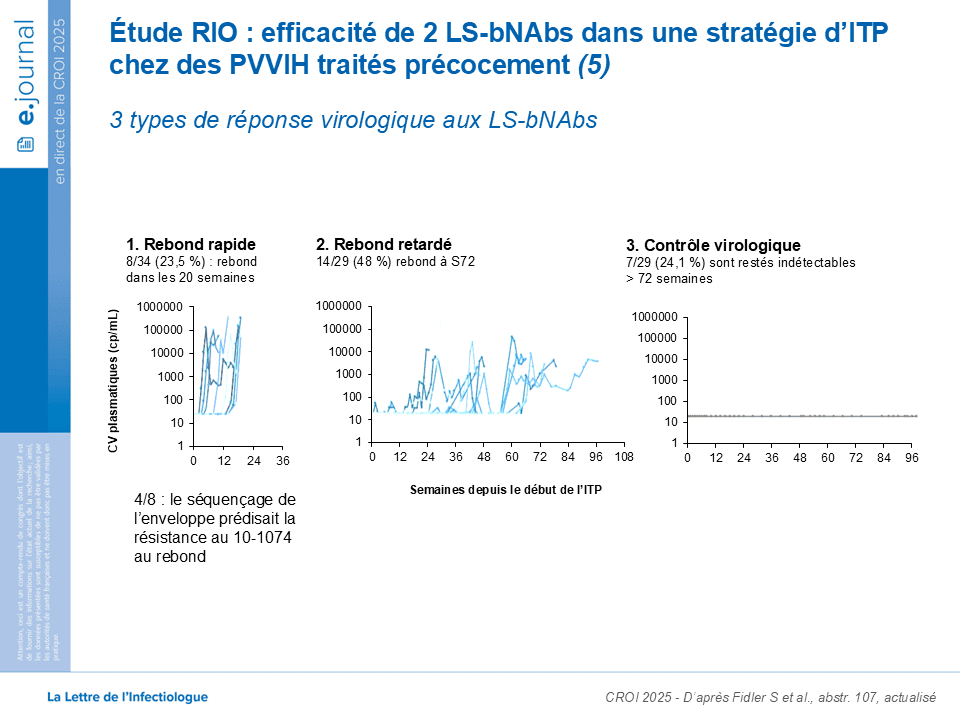
Par ailleurs, cinq patients ont présenté un rebond virologique dépassant 1000000 copies/ml.
Une tolérance satisfaisante et des effets immunologiques
Les niveaux des deux LS-bNAbs sont restés supérieurs à 10 µg/ml pendant plus de six mois après la dernière perfusion. Leur demi-vie a été estimée à 72,5 jours pour le 10-1074-LS et 64,8 jours pour le 3BNC117-LS. Aucun événement indésirable grave lié aux anticorps ou à l’interruption du traitement n’a été rapporté. Tous les patients ayant présenté un rebond virologique ont retrouvé un contrôle viral après la reprise du traitement antirétroviral.

L’analyse du réservoir viral a montré une diminution de la taille du réservoir de VIHVIH Virus de l’immunodéficience humaine. En anglais : HIV (Human Immunodeficiency Virus). Isolé en 1983 à l’institut pasteur de paris; découverte récemment (2008) récompensée par le prix Nobel de médecine décerné à Luc montagnier et à Françoise Barré-Sinoussi. avec une réduction de l’ADN viral intact. De plus, une amélioration des réponses des lymphocytes T spécifiques du VIH (protéine Gag) a été observée, suggérant un possible effet immunologique des anticorps après leur administration.
Ces résultats montrent qu’un tiers des patients ayant reçu ces anticorps a pu maintenir un contrôle virologique pendant 72 semaines sans traitement antirétroviral. L’amélioration des réponses immunitaires observée suggère que ces anticorps pourraient avoir un effet durable sur le système immunitaire, ouvrant ainsi la voie à de nouvelles approches thérapeutiques pour le contrôle du VIH à long terme.
D’après Fidler S et al., abstr. 107, actualisé
Une version de cet article et cette présentation ont été précédemment publiés dans le e-journal de la Lettre de l’infectiologue à l’occasion de la CROICROI «Conference on Retroviruses and Opportunistic Infections», la Conférence sur les rétrovirus et les infections opportunistes annuelle où sont présentés les dernières et plus importantes décision scientifiques dans le champs de la recherche sur le VIH. 2025.
