Avec le cabotégravir, la PrEP injectable est disponible aux États-Unis depuis décembre dernier. Le CDC (Center for Disease Control and Prevention) la recommande «pour tous les adultes sexuellement actifs qui déclarent avoir des comportements sexuels les exposant à “un risque continu substantiel d’exposition et d’acquisition du VIH”».
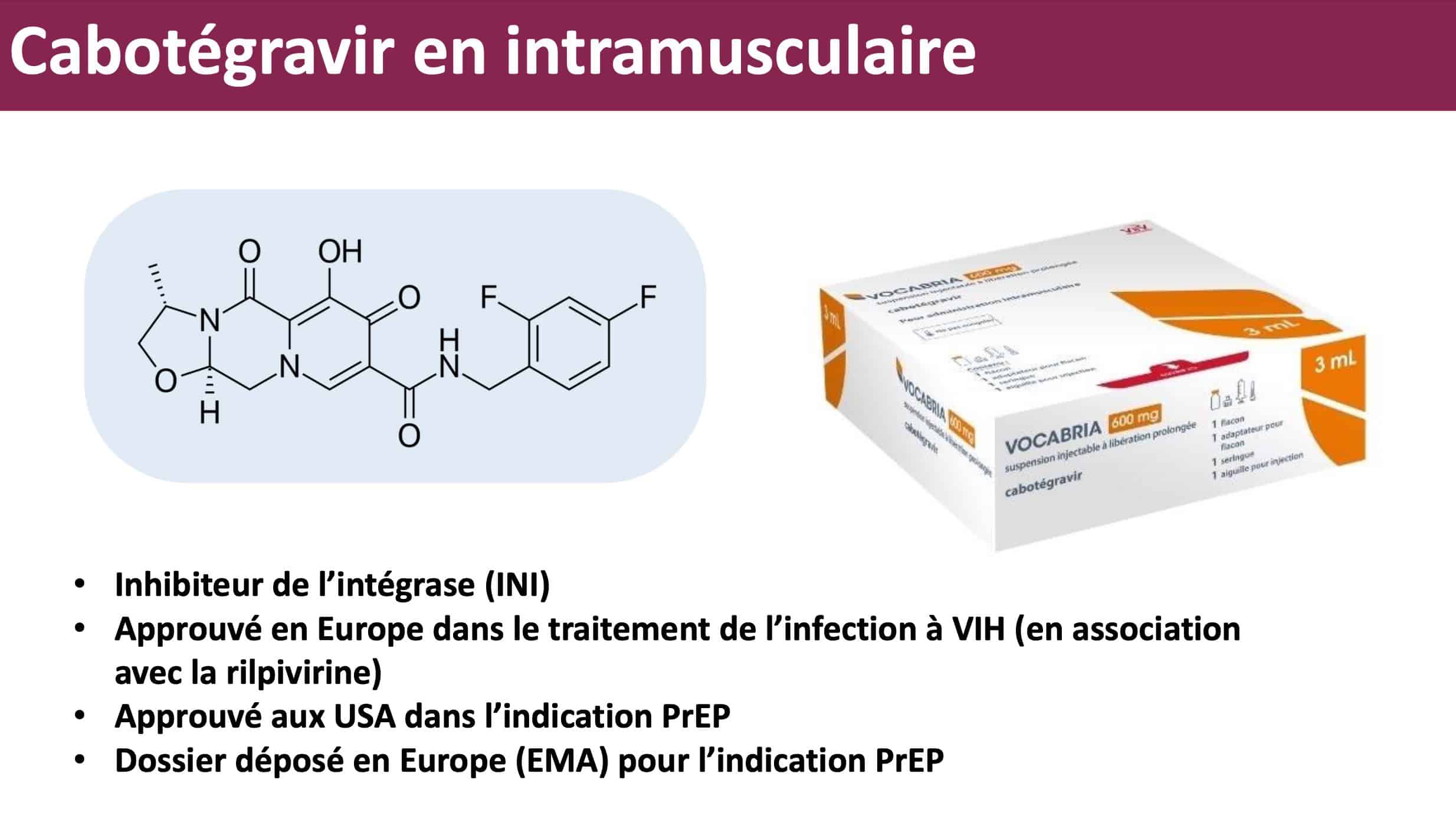
Son efficacité avait été démontrée grâce aux études HPTN 083 et HPTN 084, qui ont mené à son autorisation par la Food and Drug Administration (FDA) aux Etats-Unis. La PrEPPrEP Prophylaxie Pré-Exposition. La PrEP est une stratégie qui permet à une personne séronégative exposée au VIH d'éliminer le risque d'infection, en prenant, de manière continue ou «à la demande», un traitement anti-rétroviral à base de Truvada®. orale quotidienne “classique” a eu d’excellents résultats chez les HSHHSH Homme ayant des rapports sexuels avec d'autres hommes. mais des études ont montré qu’elle était moins efficace dans les conditions de la vie réelle chez les femmes cis, en grande partie en raison de la difficulté à maintenir une adhérence optimale. La PrEP sous forme injectable permet de contourner ce problème et dans cette population, la molécule à action prolongée s’est avérée à 89% plus efficace que la PrEP quotidienne sous forme de cachets oraux.
En France comme en Europe, aucune date de commercialisation ou d’autorisation n’ont été pour le moment avancées, même s’il semble probable qu’elle soit disponible sur le continent d’ici la fin de l’année. Il y a d’autres molécules qui sont en train d’être étudiées, comme le lénacapavir (essais PURPOSE 1 et 2, avec une injection sous cutanée tous les 6 mois) et l’islatravir, dont plusieurs essais ont été arrêtés à cause d’une probable toxicité lymphocytaire de la molécule.

Une grande efficacité, mais des cas d’infections à surveiller
On l’a vu, les études montrent que la PrEP injectable est efficace et même dans des populations qui sont parfois absente des programmes de PrEP classique : Dans les 5000 personnes participants à l’essai HPTN-083, il y avait 50% de moins de 30 ans, plus de 10% de femmes trans et plus de 50% de personnes afro-américaine. Cet essai a d’ailleurs arrêté prématurément du fait du grand nombre d’infections dans le bras “PrEP orale” lors d’une analyse intermédiaire en mai 2020, et a ainsi montré la supériorité de la PrEP injectable.
Comment expliquer le niveau d’infections dans les deux bras? Dans le bras PrEP orale, les données ont montré que près de 20% des personnes qui étaient supposées prendre la PrEP ne l’a prenaient pas ou étaient sous-exposées au médicament.
Dans le groupe cabotegravir, les chercheurs ont identifié plusieurs type d’infections :
- Les personnes diagnostiquées au moment de leur entrée dans l’étude. Certaines avaient déjà commencé le cabotégravir mais ces infections sont antérieures à l’inclusion dans l’étude.
- Les infections survenant chez les personnes ne respectant pas le protocole et la fréquence des injections de l’étude.
- Les infections qui surviennent chez des participants recevant le cabotégravir injectable et observants du protocole. Aujourd’hui, les chercheurs ne sont pas en mesure de donner une explication claire pour ces cas, rares, mais néanmoins graves, d’infection en présence de cabotégravir injectable.
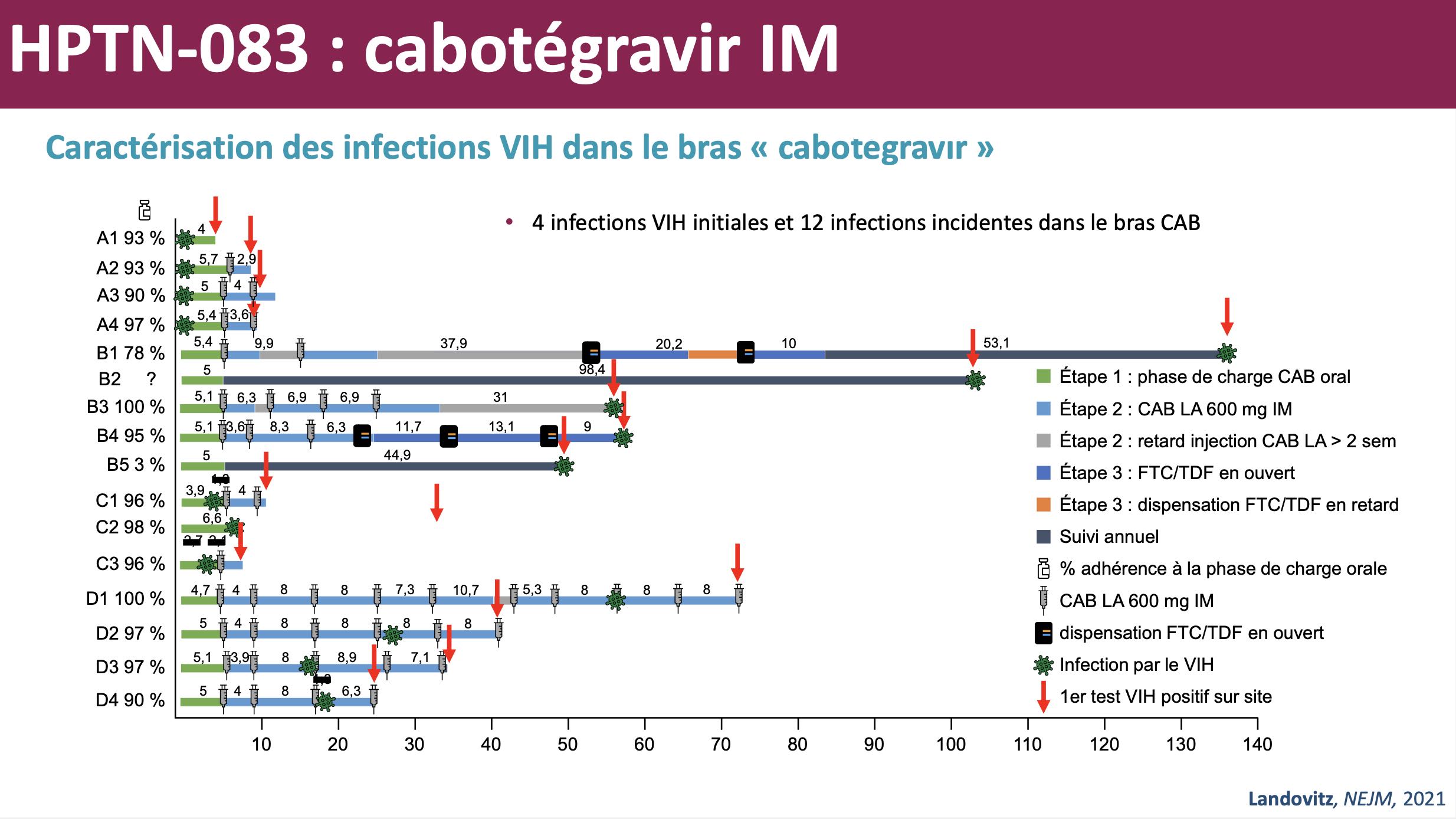
C’est bien sûr cette catégorie qu’il faudra étudier pour mieux connaître les limites de la PrEP injectable. Dans ces cas de figure, les participants sont infectés alors qu’ils ne sont pas sous-exposés en cabotégravir (les dosages réguliers montrent une concentration régulière dans le sang).
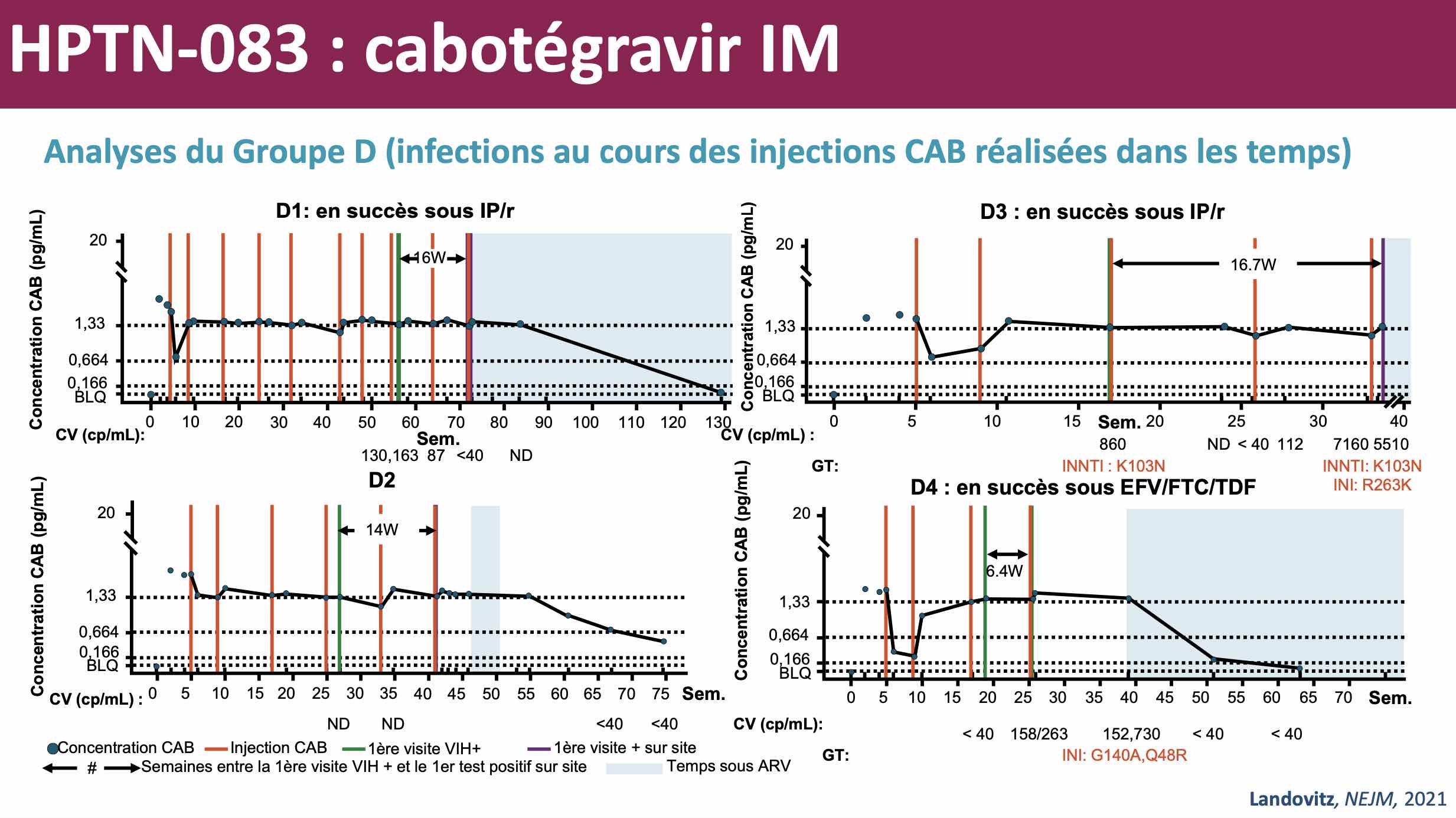
Retard de diagnostic et risque de résistance
Autre problème, la présence de la PrEP a d’ailleurs délayé leur diagnostic de plusieurs semaines, voire de plusieurs mois. C’est là l’une des faiblesses de la formule injectable, dont la présence dans le corps impacte les marqueurs de diagnostic, en provoquant une séroconversionSéroconversion Période d'apparition, dans le sang, d'anticorps spécifiques en réponse au virus. tardive et une charge viraleCharge virale La charge virale plasmatique est le nombre de particules virales contenues dans un échantillon de sang ou autre contenant (salive, LCR, sperme..). Pour le VIH, la charge virale est utilisée comme marqueur afin de suivre la progression de la maladie et mesurer l’efficacité des traitements. Le niveau de charge virale, mais plus encore le taux de CD4, participent à la décision de traitement par les antirétroviraux. faible (voire indétectable). Les autorités américaines préconisent d’ailleurs pour le dépistage des personnes sous PrEP injectable, de recherche l’ARN-VIH, tous les deux mois.
D’autre part, les gens qui vont connaître une séroconversion sous monothérapie s’exposent à l’apparition rapide de souches résistantes au traitement, puisque l’infection n’est pas contrôlée par une multithérapie.

Source : Romain Palich, Journées Thématiques SFLS 2022.
Sur les 12 infections ayant eu lieu sous le bras cabotégravir, 7 ont montré des mutations de résistance:
- 5 avec des mutations de résistance aux INIINI Les inhibiteurs de l’intégrase, ou anti-intégrases sont l'une des dernières classes d’antirétroviraux. Ils agissent en empêchant le VIH d’intégrer son message génétique dans celui de la cellule cible. Ces médicaments ont un profil de résistances différent des autres molécules, ce qui les rend intéressants en cas de multi-résistances face aux autres traitements. (Q148R ou R263K) dont un avec 1 mutation de résistance en plus aux INNTINNRTI Les inhibiteurs non nucléosidiques de la transcriptase inverse (INNTI en Français ou «non-nucleoside reverse transcriptase inhibitors», NNRTI, en anglais) ont un effet inhibiteur direct sur la transcriptase inverse (TI) du VIH-1 en formant une liaison réversible et non compétitive avec l'enzyme. La nevirapine, la delavirdine et l'efavirenz sont des NNRTI.
- 1 avec des mutations de résistance aux INNTI seulement
- 1 avec des mutations de résistance aux INTIINTI Les inhibiteurs nucléosidiques de la transcriptase inverse du VIH ou INTI, sont des composés de synthèse utilisés dans le traitement du VIH et des hépatites. et aux INNTI
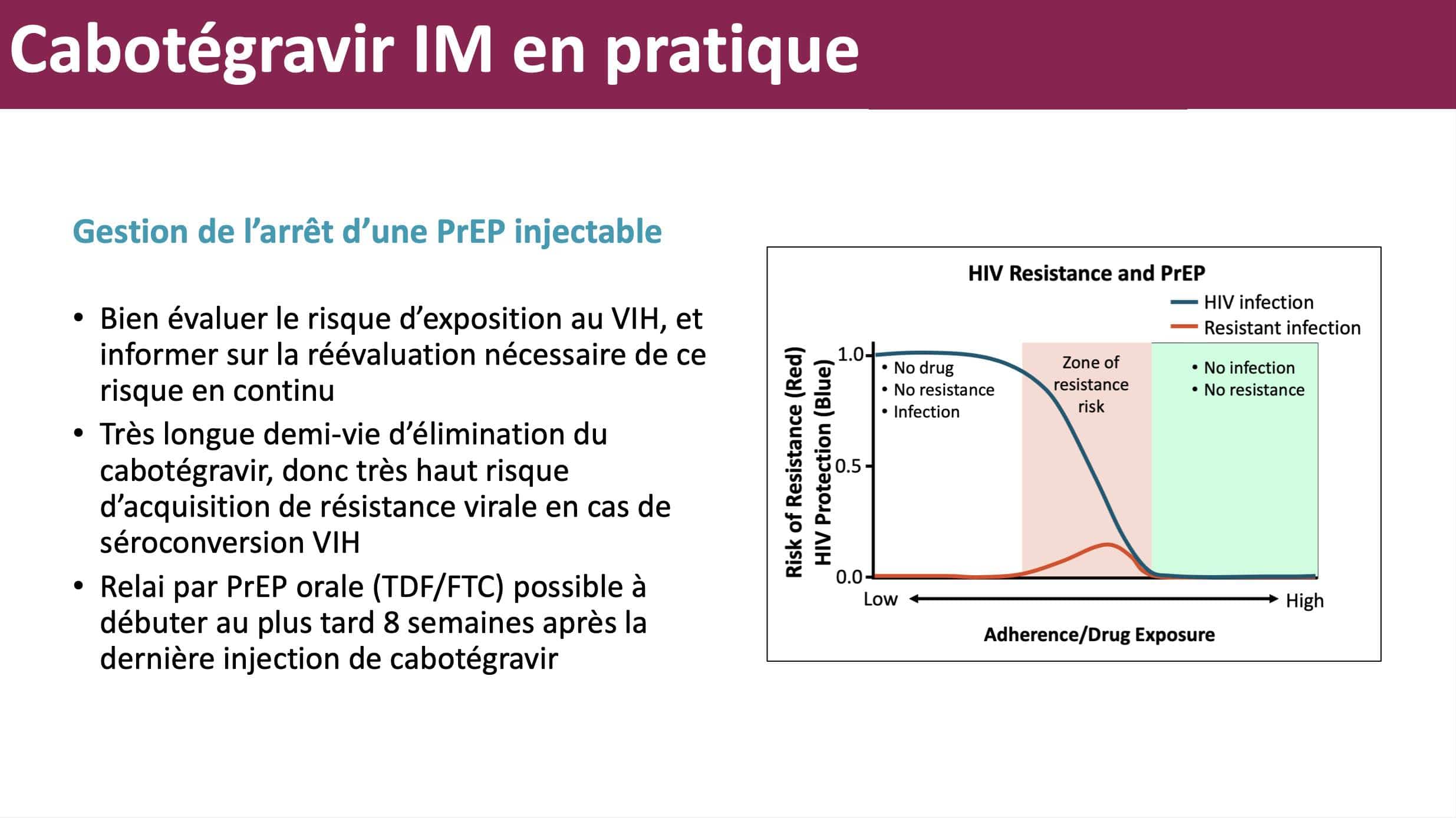
La gestion de l’arrêt
Ce risque de résistance est aussi présent lors de l’arrêt de la PrEP injectable. Le cabotégravir injectable est efficace au bout de 2 mois, mais reste dans le sang pendant 6 mois. La molécule a en effet une très longue demi-vie d’élimination, et donc il existe un très haut risque d’acquisition de résistance virale en cas de séroconversion VIH dans les 6 mois qui suivent la dernière injection, pendant que le patient se trouve dans un situation de monothérapie avec un faible dosage plasmatique. Il est donc nécessaire de proposer un relai préventif sous forme de PrEP par voie orale durant cette période.