D’après Matthews RP et al. Abstract 88LB actualisé.
L’islatravir (MK-8591) est un inhibiteur de la translocation de la transcriptase inverse des nucléosides, très puissant et à longue demi-vie, actuellement en développement pour la PrEPPrEP Prophylaxie Pré-Exposition. La PrEP est une stratégie qui permet à une personne séronégative exposée au VIH d'éliminer le risque d'infection, en prenant, de manière continue ou «à la demande», un traitement anti-rétroviral à base de Truvada®. sous forme de comprimé oral mensuel. Par ailleurs, des prototypes d’implants d’islatravir (contenant uniquement un polymère et de l’islatravir) ont démontré le potentiel d’une administration annuelle pour la PrEP. Des implants radio-opaques à élution d’islatravir de nouvelle génération ont fait l’objet d’études précliniques pour établir la tolérance générale et évaluer la pharmacocinétique (PK) de l’islatravir parent et de l’islatravir-TP (triphosphate) actif. Ces données, ainsi que celles d’une étude de provocation par le SIV et d’essais de phase 1 antérieurs, ont servi de base pour établir une concentration seuil d’islatravir-TP de 0,05 pmol/million de cellules dans les PBMC.
Dans cet essai multicentrique de phase 1 en double aveugleDouble aveugle L'étude avec répartition aléatoire, randomisé ou en double insu (ou en double aveugle) est une démarche expérimentale utilisée en recherche médicale et pharmaceutique faisant que ni le patient ni le médecin ne sait quel traitement est pris : traitement A ou B, traitement A ou placébo. contrôlé par placeboPlacebo Substance inerte, sans activité pharmacologique, ayant la même apparence que le produit auquel on souhaite le comparer. (NDR rien à voir avec le groupe de rock alternatif formé en 1994 à Londres par Brian Molko et Stefan Olsdal.) un seul implant à élution d’islatravir (48 mg, 52 mg ou 56 mg) ou placebo a été placé chez des participants à faible risque d’infection par le VIHVIH Virus de l’immunodéficience humaine. En anglais : HIV (Human Immunodeficiency Virus). Isolé en 1983 à l’institut pasteur de paris; découverte récemment (2008) récompensée par le prix Nobel de médecine décerné à Luc montagnier et à Françoise Barré-Sinoussi. pendant 12 semaines. La sécurité et la tolérance, ainsi que la pharmacocinétique du parent islatravir et de l’islatravir-TP du plasma et des PBMC, ont été recueillies tout au long du placement et pendant 8 semaines après le retrait. Les résultats montrent que ces implants ont été généralement bien tolérés et il n’y a pas eu de différence nette en fonction de la dose dans les effets indésirables liés aux implants. Les taux d’islatravir-TP actif étaient supérieurs à la cible pour les implants tout au long de leur mise en place avec les deux dosages les plus élevés (figure ci-dessous).
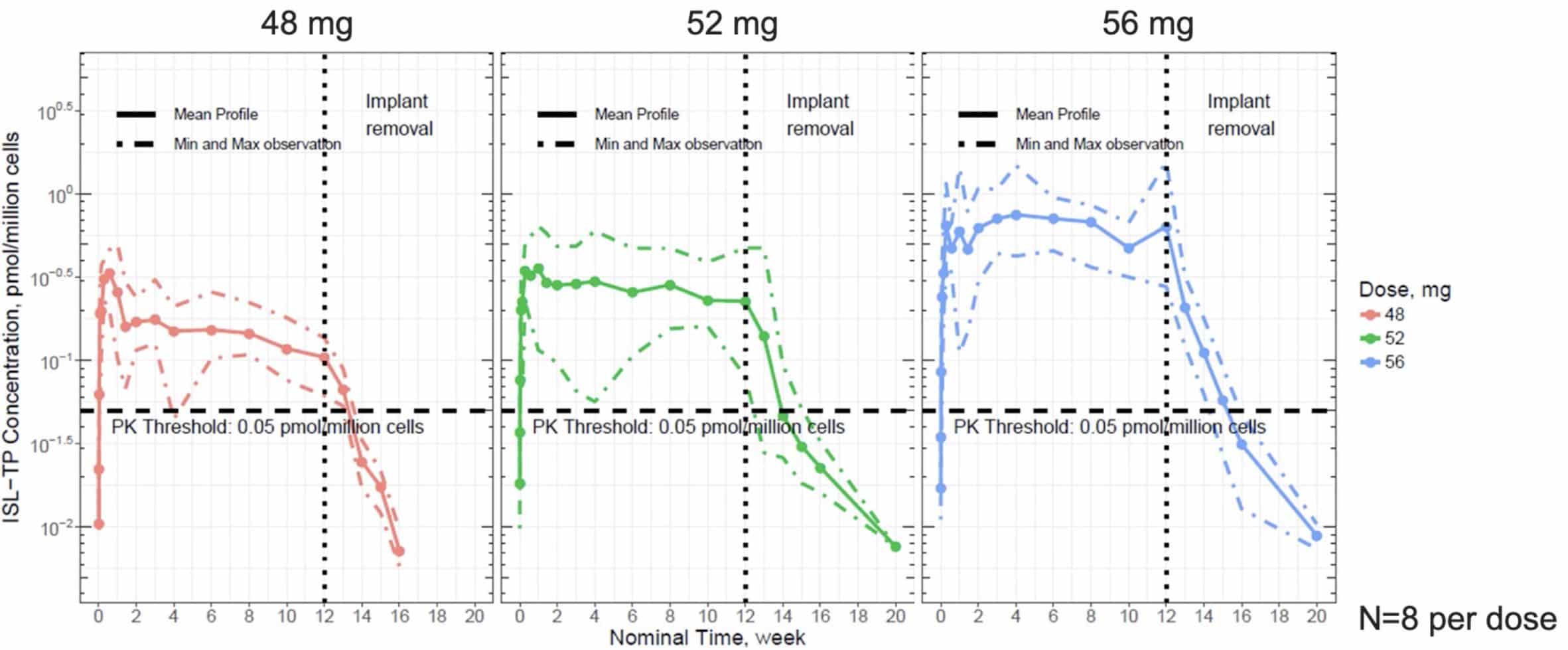
tout au long du placement de l’implant pour les deux dosages les plus élevés.
Source : Matthews RP, CROICROI «Conference on Retroviruses and Opportunistic Infections», la Conférence sur les rétrovirus et les infections opportunistes annuelle où sont présentés les dernières et plus importantes décision scientifiques dans le champs de la recherche sur le VIH. 2021.
Les données de cet essai et des évaluations in vitro des implants ISL suggèrent que des implants contenant une dose 52mg permettraient d’atteindre des concentrations moyennes ISL-TP supérieures au seuil PK à 52 semaines.
En conclusion, ces implants de nouvelle génération à élution d’islatravir permettent une libération de médicament qui devrait être suffisante pour la prophylaxie du VIH pendant au moins un an. Ils semblent être bien tolérés, et les résultats de cet essai permettront de poursuivre l’étude de ces implants dans le cadre d’un essai de phase 2. A quand une « vaccination » annuelle pour la PrEP… Tout en sachant qu’il faudra assurer l’observance annuelle pour un changement à 1 an et entre temps, l’offre global de santé sexuelle (vaccinations, dépistage et traitement des ISTIST Infections sexuellement transmissibles. prise en charge des addictions…) qui, à notre connaissance, ne sont pas inclus dans le dispositif préventif sous cutané.
Cet article a été publié initialement dans le e-journal de « La Lettre de l’infectiologue » couvrant la conférence, nous le reproduisons ici avec leur aimable autorisation.
