À l’heure où s’écrivent ses lignes, il n’y a guère que le président et ex-candidat Biden pour remettre le CovidCovid-19 Une maladie à coronavirus, parfois désignée covid (d'après l'acronyme anglais de coronavirus disease) est une maladie causée par un coronavirus (CoV). L'expression peut faire référence aux maladies suivantes : le syndrome respiratoire aigu sévère (SRAS) causé par le virus SARS-CoV, le syndrome respiratoire du Moyen-Orient (MERS) causé par le virus MERS-CoV, la maladie à coronavirus 2019 (Covid-19) causée par le virus SARS-CoV-2. dans l’actualité tourmentée de l’été. Pourtant, si on s’en réfère au bulletin de Santé publique France de la semaine 28 (du 8 au 14 juillet 2024), une circulation virale persiste bien en ce début d’été, avec, par exemple en médecine de ville, 3% du nombre d’actes pour suspicion de Covid-19Covid-19 Une maladie à coronavirus, parfois désignée covid (d'après l'acronyme anglais de coronavirus disease) est une maladie causée par un coronavirus (CoV). L'expression peut faire référence aux maladies suivantes : le syndrome respiratoire aigu sévère (SRAS) causé par le virus SARS-CoV, le syndrome respiratoire du Moyen-Orient (MERS) causé par le virus MERS-CoV, la maladie à coronavirus 2019 (Covid-19) causée par le virus SARS-CoV-2. chiffre stable par rapport à la semaine précédente. Cette dynamique peut rappeler l’été 2023, mais elle est bien inférieure à celle de l’été 2022 où ces passages représentaient près de 12% des actes de SOS Médecins. Le Covid est la cause de quelque 1,2% de l’ensemble des hospitalisations. Mais sur le terrain, notamment parmi le personnel hospitalier, très peu de gens se font dépister, et on observe çà et là des clusters au sein des équipes soignantes.
Le Covid représentait, durant la semaine 28, 0,6% des passages en réanimation. Le taux de positivité dans les laboratoires de biologie médicale du réseau Relab en ville et du réseau Renal à l’hôpital, était respectivement de 25,4% et de 11,5%. La surveillance des eaux usées est toujours aussi minime avec 12 stations de traitement des eaux usées rapportées par Santé publique France. Cette détection semble amorcer, pour représentative qu’elle soit, une décroissance à la semaine 28.
Pas de variant préoccupant
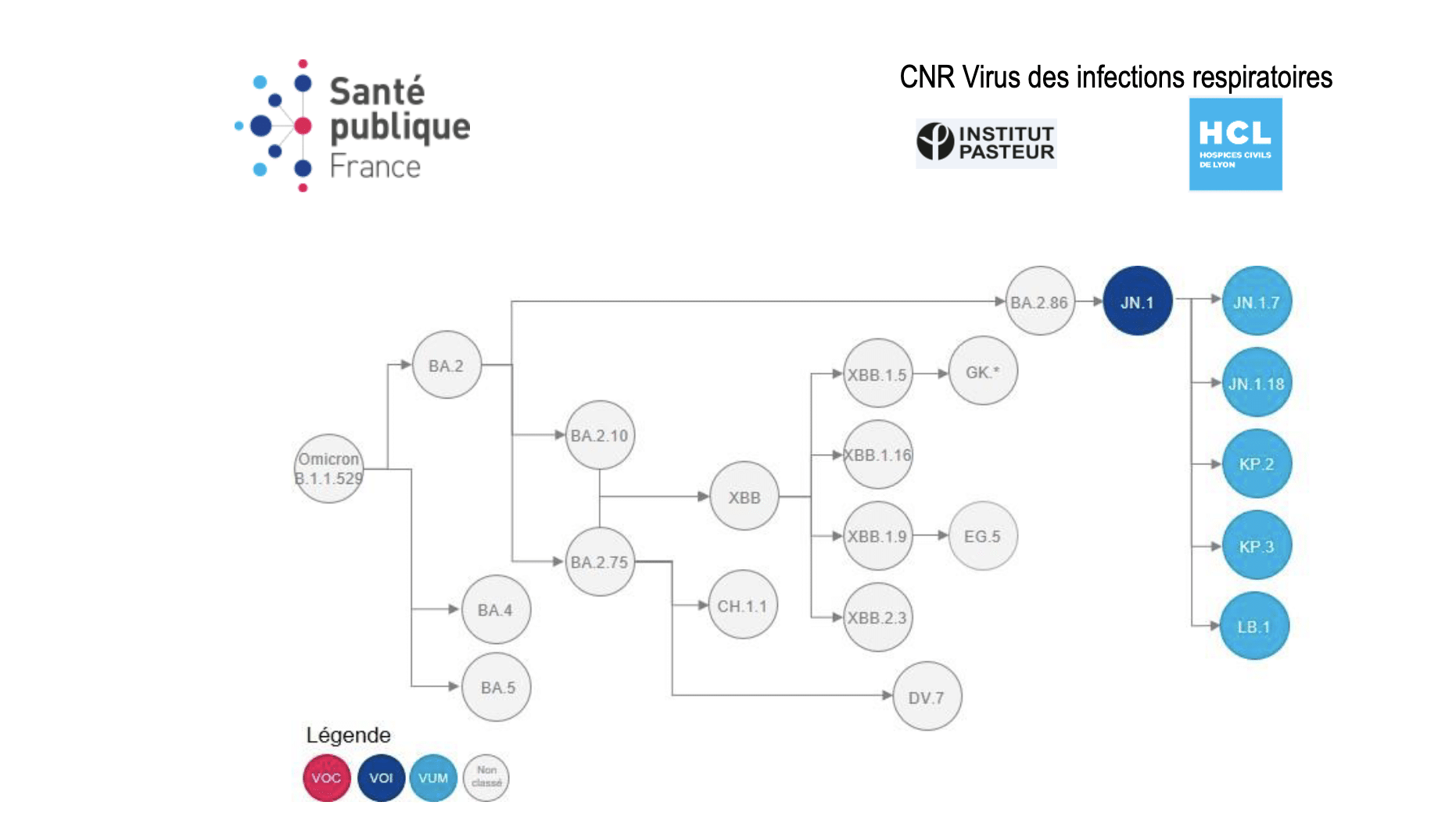
Plus important encore, sont les analyses de risques des variants en date du 8 juillet 2024 issues de la surveillance génomique. On y voit l’évolution assez préoccupante de la multiplicité des variants dérivés d’Omicron (cf. tableau 1 et Figure 1). Les variants EG5 (« Eris » de l’été 2003) ainsi que la famille des XBB recombinants précédemment classés variant à suivre (VOI) – dont XBB 1.5 (le fameux « Kraken ») – ont été déclassés, n’étant plus détectés depuis mars 2024.
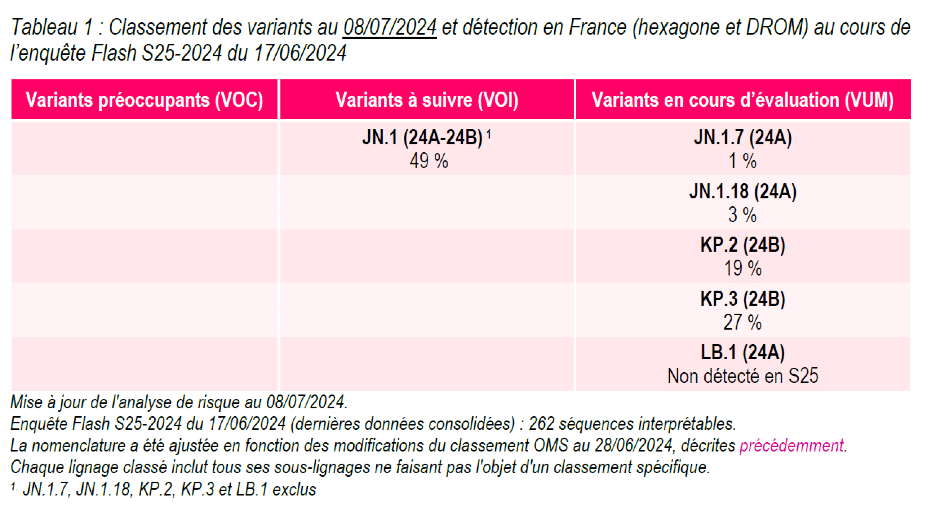
Le sous variant JN.1 est prédominant dans le monde (49% en France au 8 juillet). Ce sous-lignage de BA.2.86 (cf. Figure 1) est le lignage le plus détecté dans l’échelle mondiale avec plus de 80 % des séquences disposées sur GISAID, la base mondiale de séquences, depuis février 2024. Le sous-lignage KP.2 issu de JN.1.11 – qui a fait couler beaucoup d’encre notamment par l’appellation FLIRT trouvée par un petit malin – semble se stabiliser autour de 20% mais plusieurs études en preprint démontrent in vitro une résistance accrue aux anticorps neutralisants induits par les vaccins ciblants XBB.1.5, précisément le vaccin utilisé dans la dernière campagne vaccinale d’octobre 2023 et du printemps 2024. Cela reste à confirmer. D’autres sous-lignages de JN.1 sont apparus, tels KP.3 et LB.1 qui sont en très nette progression, avec 27% de KP.3 en France au dernier comptage de SPF. Et toujours aucun variant préoccupant (VOC) à signaler.
À chaque fois, le taux de transmission effectif serait supérieur au précédent variant avec un échappement immunitaire accru de ces sous-lignages par rapport à JN.1. Il est clair que les mutations observées telles que R346T, F456L, T572I influencent péjorativement l’évasion immunitaire, l’affinité pour les récepteurs ACE2 et l’infectiosité. Phénomène observé depuis le printemps 2024. Toutes les instances – le comité consultatif sur les vaccins de la FDA aux États-Unis, celui de l’OMS, de l’Agence européenne des médicaments (EMA) – ont demandé aux entreprises de cibler leur prochaine production vaccinale précisément sur ces variants et sous variants de JN.1 et al. pour la campagne 2024-2025. Spécialistes et agences attendent avec inquiétude l’impact des Jeux olympiques de Paris sur les circulations virales de ces variants d’échappement.
La situation particulière des immunodéprimé·es
C’est l’occasion aussi de faire le point sur ceux qui payent le plus lourd tribut à ces variants d’échappement : les immunodéprimé·es. On en parle peu, mais ils représentent une « cible » de 150 000 à 200 000 personnes en France, incluant les receveurs de greffes d’organes solides, de greffes allogéniques de cellules souches, les personnes atteintes d’hémopathies malignes, celles traitées par des anticorps anti-CD20, sous chimiothérapie ayant un déficit immunitaire acquis ou primitif sévère (dont les patients VIHVIH Virus de l’immunodéficience humaine. En anglais : HIV (Human Immunodeficiency Virus). Isolé en 1983 à l’institut pasteur de paris; découverte récemment (2008) récompensée par le prix Nobel de médecine décerné à Luc montagnier et à Françoise Barré-Sinoussi. + ayant moins de 200 CD4)… Une récente actualisation de la cohorte INFORM présentée au congrès de l’ECCMID à Barcelone en avril dernier1Dube S et al. Continued Increased Risk of COVID 19 Hospitalisation and Death in Immunocompromised Individuals Despite Receipt of ≥4 Vaccine Doses: Updated 2023 Results From INFORM, a Retrospective Health Database Study in England (Poster P0409) ; ECCMID 2024, 27-30 April 2024, Barcelona confirme à grande échelle les risques propres aux immunodéprimés. Au total, 12 024 035 patients âgés de ≥12 ans ont été inclus ; parmi eux 477 025 étaient des immunodéprimés (ID). La cohorte des ID était plus âgée et présentait plus de comorbidités que l’ensemble de la population. Près de 73% de la cohorte ID avait reçu ≥ 4 doses de vaccin Covid-19 avant le 1er janvier 2023, contre 30% de l‘ensemble de la population. La principale conclusion, qui vient corroborer les données déjà publiées notamment avant l’ère Omicron2Duly K, Farraye FA, Bhat S COVID-19 vaccine use in immunocompromised patients: A commentary on evidence and recommendations (Review) Am J Health Syst Pharm 2022 Jan 5;79(2):63-71. doi: 10.1093/ajhp/zxab344. 3Shoham S. et al. Lancet Commission on COVID-19 Vaccines and Therapeutics Task Force. Vaccines and therapeutics for immunocompromised patients with COVID-19. (Review) EClinicalMedicine. 2023 May:59:101965. doi: 10.1016/j.eclinm.2023.101965. Epub 2023 Apr 12. https://pubmed.ncbi.nlm.nih.gov/37070102/ est que, bien qu‘ils ne représentent que 4% de la population totale de l’étude, les ID représentaient 22,9% des hospitalisations et 22,3% des décès. Les personnes ID entièrement vaccinées représentaient quant à elles 24,4% des hospitalisations et 23% des décès.
Une des parades utilisées jusque-là face à la moindre réponse vaccinale chez ces patients immunodéprimés était le développement des anticorps monoclonaux (AcMc) en PrEPPrEP Prophylaxie Pré-Exposition. La PrEP est une stratégie qui permet à une personne séronégative exposée au VIH d'éliminer le risque d'infection, en prenant, de manière continue ou «à la demande», un traitement anti-rétroviral à base de Truvada®. (oui l’acronyme est aussi utilisé dans le Covid) tous mis en échec par la génération de variants Omicron et aussi, par les difficultés à atteindre la cible avec ces anticorps injectables. C’est ainsi que les associations tixagevimab/cilgavimab (Evusheld®), casirivimab/imdevimab (Ronapreve®) ou le sotrovimab XEVUDY® ne sont plus recommandés, ni en curatif, ni en prophylaxie depuis les circulaires DGS de 2022 et 2023 (DGS-URGENT N°2023-05 publié le 31/01/2023, DGS-URGENT N°2022-86, publié le 22/12/2022).
Pour prendre un seul exemple, l’association tixagévimab/cilgavimab (Evusheld®) a été prescrite chez environ 20 000 personnes sur les 200 000 de la cible. Depuis Omicron en 2022, plusieurs associations et sociétés savantes ont sonné le tocsin. Ils mettent en avant les chiffres issus du Royaume-Uni. Les personnes immunodéprimées y représentaient4Evans RA et al. Impact of COVID-19 on immunocompromised populations during the Omicron era: insights from the observational population-based INFORM study. Lancet Reg Health Eur.2023 Oct 13:35:100747. doi: 10.1016/j.lanepe.2023.100747. eCollection 2023 Dec. https://pubmed.ncbi.nlm.nih.gov/38115964/ 22% des hospitalisations Covid, 28% des soins critiques Covid et 25 % des décès liés au Covid. On sait que l’efficacité vaccinale (EV) est diminuée y compris après 3 doses de vaccins ARN-messager chez certaines populations de patients les plus immunodéprimés. L’étude de Britton5Britton A et al. Effectiveness of COVID-19 mRNA Vaccines Against COVID-19-Associated Hospitalizations Among Immunocompromised Adults During SARS-CoV-2 Omicron Predominance – VISION Network. MMWR Morb Mortal Wkly Rep . 2022 Oct 21;71(42):1335-1342. doi: 10.15585/mmwr.mm7142a4 https://pubmed.ncbi.nlm.nih.gov/36264840/ en 2022 montrait en effet que cette efficacité vaccinale 7 jours après la 3e dose était n’était que de 43% chez les patients transplantés d’organes solides ou de cellules souches hématopoïétique et de 70% chez les patients atteints de cancers solides. Tous les immunodéprimés ne sont pas dans la même échelle de risques de décès et de formes graves. L’étude SEVARVIR menée en France, et publiée depuis, montrait que, à l’ère des variants Omicron, 43% des patients infectés étaient immunodéprimés, dont 22% des patients transplantés d’organes solides6De Prost, N., Audureau, E., Heming, N. et al. Clinical phenotypes and outcomes associated with SARS-CoV-2 variant Omicron in critically ill French patients with COVID-19. Nat Commun 13, 6025 (2022). https://doi.org/10.1038/s41467-022-33801-z.
Ce risque est parfaitement perçu par les personnes immunodéprimées, comme en atteste un sondage réalisé par Ipsos pour le laboratoire AstraZeneca et 7 associations représentant les personnes immunodéprimées7Enquête réalisée par Ipsos pour les associations de patients EllyE, Fédération des greffés cœur et/ou poumon, France Rein, association Laurette Fugain, Renaloo, Transhépate et Vaincre la mucoviscidose, et le laboratoire Astra Zeneca.
Questionnaire auto-administré en ligne du 15 janvier au 5 février 2024, auprès d’un échantillon de 588 patients immunodéprimés et d’un échantillon de 1 500 personnes représentatives de la population française.. On y apprend que 73% des personnes immunodéprimées continuent de considérer le Covid-19 comme une menace grave pour leur santé (vs 49% des Français), 50% sont inquiets face aux risques de contracter le Covid-19 (vs 29% des Français), 30% des patients représentatifs des personnes immunodéprimées en France ont vécu un Covid-19 compliqué « dont 20% ont eu un Covid long et 17% ont été hospitalisées », 67% déclarent que la crainte de contracter le Covid-19 a toujours un impact sur leur quotidien, dont 30% un fort impact; 41% déclarent que le virus a eu au moins une conséquence négative sur leur suivi de pathologies. Dernier message fort malheureusement peu entendu par les autorités sanitaires: 93% des personnes immunodéprimées souhaiteraient que le port du masque soit obligatoire dans les établissements de soins.
Le renouveau des anticorps monoclonaux (AcMc)
Reste que l’espoir renait pour les personnes immunodéprimées avec l’émergence de nouveaux anticorps monoclonaux à longue durée d’action et adaptés aux nouveaux variants. Il en est ainsi du sipavibart (ex AZD3152) qui a eu récemment une autorisation en France pour un accès compassionnel pour les populations à très haut risque de Covid-19 sévère. Il est efficace en neutralisation in vitro sur les sous-lignages XBB ne portant pas la mutation F456L et sur les variants issus de BA2.86 incluant JN.18Francica JR, Cai Y, Diallo S, et al. 1355. The SARS-CoV-2 Monoclonal Antibody AZD3152 Potently Neutralizes Historical and Emerging Variants and is Being Developed for the Prevention and Treatment of COVID-19 in High-risk Individuals. Open Forum Infect Dis. 2023 Nov 27;10(Suppl 2):ofad500.1192. doi: 10.1093/ofid/ofad500.1192.
Cai Y, Diallo S, Rosenthal K et al. AZD3152 neutralizes SARS-CoV-2 historical and contemporary variants and is protective in hamsters and well tolerated in adults. Sci Transl Med. 2024 Jun 26;16(753):eado2817. doi: 10.1126/scitranslmed.ado2817. Epub 2024 Jun 26 https://www.science.org/doi/10.1126/scitranslmed.ado2817
Francica JR, , Cai Y, Diallo S, et al. The SARS-CoV-2 Monoclonal Antibody AZD3152 Potently Neutralises Historical and Currently Circulating Variants. Poster presented at: ECCMID, 15–18 April 2023, Copenhagen, Denmark. Poster: P2636.
Francica JR, Cai Y, Diallo S, et al. The SARS-CoV-2 monoclonal antibody AZD3152 potently neutralises historical and emerging variants and is being developed for the prevention and treatment of COVID-19 in high-risk individuals [poster]. Presented at: IDWeek 2023; October 11-15, 2023; Boston, MA, United States. Poster: 1355.. L’originalité de cet anticorps préventif, le sipavibart, est qu’il est dérivé de cellules B données par des patients convalescents après une infection par le Sars-CoV-2 et optimisé avec la même prolongation de la demi-vie (6 mois), une fonction effectrice Fc réduite et une plateforme de liaison au complément (C1q)9Francica JR, Cai Y, Diallo S, et al. 1355. The SARS-CoV-2 Monoclonal Antibody AZD3152 Potently Neutralizes Historical and Emerging Variants and is Being Developed for the Prevention and Treatment of COVID-19 in High-risk Individuals. Open Forum Infect Dis. 2023 Nov 27;10(Suppl 2):ofad500.1192. doi: 10.1093/ofid/ofad500.1192.. La fonction effectrice Fc réduite vise à minimiser le risque de renforcement de l’infection dépendant des anticorps (ADCC) – un phénomène dans lequel les anticorps spécifiques du virus favorisent, plutôt qu‘ils n’inhibent, l‘infection et/ou la maladie. Qui plus est, il est administrable en intramusculaire ce qui devrait faciliter son accès.
Les principaux résultats qui ont permis l’accès compassionnel sont issus de l’étude Supernova. L’étude Supernova est une étude de phase I/III en double aveugleDouble aveugle L'étude avec répartition aléatoire, randomisé ou en double insu (ou en double aveugle) est une démarche expérimentale utilisée en recherche médicale et pharmaceutique faisant que ni le patient ni le médecin ne sait quel traitement est pris : traitement A ou B, traitement A ou placébo. et randomisée. La phase I évalue la sécurité, la pharmacocinétique de l’AZD5156 (association AZD3152+cilgavimab) vs placeboPlacebo Substance inerte, sans activité pharmacologique, ayant la même apparence que le produit auquel on souhaite le comparer. (NDR rien à voir avec le groupe de rock alternatif formé en 1994 à Londres par Brian Molko et Stefan Olsdal.) . La phase III évalue l’efficacité et la tolérance du sipavibart par rapport au tixagevimab/cilgavimab et/ou au placebo en prévention d’un Covid-19 symptomatique. À ce jour, l’activité de neutralisation du sipavibart a uniquement été publié sur la base d’étude in vitro sur les variants qui ont circulé jusqu’à JN.1. Ensuite, l’étude LITTLE DIPPER de phase I, en double aveugle, randomisée, d’exploration des doses, évalue l’innocuité et la pharmacocinétique du sipavibart. Le développement de type d’anticorps nécessite, comme pour les vaccins de s’adapter à l’évolution des variants. Pour cela les industriels des vaccins et des AcMc peuvent avoir recours à la méthode de l’immunobridging. Une approche scientifique et réglementaire qui permet, suite à la mise en évidence de l’efficacité d’un vaccin ou d’un anticorps chez une population donnée, d’extrapoler l’efficacité dans d’autres situations (groupe d’âge ou populations différentes, doses différentes ou schéma vaccinal différent, plateforme vaccinale différente, etc.). Lorsque c’est scientifiquement justifié, par exemple en cas de variation des souches circulantes, cette méthode permet de se baser sur la réponse immune conférant la protection et de se passer d’un nouvel essai d’efficacité clinique.
Ainsi, pour le développement par AstraZeneca de l’AZD3152, bien que les variants SARS-CoV-2 en circulation soient différents de ceux qui étaient en circulation lors de l’approbation de tixagevimab/cilgavimab, l’immunobridging permet d’évaluer l’efficacité clinique sur les nouveaux variants, en se basant sur le pouvoir neutralisant des anticorps in vitro post-administration de l’AZD3152. Plusieurs études et une méta-analyse ont montré que le taux d’AC neutralisants permettait d’estimer la protection vis-à-vis du Covid-19 symptomatique avec un excellent taux de corrélation. L’étude SUPERNOVA démontre qu’AZD3152 neutralise les variants VOC majoritairement en circulation aujourd’hui, aussi efficacement que tixagevimab/cilgavimab neutralisait les VOC vis-à-vis desquels son efficacité clinique (PrEP) a été mise en évidence.
D’autres AcMc sont en cours de développement. Une récente revue de la littérature parue dans CMI fait pourtant état d’un pipeline assez modeste : «le pipeline clinique d’anticorps monoclonaux anti-spike est actuellement limité à quelques agents (la plupart étant des anticorps uniques) dont l’efficacité contre la sous-lignée dominante JN.1 est inconnue. Le domaine des thérapies à base d’anticorps a besoin d’être stimulé à la fois par les fabricants et les institutions», soulignent les auteurs. Sont présentées les données parcellaires du VYD222 d’Invivyd, du REGN-17092 de Regeneron et de l’AER-800 d’Aerium Therapeutics10Focosi D, Franchini M, Casadevall 4, Maggi F. An update on the anti-spike monoclonal antibody pipeline for SARS-CoV-2. . 2024 Aug;30(8):999-1006. doi: 10.1016/j.cmi.2024.04.012. Epub 2024 Apr 24. Review Clin Microbiol Infect.
D’autres approches sur des modèles animaux proposent les anticorps synthétiques codés dans l’ADN (DMAb), constituant une stratégie importante pour l’administration directe in vivo d’un AcM protecteur. L’administration prophylactique a protégé les macaques rhésus contre les signes de la maladie pulmonaire associée au Sars-CoV-2 (USA-WA1/2020). Dans l’ensemble, ces données plaident en faveur d’une étude plus approfondie des anticorps codés dans l’ADN en tant que mode d’administration supplémentaire pour la prévention des maladies graves liées au Covid-19. Ces données ont des implications pour la transposition chez l’homme des AcM codés dans les gènes pour les maladies infectieuses émergentes et l’administration d’AcM à faible dose contre le Covid-1911Patel A, Rosenke K, Parzych E et al. In vivo delivery of engineered synthetic DNA-encoded SARS-CoV-2 monoclonal antibodies for pre-exposure prophylaxis in non-human primates. Emerg Microbes Infect. 2024 Dec;13(1):2294860. doi: 10.1080/22221751.2023.2294860. Epub 2024 Feb 28..
