C’était l’un des moments forts des 25e journées nationales d’infectiologie (JNI) qui se déroulaient à Deauville du 12 au 14 juin 2024: le symposium du laboratoire Takeda sur la dengue au cœur de la lutte contre cette «menace sans frontières», qui faisait suite à une session de communications orales entièrement dédiée à la dengue. Les présentations abordaient notamment les risques en Hexagone à quelques semaines des Jeux olympiques, que les cas soient importés ou autochtones.
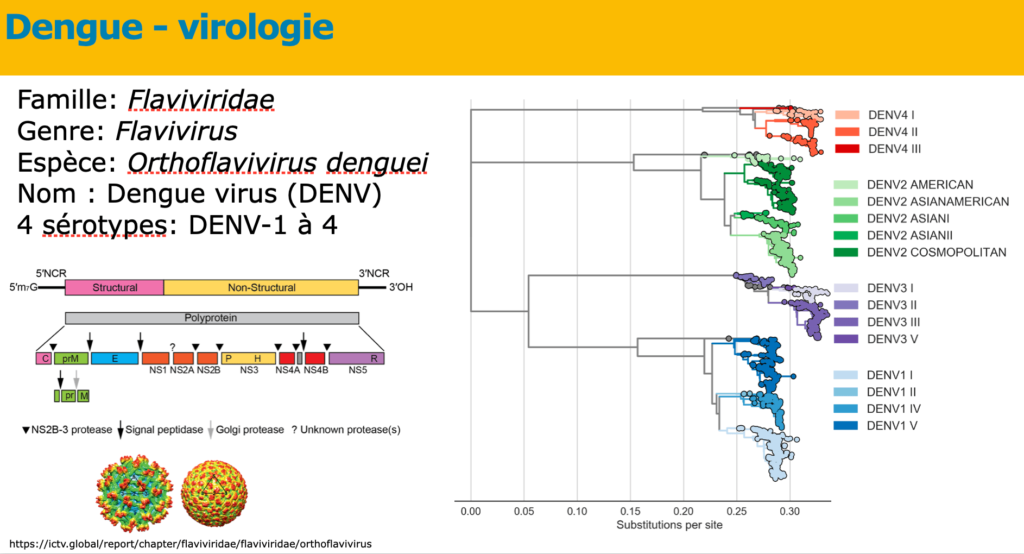
Les principaux sujets abordés ont été l’augmentation des cas de dengue en France hexagonale, l’arrêt de la commercialisation du vaccin disponible lors de la communication du Pr André Cabié du CHU de Martinique, l’annonce d’un nouveau vaccin contre la dengue prometteur et la lutte antivectorielle, dans une perspective One Health. Abordés également, la question plus spécifique des risques présentés par les arbovirosesArbovirose Les arboviroses sont des maladies virales dues à des arbovirus transmis obligatoirement par un vecteur arthropode (moustique, moucheron piqueur, tique) à des hôtes vertébrés (mammifères, oiseaux), d’où leur nom adapté de l’anglais : ARthropod-BOrne virus. en cas de grossesse, au-delà du cas connu de Zika. Une cuvée des JNI avec, donc, la dengue à tous les étages.

Aujourd’hui, le vaccin TAK-003 (Qdenga®), est désormais le seul vaccin contre la dengue disposant d’une autorisation de mise sur le marché en Europe. En France, on attend à la fois les recommandations du comité technique des vaccinations (CTV) et de la Haute Autorité de santé (HAS) pour ce médicament, et bien sûr, de connaître la fixation de son prix.
Le précédent vaccin non recommandé en France
En janvier 2019, une stratégie de vaccination contre la dengue avait été définie pour le vaccin Dengvaxia® (CYD-TDV). On se souvient de la polémique et du débat juridique entre le gouvernement des Philippines et le fabricant du vaccin. Ce dernier étant accusé par les autorités des Philippines d’avoir entraîné des centaines de morts d’enfants dans le cadre d’une des plus vastes opérations de vaccination contre la dengue. Huit cent mille enfants avaient été vaccinés lors d’une campagne où se sont mêlés les limites du vaccin en termes de sérotype et en cas de sérologieSérologie Étude des sérums pour déterminer la présence d’anticorps dirigés contre des antigènes. négative, les peurs et les controverses, comme présenté dans cette publication de Yu et al., «Fear, mistrust, and vaccine hesitancy: Narratives of the dengue vaccine controversy in the Philippines»1En décembre 2017, près de deux ans après le lancement du programme – et alors que plus de 800 000 écoliers philippins ont déjà reçu au moins une dose du vaccin – Sanofi a annoncé que Dengvaxia pourrait en fait être dangereux pour certaines populations. Le programme est immédiatement devenu une cause célèbre aux Philippines. Quelques jours après l’annonce, la presse écrite, audiovisuelle et en ligne2 a relayé 3les informations faisant état d’enfants vaccinés décédés ou tombés gravement malades à cause de la dengue. L’administration Duterte a lancé des enquêtes criminelles contre des hommes politiques de haut rang et des responsables du ministère de la Santé qui avaient lancé le programme de vaccination, la plupart d’entre eux appartenant à l’opposition ou à l’administration précédente, tandis que le bureau du procureur général (PAO) menait sa propre enquête très médiatisée impliquant des autopsies télévisées et des entretiens avec des familles endeuillées. Ces investigations, tant sur les aspects cliniques que politiques du programme, se sont poursuivies au cours des mois suivants et ont bénéficié d’une couverture médiatique constante ; à un moment donné, un groupe d’experts de l’Hôpital général des Philippines, le centre de référence du gouvernement national, a même dû demander publiquement au ministère de la Justice d’intervenir contre la gestion sensationnaliste des événements par la PAO..
Il avait été alors constaté que les participants séronégatifs vaccinés présentaient un risque deux fois plus élevé de dengue sévère et d’hospitalisation que les participants non vaccinés. La vaccination entraîne la production d’anticorps facilitants qui favoriseraient la survenue de forme grave plus encore qu’une première infection connue comme étant un facteur de risque de forme grave amplifié par les comorbidités [âge, obésité, bronchopneumopathie chronique obstructive (BPCO), diabète, etc.].
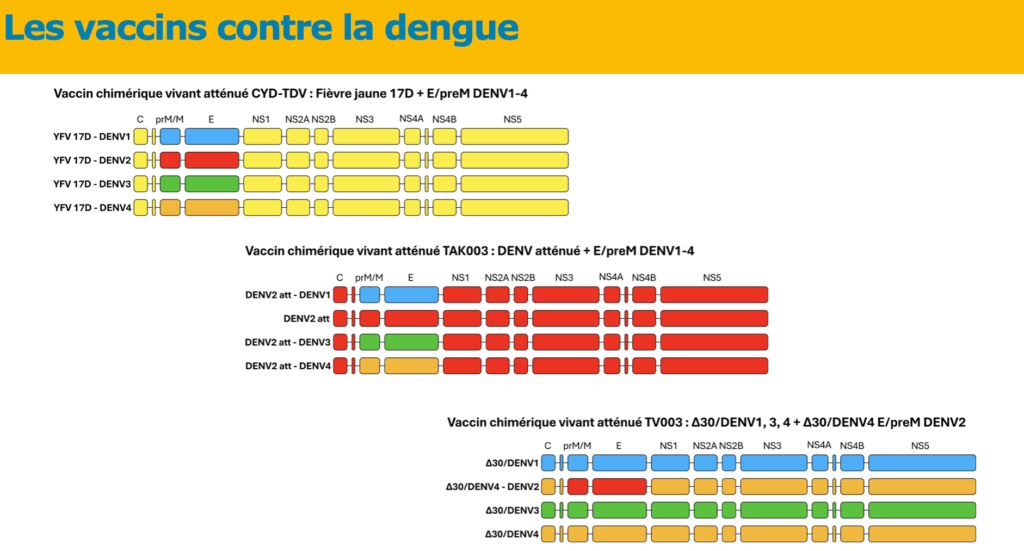
Rappelons que le Dengvaxia® a obtenu le 12 décembre 2018 une AMMAMM Autorisation de Mise sur le Marché. Procédure administrative qui autorise un laboratoire pharmaceutique à commercialiser une molécule. européenne restreinte aux personnes âgées de 9 à 45 ans ayant un antécédent d’infection par le virus de la dengue confirmé biologiquement, ce qui a considérablement limité son utilisation. En 2019, la HAS n’a pas recommandé l’utilisation de Dengvaxia® sur l’île de la Réunion et à Mayotte malgré la poussée endémique. Ces recommandations n’ont pas été modifiées par le nouvel avis de la HAS datant du 30 juin 2022.
Vers une nouvelle stratégie de vaccination française
Suite à l’autorisation de mise sur le marché du vaccin de Takeda par la Commission européenne le 5 décembre 2022, la Direction générale de la santé (DGS) a saisi la Haute Autorité de santé (HAS) le 3 avril 2023 pour qu’elle révise sa stratégie face à la dengue en incluant l’évaluation du Qdenga®. La DGS souhaite que l’évaluation du vaccin Qdenga® soit effectuée en fonction de l’âge, du statut immunitaire et des comorbidités et que les recommandations en attente couvrent l’hexagone et les départements et régions d’outre-mer.
Notons que le TAK-003 a été préqualifié par l’Organisation mondiale de la Santé (OMS) le 10 mai 2024, second vaccin, donc, contre la dengue à être préqualifié par l’OMS. La préqualification OMS est une étape importante dans l’élargissement de l’accès mondial aux vaccins, car elle permet leur achat par les organisations du système des Nations unies, notamment l’Unicef et l’Organisation panaméricaine de la santé.
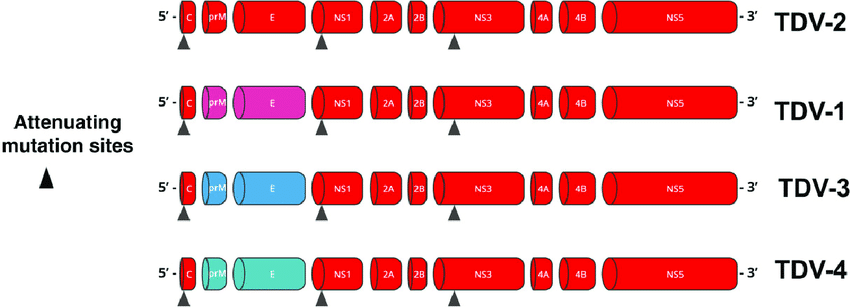
Les JNI ont été l’occasion de rappeler la feuille de route type d’un vaccin contre la dengue : démontrer une protection croisée contre les 4 types de virus, diminuer le risque inhérent à cette arboviroseArbovirose Les arboviroses sont des maladies virales dues à des arbovirus transmis obligatoirement par un vecteur arthropode (moustique, moucheron piqueur, tique) à des hôtes vertébrés (mammifères, oiseaux), d’où leur nom adapté de l’anglais : ARthropod-BOrne virus. virale de survenue d’anticorps facilitants ayant un effet délétère — surtout après une première infection par un des virus de la dengue —, contourner l’absence de modèle animal satisfaisant et la difficulté d’avoir des corrélats de protection en termes de taux d’anticorps neutralisants.
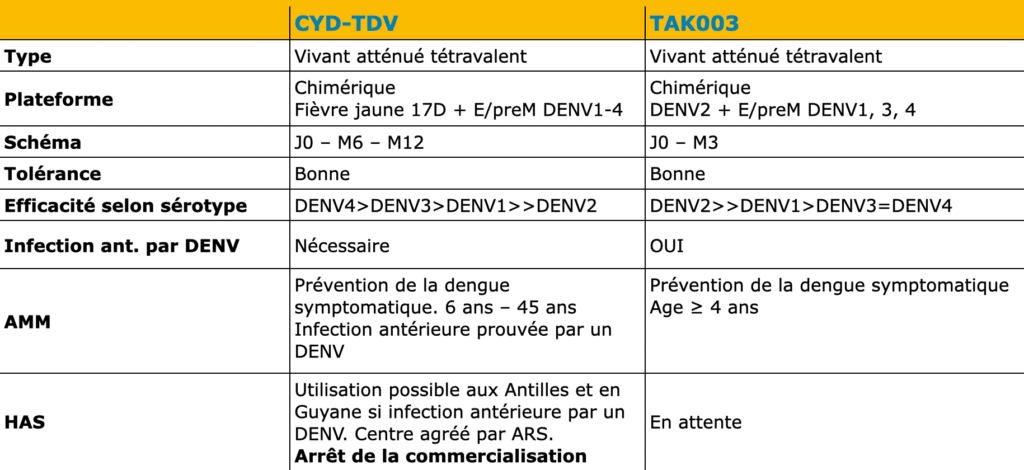
Sur le plan théorique, trois vaccins ont été développés : le CYD-TDV de Sanofi, actuellement retiré, le TAK-003 de Takeda et un autre vaccin chimérique vivant atténué, le TV003 en cours de développement.
Pour l’heure, c’est ce second vaccin qui attire tous les regards. Il s’agit d’un vaccin vivant, tétravalent et chimérique qui, à la différence du vaccin Dengvaxia® de Sanofi, utilise comme base un virus dengue sérotype 2 atténué (et non le virus de la fièvre jaune atténué). L’essai pivot qui a permis cette autorisation de mise sur le marché a débuté en 2016, auprès de 20 071 enfants âgés de 14 à 16 ans dans un essai randomisé avec contrôle par placeboPlacebo Substance inerte, sans activité pharmacologique, ayant la même apparence que le produit auquel on souhaite le comparer. (NDR rien à voir avec le groupe de rock alternatif formé en 1994 à Londres par Brian Molko et Stefan Olsdal.) dans 8 pays d’Asie et d’Amérique à forte activité endémique. L’efficacité pour prévenir une dengue symptomatique 18 mois après les deux injections de vaccination était globalement de 80,2% (73,3% – 85,3%), chez les personnes séronégatives vis-à-vis de la dengue, l’efficacité était de 66,2% et elle varie en fonction du sérotype, allant de 95% pour DENV-2 à 48,9% pour DENV-3. Cinq ans après la première injection, cette efficacité globale était encore de 61,2% (56% – 65,8%). L’efficacité vaccinale vis-à-vis du risque d’hospitalisation est de 90,4% 18 mois après la deuxième dose4Biswal S, Reynales H, Saez-Llorens X, et al TIDES Study Group. Efficacy of a Tetravalent Dengue Vaccine in Healthy Children and Adolescents. N Engl J Med. 2019 Nov 21;381(21):2009-2019. doi: 10.1056/NEJMoa1903869. Epub 2019 Nov 6.
Biswal S, Borja-Tabora C, Martinez Vargas L. et al TIDES study group. Efficacy of a tetravalent dengue vaccine in healthy children aged 4-16 years: a randomised, placebo-controlled, phase 3 trial. Lancet. 2020 May 2;395(10234):1423-1433. doi: 10.1016/S0140-6736(20)30414-1. Epub 2020 Mar
Rivera L, Biswal S, Sáez-Llorens X. et al. Three-year Efficacy and Safety of Takeda’s Dengue Vaccine Candidate (TAK-003) Clin Infect Dis. 2022 Aug 24;75(1):107-117. doi: 10.1093/cid/ciab864. PMID: 34606595 Free PMC article. Clinical Trial. Aucun effet indésirable grave n’a été rapporté dans les différentes publications si l’on excepte 16 cas d’anaphylaxie décrits au Brésil, dont 3 chocs anaphylactiques avec une fréquence faible évaluée à 0,8 pour 100 000 doses.
L’OMS a recommandé d’utiliser le TAK-003 chez les enfants âgés de 6 à 16 ans dans les zones de transmissions élevées de la dengue. Le vaccin doit être administré 1 à 2 ans avant l’âge correspondant au pic incident d’hospitalisations. Sachant qu’une vaccination de rattrapage peut être envisagée pour d’autres groupes d’âge notamment les 6-16 ans et les personnes ayant des comorbidités. Enfin, et c’est un sujet majeur, mais qui ne se retrouve pas dans toutes les recommandations, le dépistage sérologique pré-vaccinal, qui était un obstacle majeur pour le précédent vaccin, n’est pas recommandé dans l’AMM européenne. On peut préciser, comme l’a fait Christophe RAPP (Hôpital américain), que ces « zones de transmissions élevées de la dengue » sont définies par une séroprévalence à l’âge de 9 ans supérieure à 60% et un pic des hospitalisations de dengue avant l’âge de 16 ans.
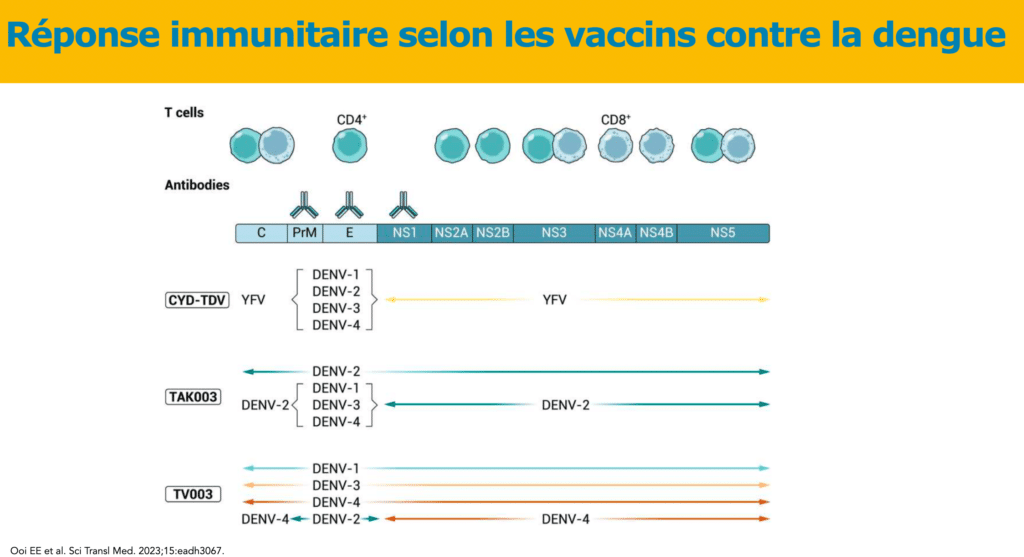
Besoin de clarification
Par ailleurs, l’Organisation panaméricaine de la santé (OPS) s’est alignée sur les recommandations de l’OMS et a demandé au laboratoire Takeda de réaliser des études de phase 4 pour apporter des réponses aux incertitudes sur l’efficacité du vaccin contre DENV-3 et DENV-4 chez les individus séronégatifs de la dengue.
Chez les personnes qui vivent dans des pays où la dengue n’est pas endémique et qui ont déjà été infectés par l’un quelconque des 4 sérotypes du virus à la suite d’un voyage, la vaccination par le TAK-003 peut être utile pour prévenir une deuxième infection. La protection débute 14 jours après la première dose.
Si l’on compare les recommandations belges, suisses, allemandes, espagnoles, on constate des positions différentes quant au fait d’avoir déjà contracté ou non la dengue pour recommander cette vaccination. En Belgique et en Suisse par exemple, avoir eu la dengue rentre dans les critères d’indication alors qu’en Allemagne, cette vaccination est indépendante du statut sérologique vis-à-vis de la dengue. On attend avec impatience la clarification des autorités françaises sur ce point.
Des questions en suspens
Après la désillusion du premier vaccin contre la dengue, développé à partir d’une souche atténuée du virus de la fièvre jaune, et la polémique autour des décès d’enfants aux Philippines, un certain nombre de questions demeurent.
Notamment la question sur le territoire français de l’hésitation vaccinale , extrêmement présente dans les Antilles et en Guyane, des régions particulièrement concernées par l’épidémie actuelle de dengue. Cette hésitation face à la vaccination avait d’ailleurs pris de l’ampleur lors de la crise du CovidCovid-19 Une maladie à coronavirus, parfois désignée covid (d'après l'acronyme anglais de coronavirus disease) est une maladie causée par un coronavirus (CoV). L'expression peut faire référence aux maladies suivantes : le syndrome respiratoire aigu sévère (SRAS) causé par le virus SARS-CoV, le syndrome respiratoire du Moyen-Orient (MERS) causé par le virus MERS-CoV, la maladie à coronavirus 2019 (Covid-19) causée par le virus SARS-CoV-2. Aucune donnée n’est actuellement disponible sur l’acceptabilité, aux Antilles et en Guyane, de ce type de vaccin et de ses modalités d’administration. Même question sur l’impact négatif qu’aurait pu avoir la polémique aux Philippines sur Dengvaxia®, qui avait vu reculer d’autres vaccinations : la vaccination contre la rougeole aura vu sa couverture vaccinale baisser de 80 à 50%.
Il reste que la dengue constitue un danger de santé publique majeur qui justifie toute recherche vaccinale : on estime de 100 à 400 millions le nombre de cas dans le monde chaque année et à 3,8 milliards la population vivant dans des pays où la maladie est endémique (Asie, Afrique, Amériques). Sachant que l’année 2023 est celle qui a vu le plus grand nombre de cas de dengues jamais signalé auparavant avec 2 300 décès rapportés par l’Organisation mondiale de la santé et pour ce qui concerne la France, le double record à la fois de dengue autochtone et de dengue d’importation qui se confirment pour les premiers mois de 2024. Dans le contexte spécifique de la France, la question de l’acceptation d’un tel vaccin, après les polémiques sus-citées et le climat d’hésitation vaccinale notamment dans les Antilles et en Guyane, demeure un immense point d’interrogation5Lucarelli MA, Vignier N, Mergeayfabre M, Clerc Renaud A, Mulot S, Odonne G, Epelboin L. Covid and society in French Guiana and the French West Indies Scientific day – March 25, 2022 – Cayenne, French Guiana. Med Trop Sante Int. 2022 Aug 29;2(3):mtsi.v2i3.2022.270. doi: 10.48327/mtsi.v2i3.2022.270. eCollection 2022 Sep 30..
