En France, la transplantation rénale entre donneurs et receveurs séropositifs (D+/R+) est possible depuis juillet 2021 grâce à la mobilisation des associations comme le TRT-5 CHV, et elle a permis une douzaine de greffes entre 2022 et 2024. Aux États-Unis, elle s’est développée depuis 2013 et l’adoption du HIV Organ Policy Equity (HOPE) Act. Une étude secondaire de l’essai «HOPE in Action», menée sur 198 transplantations, apporte des éléments rassurants, tout en identifiant certaines particularités infectieuses.
Les chercheurs ont comparé 99 transplantations D+/R+ à 99 transplantations D-/R+ issues de 26 centres américains. Les receveurs devaient présenter un taux de CD4 supérieur à 200 cellules/µL et une charge viraleCharge virale La charge virale plasmatique est le nombre de particules virales contenues dans un échantillon de sang ou autre contenant (salive, LCR, sperme..). Pour le VIH, la charge virale est utilisée comme marqueur afin de suivre la progression de la maladie et mesurer l’efficacité des traitements. Le niveau de charge virale, mais plus encore le taux de CD4, participent à la décision de traitement par les antirétroviraux. indétectable. Les donneurs séropositifs ne devaient avoir aucune infection opportuniste active. Le critère principal évaluait le délai de survenue de la première infection cliniquement significative dans les 24 mois post-transplantation, définie selon les critères de la Swiss Transplant Cohort Study.
Résultats principaux
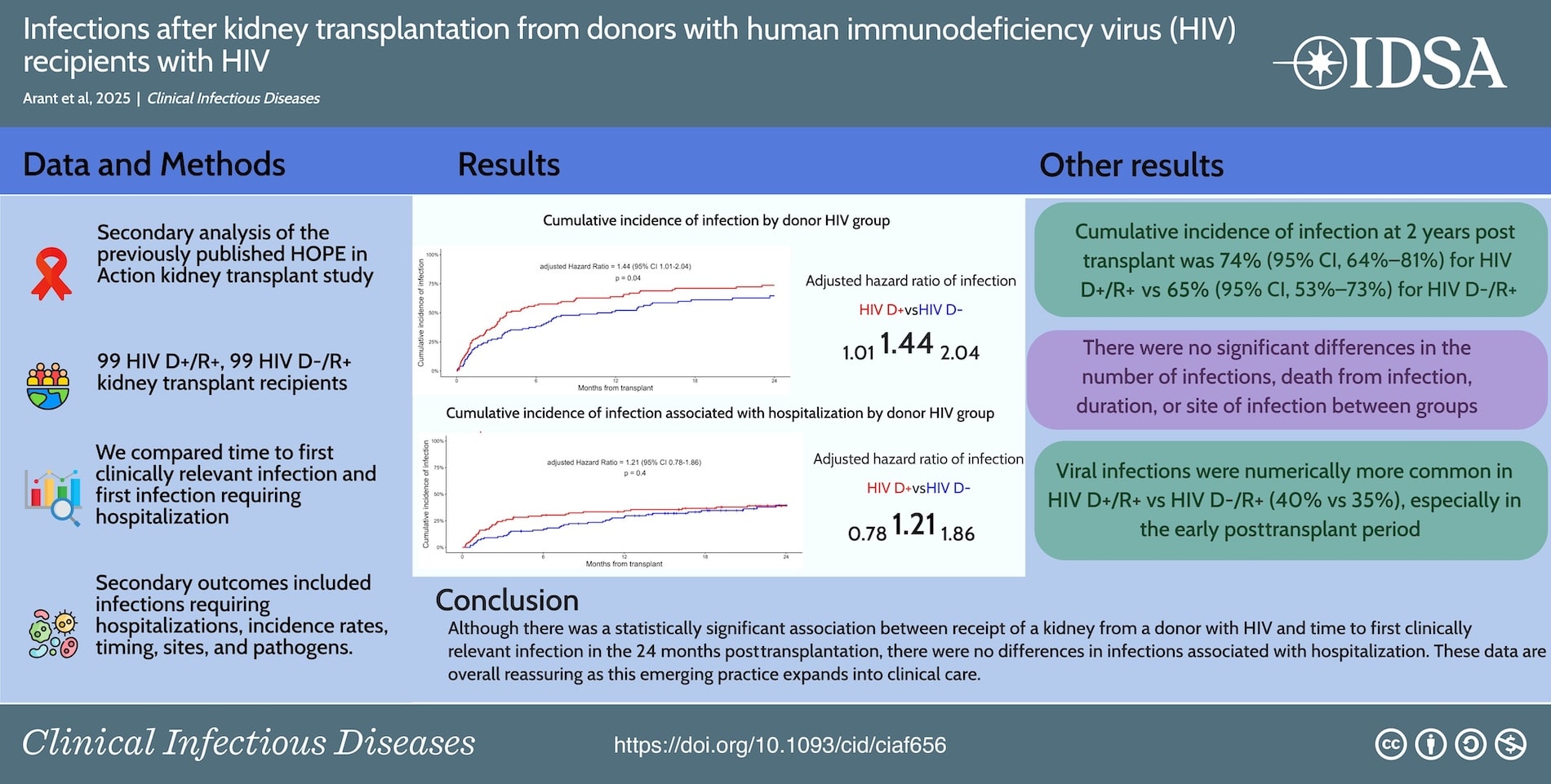
L’incidence cumulée d’au moins une infection à 24 mois atteignait 73,8% en D+/R+ contre 64,7% en D-/R+. Le hazard ratio ajusté de 1,44 (IC 95% : 1,01-2,04) traduit une association statistiquement significative entre le statut sérologique du donneur et la survenue précoce d’infection. Le pic d’infections survenait durant le premier mois post-transplantation : 34,9 pour 100 personnes-mois en D+/R+ contre 24,4 en D-/R+. Toutefois, aucune différence n’était observée concernant les infections nécessitant une hospitalisation, ce qui suggère que le surrisque concerne principalement des infections moins graves. Le nombre total d’infections et le taux global d’incidence ne différaient pas significativement entre groupes.
Les infections bactériennes dominaient dans les deux groupes (45% des infections en D+/R+, 56% en D-/R+), avec une prédominance d’Escherichia coli et Klebsiella pneumoniae. Les infections à Clostridioides difficile concernaient 8% des receveurs, légèrement au-dessus des données habituelles, avec un nombre de cas plus élevé dans le groupe D-/R+ que dans le groupe D+/R+ (11 contre 5).
Les infections virales montraient une tendance non significative vers plus de cas en D+/R+ (40% versus 33%). Le SARS-CoV-2 prédominait dans les deux groupes. Les infections à cytomégalovirus (CMV) sont restées rares (11% versus 7% des infections virales). Le virus BK mérite une attention particulière : 28% des infections virales en D+/R+ contre 22% en D-/R+. Bien que la plupart correspondaient à des virémies sans néphropathie, 71% ont nécessité une réduction d’immunosuppression. Cette observation soulève l’hypothèse d’une transmission possible par le greffon.
Les infections opportunistes sont restées exceptionnelles et comparables (4% des infections dans chaque groupe), avec une prédominance d’infections herpétiques et de candidoses œsophagiennes. Les trois cas de sarcome de Kaposi sont survenus exclusivement en D-/R+, et sont probablement des cas de réactivation chez le receveur.
La mortalité infectieuse s’est révélée négligeable : 2% en D+/R+ et 4% en D-/R+, tous les décès étant liés au Covid-19Covid-19 Une maladie à coronavirus, parfois désignée covid (d'après l'acronyme anglais de coronavirus disease) est une maladie causée par un coronavirus (CoV). L'expression peut faire référence aux maladies suivantes : le syndrome respiratoire aigu sévère (SRAS) causé par le virus SARS-CoV, le syndrome respiratoire du Moyen-Orient (MERS) causé par le virus MERS-CoV, la maladie à coronavirus 2019 (Covid-19) causée par le virus SARS-CoV-2.
Implications et questionnements éthiques
Cette étude apporte de nouveaux arguments solides pour l’utilisation de greffons de donneurs séropositifs. Le surrisque infectieux, bien que statistiquement significatif, reste cliniquement modéré et doit être mis en balance avec les bénéfices : réduction du temps d’attente et augmentation de l’accès à la greffe pour les personnes vivant avec le VIHVIH Virus de l’immunodéficience humaine. En anglais : HIV (Human Immunodeficiency Virus). Isolé en 1983 à l’institut pasteur de paris; découverte récemment (2008) récompensée par le prix Nobel de médecine décerné à Luc montagnier et à Françoise Barré-Sinoussi.
L’expansion récente de cette pratique au-delà du cadre de recherche nécessitera une vigilance particulière durant les premiers mois après la transplantation. Le développement de protocoles standardisés de surveillance, notamment pour le virus BK et le CMV, constitue une priorité pour optimiser la prise en charge de ces patients.
Aux États-Unis, la position officielle du Réseau uni pour le partage d’organes (UNOS) est que les patients séropositifs asymptomatiques «ne devraient pas nécessairement être exclus de la liste des candidats à la transplantation d’organes». Mais dans la pratique, la plupart des centres craignent les risques qu’une greffe peut faire courir aux patients vivant avec le VIH et estiment que les greffons, rares, ne doivent pas être attribués à des patients dont le pronostic risque d’être défavorable. Par ailleurs, les compagnies d’assurance refusent généralement de prendre en charge la transplantation hépatique chez les patients séropositifs.
Un autre article majeur du New England Journal of Medecine a ainsi résumé ces deux questions éthiques distinctes qui se posent donc à propos de l’efficacité : la transplantation est-elle bénéfique pour les patients concernés? Serait-il plus intéressant (en terme de bénéfice collectif) de réserver ces greffes à d’autres patients que des patients séropositifs?
Même si les receveurs de transplantation séropositifs présentent des résultats légèrement moins favorables, rappelons que l’efficacité relative n’est pas le seul critère éthique pour déterminer l’éligibilité. En effet, l’un des autres critères important en transplantation cardiaque, pulmonaire et hépatique est l’urgence médicale. Ce qui explique pourquoi les patients ayant besoin d’une transplantation rapide en bénéficient systématiquement, même si leur espérance de vie est considérablement réduite.
Référence
Elizabeth C Arant, Thibaut Davy-Mendez, Tao Liang, Moreno Rodrigues, Cynthia L Gay, Meenakshi M Rana, Rachel Friedman-Moraco, Alexander Gilbert, Peter Stock, Sapna A Mehta, Shikha Mehta, Valentina Stosor, Marcus R Pereira, Michele I Morris, Jonathan Hand, Saima Aslam, Maricar Malinis, Ghady Haidar, Catherine B Small, Carlos A Q Santos, Joanna Schaenman, John W Baddley, David Wojciechowski, Emily A Blumberg, Karthik Ranganna, Oluwafisayo Adebiyi, Nahel Elias, Jose A Castillo-Lugo, Emmanouil Giorgakis, Senu Apewokin, Megan Morsheimer, Christian van Delden, Oriol Manuel, Nicolas J Mueller, Dionysios Neofyotos, Aaron A R Tobian, Allan Massie, Dorry L Segev, William Werbel, Christine M Durand, Infections After Kidney Transplantation From Donors With Human Immunodeficiency Virus (HIV) to Recipients With HIV, Clinical Infectious Diseases, 2026;, ciaf656, https://doi.org/10.1093/cid/ciaf656
