Une bonne nouvelle dans le champ souvent difficile de la recherche d’un vaccin préventif contre le VIH: les premiers résultats de la phase 1 de l’essai ANRS VRI06 visant à évaluer un vaccin préventif contre le VIHVIH Virus de l’immunodéficience humaine. En anglais : HIV (Human Immunodeficiency Virus). Isolé en 1983 à l’institut pasteur de paris; découverte récemment (2008) récompensée par le prix Nobel de médecine décerné à Luc montagnier et à Françoise Barré-Sinoussi. montrent que le candidat, «CD40.HIVRI.Env», induit des réponses immunes précoces, fortes et durables. Il est néanmoins important de noter que l’efficacité du vaccin reste encore à démontrer, malgré ces résultats préliminaires encourageants.
Ces données ont été présentées par l’Inserm-ANRS et le Vaccine Research Institute (ANRS et Université Paris-Est Créteil) le 21 février 2023 à la CROICROI «Conference on Retroviruses and Opportunistic Infections», la Conférence sur les rétrovirus et les infections opportunistes annuelle où sont présentés les dernières et plus importantes décision scientifiques dans le champs de la recherche sur le VIH. 2023. Ce candidat vaccin repose sur l’injection d’anticorps monoclonaux ciblant spécifiquement un récepteur, la molécule CD40, à la surface des cellules dendritiques. Dans cette phase 1, l’objectif est d’analyser la tolérance et l’immunogénicitéImmunogénicité Capacité à produire une réponse immunitaire. de différentes doses du vaccin CD40.
Une première analyse intermédiaire
Le recrutement des personnes nécessaires pour mener l’essai de phase I s’est terminé en France et en Suisse en octobre 2022, avec 72 personnes. L’analyse intermédiaire des résultats porte sur 36 volontaires, âgés en moyenne de 34 ans et des hommes à 64%. Un premier groupe de 12 personnes a reçu par voie sous cutanée une dose de 0,3 mg de vaccin à l’inclusion et aux semaines 4 et 24. Le second et le troisième groupe ont ensuite reçu respectivement des doses de 1 et 3 mg selon le même schéma.
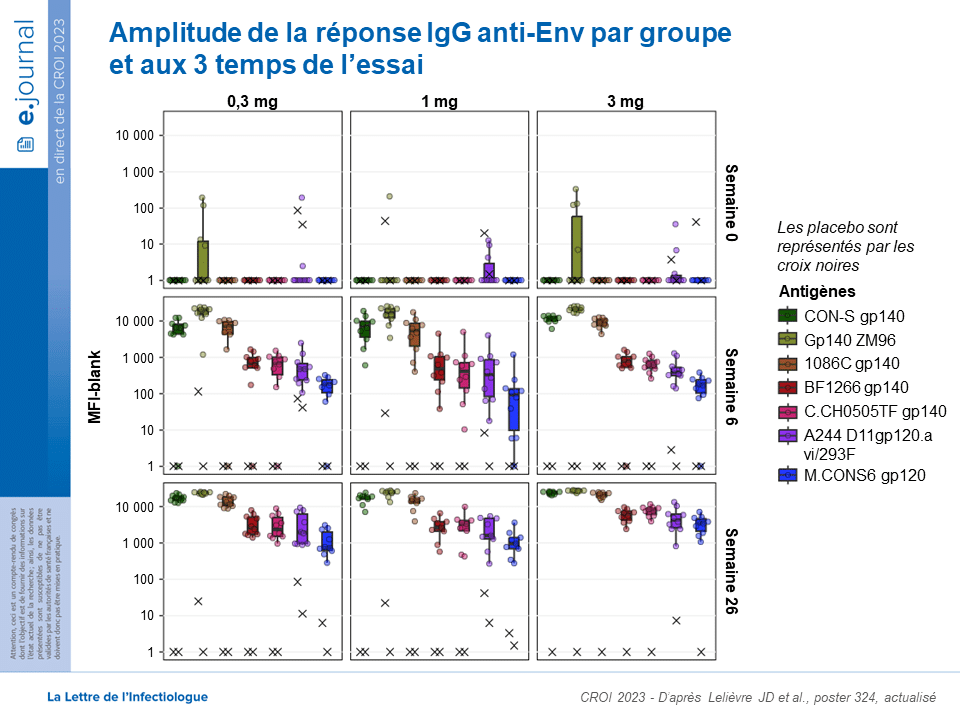
CROI 2023 – D’après Lelièvre JD et al., poster 324, actualisé
Source : Le e-journal de La lettre de l’infectiologue.
Les résultats à S26 des 36 volontaires sains ont montré que le vaccin présentait une bonne tolérance avec des événements de réactogénicité locale et systémique fréquents, de grade 1 ou 2. Deux effets secondaires sévères ont été rapportés mais ils ont été analysés comme non liés à la vaccination.
L’équipe a observé que le vaccin induisait des taux élevés d’anticorps dirigés contre les protéines d’enveloppe du VIH: Les taux de réponse des immunoglobulines de type G (IgG) contre les glycoprotéines d’enveloppe gp140 et gp120 étaient de 80 à 100 % à S6, et de 100 % à S26 dans tous les groupes avec une stabilité voire une légère diminution à S48.
Des anticorps ciblant une zone spécifique de l’enveloppe du VIH (la région V1/V2) ont également été produits. De plus, des anticorps neutralisants ont été détectés chez 50% des personnes vaccinées du groupe 0,3 mg et chez 100% des deux autres groupes à la semaine 26.
«Ces premiers résultats de phase I sont prometteurs, rapporte le Pr Yves Lévy, directeur du VRI. Le vaccin CD40.HIVRI.Env a montré à la fois sa sécurité et sa capacité à induire des réponses précoces, puissantes et durables. Les différents anticorps produits et l’activation de lymphocytes T CD4+ polyfonctionnels ont été associés à un risque réduit d’infection par le VIH dans un précédent essai vaccinal, le RV144. Toutefois, à ce stade précoce de développement du vaccin, il est important de rappeler que les volontaires doivent continuer à se protéger de tout risque d’infection par le VIH, l’efficacité du vaccin n’étant évaluée qu’en phase II/III.»
De l’espoir, donc, mais la route reste encore longue.
Bibliographie
CD40.HIVRI.ENV Vaccine induces strong and durable immune responses: ANRS/VRI06 Trial
Jean-Daniel Lelièvre, Christiane Moog, Aurélie Wiedemann, Christine Lacabaratz, Fabio Candotti, Melany Durand, Véronique Rieux, Lucile Hardel, Alpha Diallo, Song Ding, Mireille Centlivre, Rodolphe Thiebaut, Giuseppe Pantaleo, Laura Richert, Yves Levy, CROI 2023.
