D’après Segal-Maurer S et al., abstr. 127, et VanderVeen L et al., abstr. 128, actualisés.
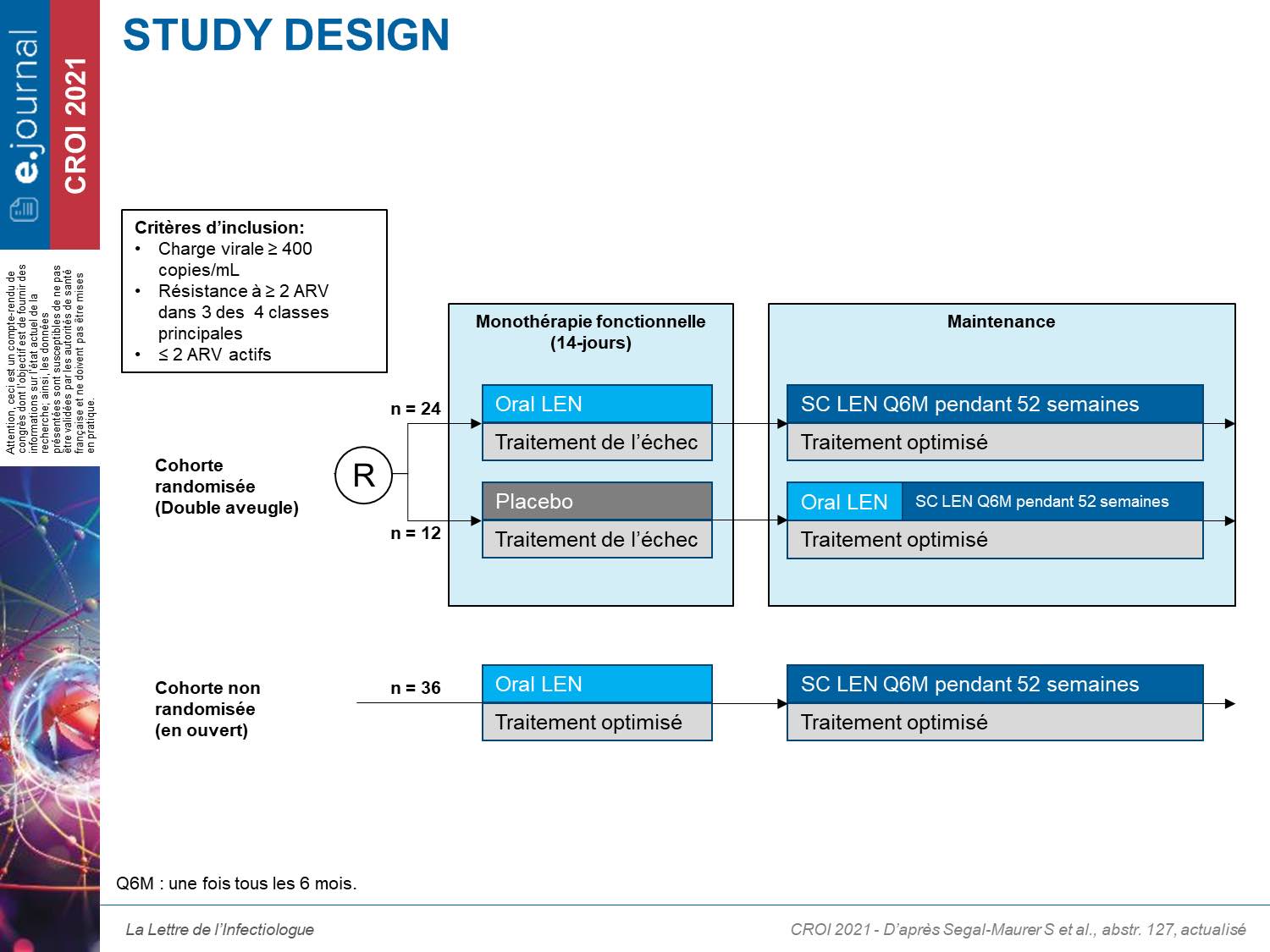
Il s’agit d’une étude de phase II/III, randomisée, en double insu comparant en monothérapie pendant 14 jours le LEN par rapport à un placeboPlacebo Substance inerte, sans activité pharmacologique, ayant la même apparence que le produit auquel on souhaite le comparer. (NDR rien à voir avec le groupe de rock alternatif formé en 1994 à Londres par Brian Molko et Stefan Olsdal.) (600 mg à J1 et J2 et 300 mg à J8 en oral), chez des patients largement prétraités, en échec virologique avec une résistance documentée à au moins 2 ARV dans au moins 3 classes thérapeutiques. Les patients étaient ensuite inclus dans un traitement de maintenance avec du LEN injectable (927 mg) tous les 6 mois associé à un traitement optimisé après un traitement oral dans le groupe placebo (schéma de l’étude ci-dessous).
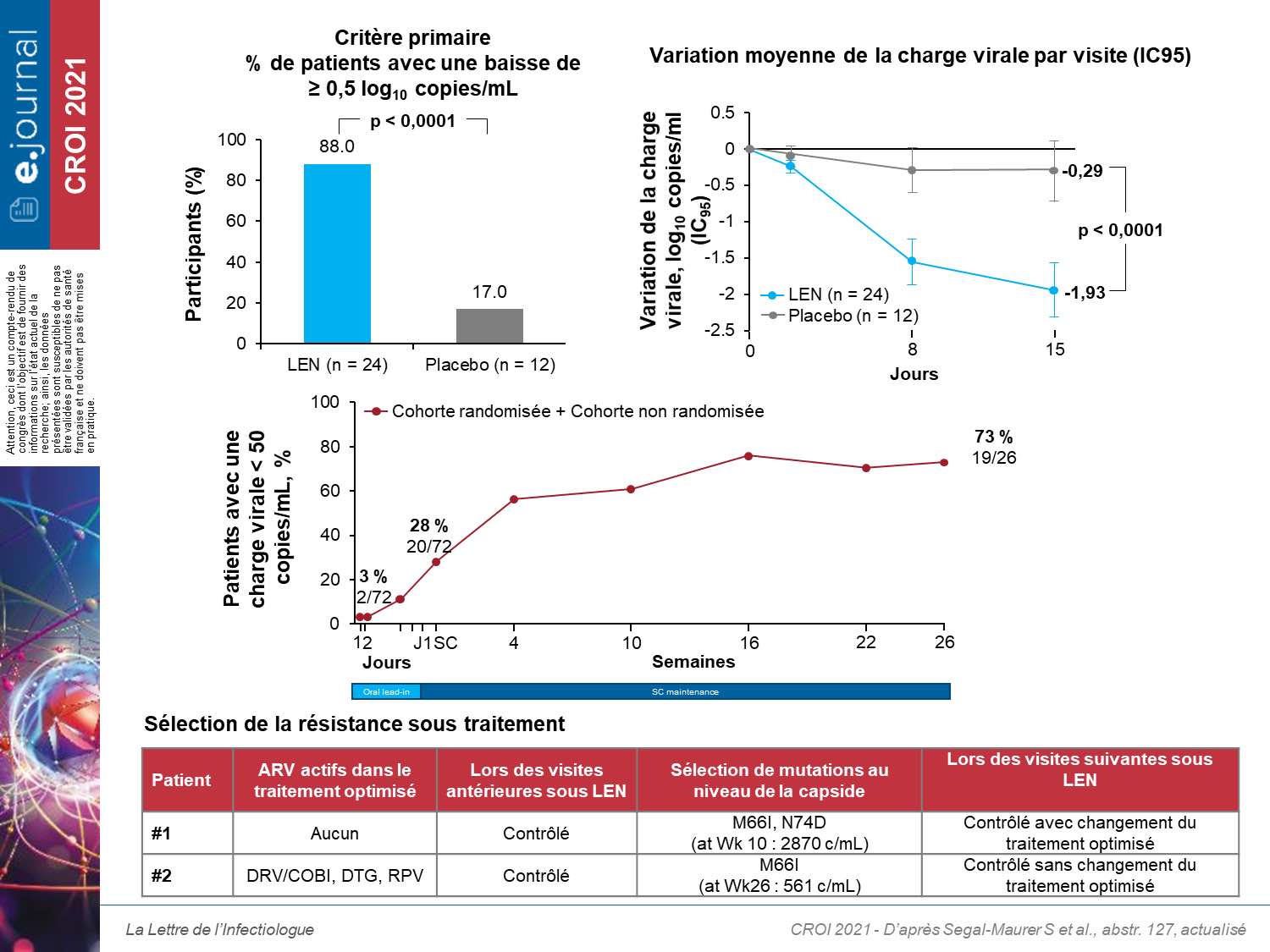
Le critère d’évaluation principal de l’efficacité était la proportion de participants avec une baisse de la CV d’au moins 0,5 log10 cp/mL à J15. 36 patients ont été randomisés avec un niveau moyen de CV de 4,27 log10cp/mL. À J15, 88 % sous LEN (21/24) avaient une baisse d’au moins 0,5 log10 cp/mL comparativement à 17 % sous placebo (2/12) (différence de 71 %, p < 0001). La variation de CV (log10 cp/mL) était significativement différente de −1,93 versus −0,29. 24 semaines après la première injection de LEN associé au traitement optimisé, 73 % des patients avaient une CV < à 50 cp/mL à S24. Sur l’ensemble des 72 patients largement prétraités des 2 cohortes, 2 patients ont présenté une sélection de résistances au LEN avec la sélection de la mutation M66I isolée pour un patient et associée à la N74D pour le second. ll n’y a pas eu d’effets indésirables graves liés au traitement, ni d’arrêt ou de décès. Les effets indésirables les plus fréquents étaient les réactions au site d’injection (46 %).
Les mutations identifiées sous pression de sélection in vitro sont au nombre de 7 (L56I, M66I, Q67H, K70N, N74D, N74S et T107N) conférant une sensibilité réduite au LEN notamment avec la M66I conduisant à une résistance de plus de 2 700 fois et une capacité réplicative réduite. Dans cette étude in vitro, le LEN était efficace sur les souches résistantes aux IP et sur tous les sous-types avec des niveaux d’IC50 similaires.
Ces données démontrent l’intérêt du développement du lénacapavir dans le traitement et la prévention de l’infection par le VIHVIH Virus de l’immunodéficience humaine. En anglais : HIV (Human Immunodeficiency Virus). Isolé en 1983 à l’institut pasteur de paris; découverte récemment (2008) récompensée par le prix Nobel de médecine décerné à Luc montagnier et à Françoise Barré-Sinoussi.
Cet article a été publié initialement dans le e-journal de « La Lettre de l’infectiologue » couvrant la conférence, nous le reproduisons ici avec leur aimable autorisation.
