Des épidémies difficiles à distinguer et à contrôler
Dans de nombreuses zones d’Afrique subsaharienne, les fièvres hémorragiques virales représentent une menace sanitaire récurrente. Les virus Ebola, Marburg ou encore celui de la fièvre de Lassa circulent dans des régions parfois proches, et leurs premiers symptômes sont souvent les mêmes : fièvre brutale, fatigue intense, douleurs musculaires, troubles digestifs.
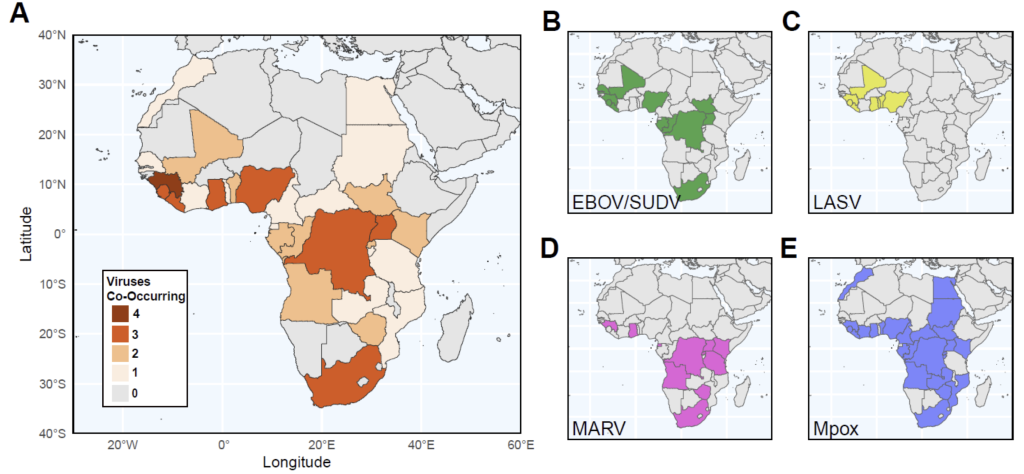
Au début de l’infection, ces signes cliniques ressemblent à ceux de nombreuses maladies tropicales courantes. Dans des contextes où les capacités diagnostiques restent limitées, identifier rapidement l’agent pathogène responsable peut s’avérer difficile. Or, cette identification conditionne la mise en place des mesures de contrôle et, lorsque cela existe, des stratégies vaccinales.
Face à cette complexité, certains chercheurs explorent une approche différente : développer un vaccin capable de protéger simultanément contre plusieurs virus responsables de fièvres hémorragiques. Une étude préclinique récente apporte de nouveaux éléments en ce sens, en testant un candidat vaccin conçu pour cibler trois agents pathogènes majeurs : le virus Sudan, responsable de certaines épidémies d’Ebola, le virus Marburg et le virus de la fièvre de Lassa.
Un vaccin multivalent basé sur une plateforme bien connue
Pour concevoir ce vaccin, les chercheurs ont utilisé une plateforme vaccinale déjà largement étudiée : le virus vaccinia modifié Ankara (MVA). Ce vecteur viral atténué est utilisé dans plusieurs vaccins expérimentaux contre des agents pathogènes émergents et possède un profil de sécurité bien documenté. Il existe surtout sous la forme de vaccinia modifié Ankara-Bavarois Nordique (MVA-BN), une version vivante, atténuée, non réplicative et exclusive du virus MVA, utilisé pour la prévention de la variole et de la variole du singe notamment dans le monde lors de l’épidémie de 2022.
Son intérêt réside notamment dans sa capacité à transporter plusieurs antigènes viraux. Les scientifiques ont ainsi introduit dans ce vecteur différentes protéines issues des virus ciblés. La glycoprotéine des virus Sudan (de la famille des Orthoebolavirus dans laquelle on retrouve le virus Ebola, le virus Soudan, le virus Taï Forest et le virus Bundibugyo) et Marburg a été sélectionnée car elle joue un rôle central dans l’entrée du virus dans les cellules. Pour le virus de la fièvre de Lassa, les chercheurs ont retenu la nucléoprotéine, connue pour déclencher des réponses immunitaires cellulaires importantes.
La stratégie vaccinale reposait sur un schéma en plusieurs étapes. Les animaux (sous sédation) ont d’abord reçu une injection d’ADN (HFVac3.v1) codant ces antigènes viraux, destinée à amorcer la réponse immunitaire. Cette première étape a été suivie de rappels avec le vaccin MVA recombinant afin de renforcer la réponse immunitaire. On parle de stratégie de prime-boost, une approche vaccinale classique où les premières injections de la primo-vaccination se font avec des vaccins différents.
Pour évaluer l’efficacité de cette approche, les chercheurs ont utilisé un modèle animal de cobayes, couramment employé pour étudier les fièvres hémorragiques. Les animaux vaccinés ont ensuite été exposés à une dose létale de l’un des virus étudiés.
Une protection élevée contre trois virus différents
Les résultats obtenus sont particulièrement encourageants. Chez les animaux non vaccinés, l’infection par les virus Sudan et Marburg s’est révélée rapidement fatale. Tous les cobayes témoins sont morts en moins de dix jours. Chez les animaux vaccinés, la situation était très différente. La vaccination a conféré une protection complète contre le virus Sudan. Face au virus Marburg, la protection atteignait 95 %. Quant à l’infection par le virus de la fièvre de Lassa, aucun des animaux vaccinés n’est décédé, alors que la quasi-totalité des cobayes témoins y ont succombé.
Les chercheurs ont également observé une forte réduction de la charge viraleCharge virale La charge virale plasmatique est le nombre de particules virales contenues dans un échantillon de sang ou autre contenant (salive, LCR, sperme..). Pour le VIH, la charge virale est utilisée comme marqueur afin de suivre la progression de la maladie et mesurer l’efficacité des traitements. Le niveau de charge virale, mais plus encore le taux de CD4, participent à la décision de traitement par les antirétroviraux. chez les animaux vaccinés. Dans de nombreux cas, le virus était à peine détectable dans le sang ou les principaux organes. Les signes cliniques restaient limités et les animaux conservaient un poids et une température corporelle relativement stables.
Une réponse immunitaire plus complexe que prévu
L’analyse des réponses immunitaires humorales et cellulaires apporte un autre enseignement important. Les animaux vaccinés ont bien développé des anticorps neutralisants dirigés contre les protéines virales. Cependant, les taux d’anticorps variaient fortement d’un animal à l’autre.
Surtout, les chercheurs n’ont pas observé de corrélation claire entre la quantité d’anticorps et la protection contre l’infection (corrélat de protection). Certains cobayes protégés présentaient des titres d’anticorps relativement modestes.
Ces résultats suggèrent que la protection ne repose pas uniquement sur les anticorps neutralisants. Les analyses immunologiques indiquent en effet que les réponses des lymphocytes T jouent probablement un rôle majeur, en particulier contre la nucléoprotéine du virus de la fièvre de Lassa.
Cette observation rejoint ce que montrent plusieurs études menées chez des survivants de la fièvre de Lassa : la réponse immunitaire cellulaire semble déterminante pour contrôler l’infection.
Vers une nouvelle génération de vaccins contre les fièvres hémorragiques ?
Si ces travaux restent précliniques, ils apportent une preuve de concept importante : un vaccin unique pourrait, en théorie, protéger contre plusieurs virus responsables de fièvres hémorragiques.
Une telle approche présenterait plusieurs avantages pour la santé publique. Dans les régions où ces virus coexistent, un vaccin multivalent permettrait de simplifier les stratégies de vaccination et de réduire la dépendance à un diagnostic virologique rapide. Il pourrait également faciliter la constitution de stocks de vaccins utilisables en cas d’épidémie.
Avant toute utilisation chez l’humain, de nombreuses étapes restent toutefois nécessaires. Des études supplémentaires devront confirmer la sécurité et l’efficacité de cette stratégie vaccinale dans d’autres modèles expérimentaux, puis dans des essais cliniques. Une fois toutes ces étapes franchies avec succès, encore faudra-t-il qu’il soit facilement accessible aux populations les plus durement concernées : on se souvient du vaccin MVA-BN contre le mpox, dont la diffusion dans les régions endémiques avait été tardive et partielle, limitant son impact initial (lire l’article sur le site de rfi).
Mais ces résultats ouvrent une perspective intéressante : celle d’une approche vaccinale intégrée face à des virus qui, malgré leur rareté relative, continuent de provoquer des flambées épidémiques meurtrières.
Référence :
Darwyn Kobasa et al. Simultaneous broad protection against Ebola Sudan, Marburg and Lassa viruses conferred by a DNA primed MVA-vectored multivalent vaccine https://www.biorxiv.org/content/10.64898/2026.03.18.712579v1
