L’ANRS-MIE a organisé le 15 janvier 2026 un point presse sur les zoonoses respiratoires émergentes. À cette occasion, Éric Cardinale, directeur scientifique de la santé animale à l’Anses, et Sibylle Bernard-Stoecklin, épidémiologiste à Santé publique France, ont fait le point sur la situation épidémiologique du virus influenza aviaire H5N1 et les dispositifs de surveillance déployés en santé animale et humaine.
Le 1er août 2025 marque le début de la saison de surveillance alignée sur les migrations aviaires. Depuis cette date, l’Europe a recensé 503 foyers en élevages de volailles, 104 foyers touchant des oiseaux captifs et 4 060 cas chez les oiseaux sauvages dans 29 pays. L’Allemagne apparaît comme le pays le plus touché avec 163 foyers en élevage et plus de 2 200 cas chez les oiseaux sauvages, suivie par le Royaume-Uni (79 foyers en élevage, 2 200 cas en faune sauvage) et la France (107 foyers en élevage, 244 cas chez les oiseaux sauvages).
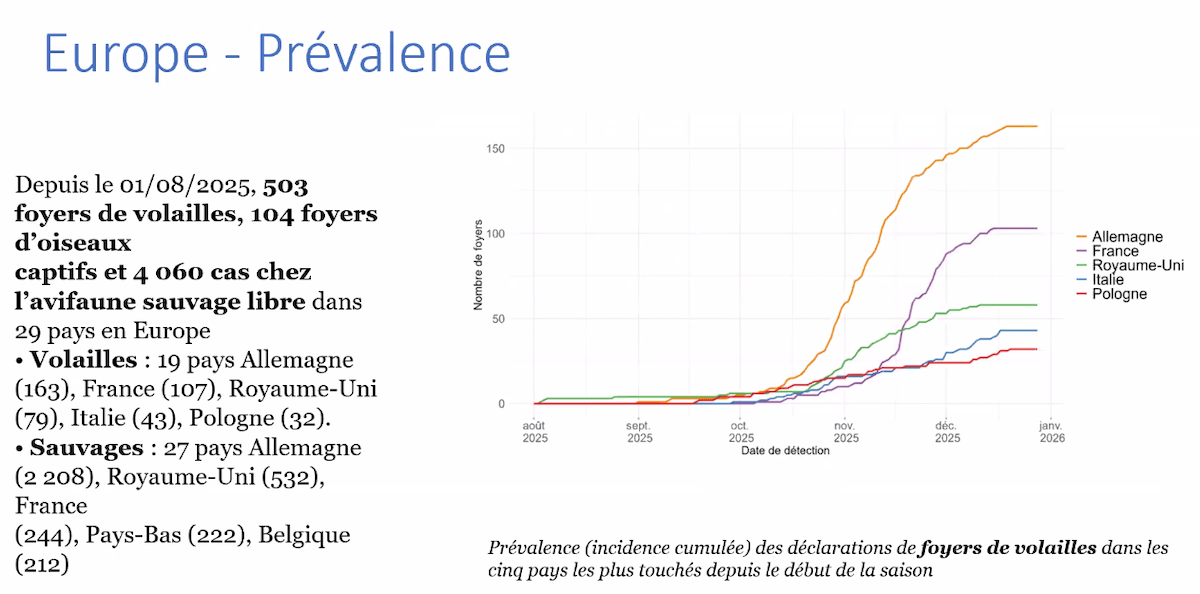
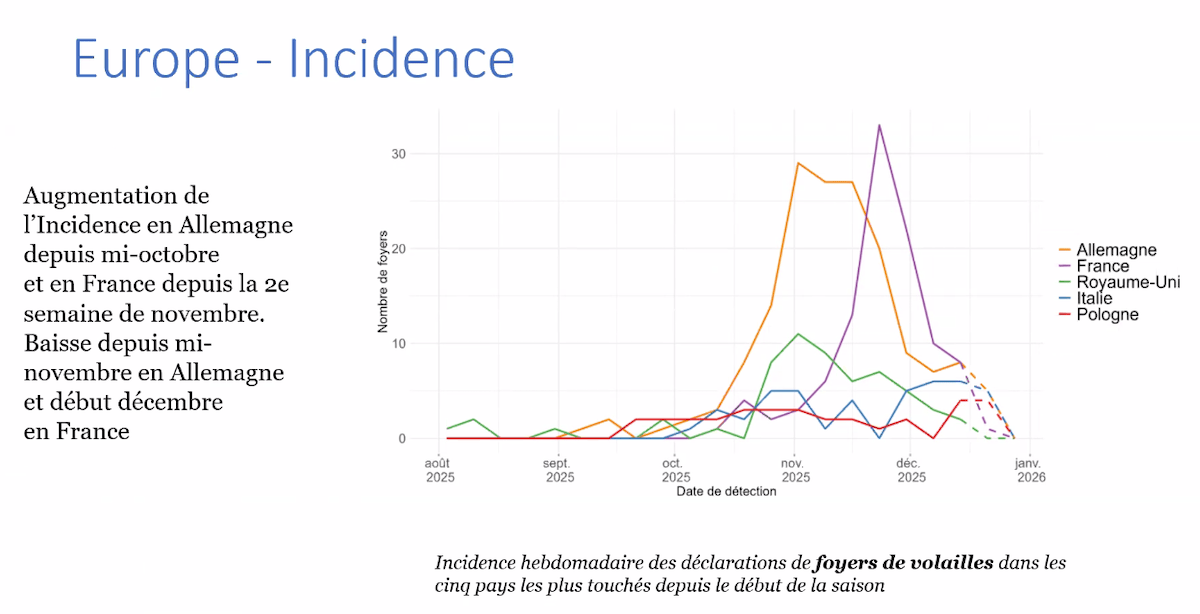
Cette saison se caractérise par une précocité inhabituelle. L’augmentation de l’incidence a débuté dès mi-octobre en Allemagne, suivie début novembre en France, avant une décrue notable à partir de mi-novembre en Allemagne et mi-décembre en France. Cette dynamique a coïncidé avec un épisode de mortalité massive touchant particulièrement les grues cendrées lors de leur migration descendante, avec plus de 10 000 mortalités recensées, principalement en Allemagne et dans le nord-est de la France. D’autres espèces ont également été affectées –anatidés, rapaces– mais les grues restent les plus impactées, comme cela avait déjà été observé en Israël en 2022 et 2021.
Sur le plan virologique, une nouvelle sous-lignée du cladeClade Les clades désignent les variations d’un même virus qui ont divergé au gré des mutations génétiques. 2.3.4.4b circulant déjà en Europe, représente désormais 85% des souches isolées chez l’animal. Cette souche, observée en 2025 en Israël et en Géorgie, témoigne d’une nouvelle introduction du virus sur le territoire européen. La pression infectieuse environnementale s’est révélée nettement plus élevée que lors des saisons précédentes, avec une extension géographique. Cela a entraîné de nouvelles expositions chez les mammifères domestiques et sauvages ; en France, des cas ont été confirmés chez des renards et des loutres, bien que ces virus restent principalement adaptés aux oiseaux.
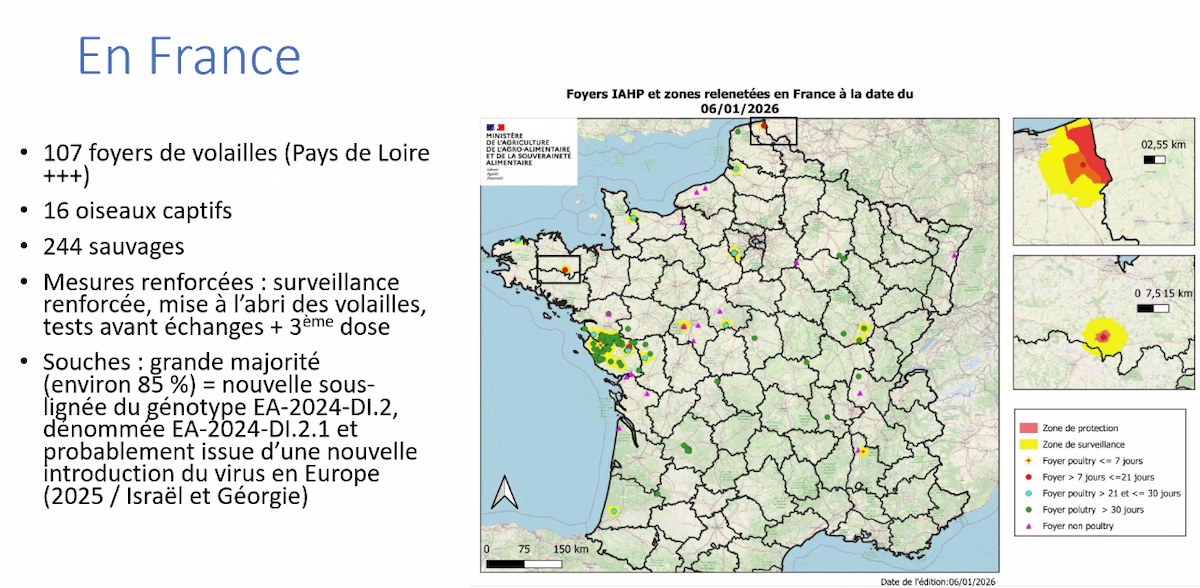
La stratégie vaccinale française des canards : un cas unique en Europe
La France demeure le seul pays européen à vacciner les canards, même si plusieurs pays ont signalé leur intérêt concernant la mise en place de campagnes de vaccination. Cette stratégie, ciblant exclusivement les canards destinés au marché local, a démontré son efficacité : avant les vaccins, les saisons 2020-2021 et 2021-2022 avaient enregistré respectivement 1200 et 400 foyers. Depuis la mise en place de la vaccination, seuls 19 foyers ont été recensés la première année et 10 l’année suivante, malgré une pression environnementale comparable aux autres pays européens et alors que la France se situe sur les trajets de migrations.
Fin novembre 2025, 6,2 millions de canards avaient reçu une première dose et 5,2 millions une deuxième dose. À ce jour, plus de 10 millions de canards ont bénéficié d’un schéma complet sur l’objectif de 60 millions d’animaux vaccinés par saison grippale. Plus de 165 000 canards ont reçu une troisième dose, notamment les canards gras à longue durée d’élevage, particulièrement dans les zones à risque comme la Vendée par exemple.
Cette vaccination s’accompagne d’une surveillance renforcée combinant deux approches : une surveillance passive reposant sur la vigilance des éleveurs signalant toute anomalie de mortalité avec une recherche directe du virus sur cadavres, et une surveillance active conduite par des vétérinaires sanitaires mandatés réalisant des détections moléculaires systématiques. Le but est désormais de comprendre les facteurs de réussite ou d’échec, afin d’améliorer la protection vaccinale et de maintenir ainsi l’immunité jusqu’à la fin de la période d’élevage.
Surveillance des cas humains
Parallèlement à cette panzootie observée depuis 2021, une recrudescence préoccupante de cas humains de H5N1 a été enregistrée au niveau international. Les premiers ont été détectés en 1997, mais le nombre le plus important a été détecté, pour l’instant, entre 2003 et 2015. Après une accalmie entre 2016 et 2021, le nombre de cas détectés est reparti à la hausse depuis l’émergence du clade 2.3.4.4b. Entre 2022 et 2025 (pas de cas encore rapporté en 2026), plus d’une centaine de cas ont été signalés à l’OMS, avec une diversification géographique remarquable : Europe (principalement Royaume-Uni), Amériques (États-Unis, Canada, Mexique, Équateur, Chili) et Asie (Cambodge, Vietnam, Inde, Bangladesh).
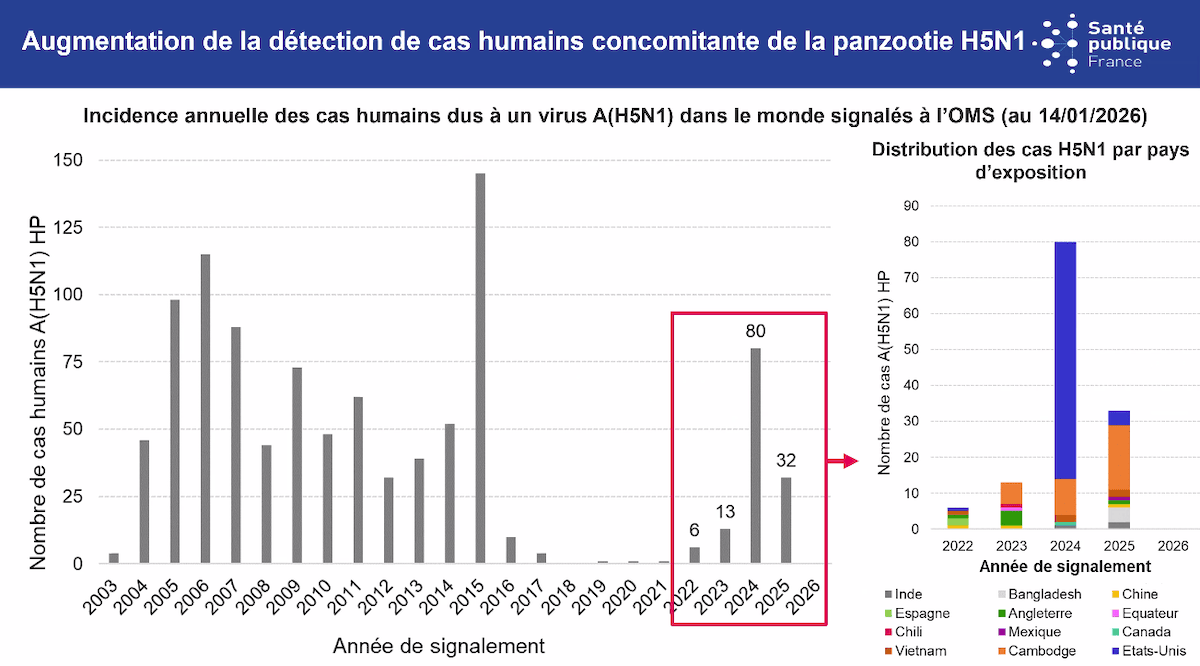
Les États-Unis ont notifié près de 70 cas en 2024, soit la majorité des détections mondiales, grâce à un dispositif de surveillance active des personnes exposées à des foyers confirmés en élevage ou basse-cour, similaire au protocole français SAGA (voir encadré ci-dessous). Cette surveillance systématique, nécessitant des moyens humains considérables, a permis de détecter des formes bénignes qui seraient autrement passées inaperçues. Depuis 2025 et la dégradation du climat politique autour de la santé publique, les données américaines se font plus rares, les cas signalés ayant été identifiés de manière fortuite, essentiellement à l’hôpital, soulevant des interrogations sur le maintien de ce dispositif dans ce contexte difficile.
Au Cambodge, un autre foyer préoccupant s’est constitué avec la détection d’un virus réassortant, résultat d’échanges de segments génomiques entre l’ancien H5N1 circulant localement depuis les années 2000 et le nouveau clade 2.3.4.4b (Voir notre article Grippe aviaire H5N1 : un nouveau virus réassortant à surveiller au Cambodge et au Vietnam).
SAGA, le dispositif français de surveillance active de H5N1
Face à ces enjeux, la France a développé et étendu depuis cette saison le protocole Surveillance active de la grippe aviaire, ou SAGA, après deux saisons pilotes en 2023-2024 et 2024-2025. Ce dispositif repose sur une articulation étroite entre santé animale et santé humaine. Lorsqu’un foyer d’influenza aviaire est confirmé, les services vétérinaires transmettent aux agences régionales de santé (ARS) et à Santé publique France les caractéristiques du foyer (notamment les espèces touchées) et la liste des personnes exposées.
Les ARS contactent ensuite ces personnes et leur proposent un dépistage systématique, même en l’absence de symptômes, deux jours après la dernière exposition au risque. Un test RT-PCR grippe A est réalisé en laboratoire de proximité. Si le résultat est négatif, la personne est invitée à surveiller son état de santé pendant 10 jours post-exposition et à consulter en cas d’apparition de symptômes. En cas de positivité pour une grippe A, le prélèvement est transmis au Centre national de référence (CNR) pour rechercher un virus aviaire. À ce jour, aucun cas humain n’a été détecté sur le territoire national.
En complément du protocole SAGA, un second dispositif cible les personnes symptomatiques ayant été exposées en dehors du contexte des foyers en élevage : basses-cours privatives, porcs, animaux sauvages. Si un patient consulte son médecin pour des symptômes évocateurs après une telle exposition, ce dernier doit prendre en charge médicalement le patient selon un protocole élaboré avec la mission Coreb et le Haut Conseil de la santé publique (HCSP). Le professionnel de santé doit également prescrire une RT-PCR avec sous-typage obligatoire, pour rechercher non seulement une grippe A mais aussi les sous-types humains H1N1 et H3N2. Une grippe A positive avec recherche négative des sous-types humains constitue un cas probable de grippe zoonotique, justifiant un signalement immédiat aux autorités sanitaires et l’envoi du prélèvement au CNR, seul habilité à confirmer ou exclure le diagnostic.
En cas de confirmation, un suivi médical adapté est mis en place, accompagné d’une investigation épidémiologique approfondie (contact tracing, recherche de la source d’infection) et de caractérisations virologiques fines.
Caractéristiques cliniques et sources d’infection
L’analyse des quelque 130 cas humains détectés depuis 2022 révèle plusieurs particularités. La majorité présente des formes bénignes, avec essentiellement une conjonctivite (un signe bénin peu décrit dans les infections H5N1 antérieures), une infection respiratoire aiguë sans notion de gravité, et des symptômes digestifs. Dans 8% des cas, aucun symptôme n’a été rapporté, les infections ayant été dépistées lors de dépistages systématiques post-exposition.

La source d’infection reste quasi exclusivement animale, par des expositions via des élevages (vaches laitières et volailles) ou des basses-cours. Dans 6% des cas néanmoins, les personnes ont été dépistées de manière fortuite, à l’hôpital, après avoir fait des formes graves.
Aucune transmission interhumaine n’a été documentée autour de ces cas, confirmant la faible adaptation de ces virus aux mammifères en général et à l’être humain en particulier. Quelques cas de transmission interhumaine suspectée ont été rapportés dans le passé, mais dans des contextes très spécifiques et non récemment.
Une évaluation de risque nuancée
Malgré la forte circulation virale dans le monde animal, les institutions internationales (OMS, FAO, ECDC/EFSA) et françaises (Santé publique France, Anses, CNR-VIR) évaluent le risque pour la santé humaine comme faible pour la population générale, et faible à modéré pour les personnes régulièrement exposées. Cette analyse globalement rassurante ne doit cependant pas masquer la vigilance nécessaire : l’évolution constante de ces virus et la pression d’exposition intense entre compartiments animal et humain constituent un risque accru de mutations et donc d’adaptation à l’être humain.
Les autorités sanitaires insistent donc sur la nécessité de renforcer le sous-typage systématique des grippes A, tant dans les réseaux de surveillance sentinelle que dans les laboratoires hospitaliers, pour détecter précocement des cas importés ou sans exposition rapportée.
À l’instar de n’importe quelle zoonose, la surveillance de la grippe zoonotique en France et au niveau international repose sur une coopération étroite entre les acteurs de la santé humaine et ceux de la santé animale. Les travaux se poursuivent pour caractériser les virus circulants, mieux comprendre leurs spécificités et les voies d’introduction. La saison 2025-2026 a confirmé que la faune sauvage constitue la voie d’introduction majeure du virus, soulignant encore une fois l’importance d’une approche intégrée «One Health» associant santé animale, santé humaine et environnement.
