Retard à l’allumage
Mathieu Chappuy, pharmacien au Csapa des Hospicescivils de Lyon a dénoncé la «mort programmée de la naloxone intranasale (Nalscue®) dans la prévention des overdoses aux opioïdes» rappelant les débuts compliqués, paradoxaux, de la dispensation de la molécule depuis 2015. Rappel des faits: connue depuis les années 1950, la naloxone a été autorisé par le National Health Institute sous sa forme de spray nasal en 2009. En France, une ATUATU Autorisation Temporaire d’Utilisation. Autorisation permettant aux malades d’avoir un accès précoce aux médicaments, avant ou hors AMM. Procédures souvent utilisée dans l'histoire du sida. de cohorte de juillet 2016 réserve le spray Nalscue® aux Csapa, Elsa, prisons, services d’addictologie et des urgences à l’hôpital et subordonne la délivrance au fait de suivre une formation. Une étude menée par le pharmacien auprès de 462 Csapamontre ainsi que, sur les 82 répondants dont 76 prennent en charge des patients dépendants aux opiacés, seuls 35ont dispensé des kits (1 116). «Les professionnels ne se sont pas investis dans le dispositif», déplore Mathieu Chappuy.
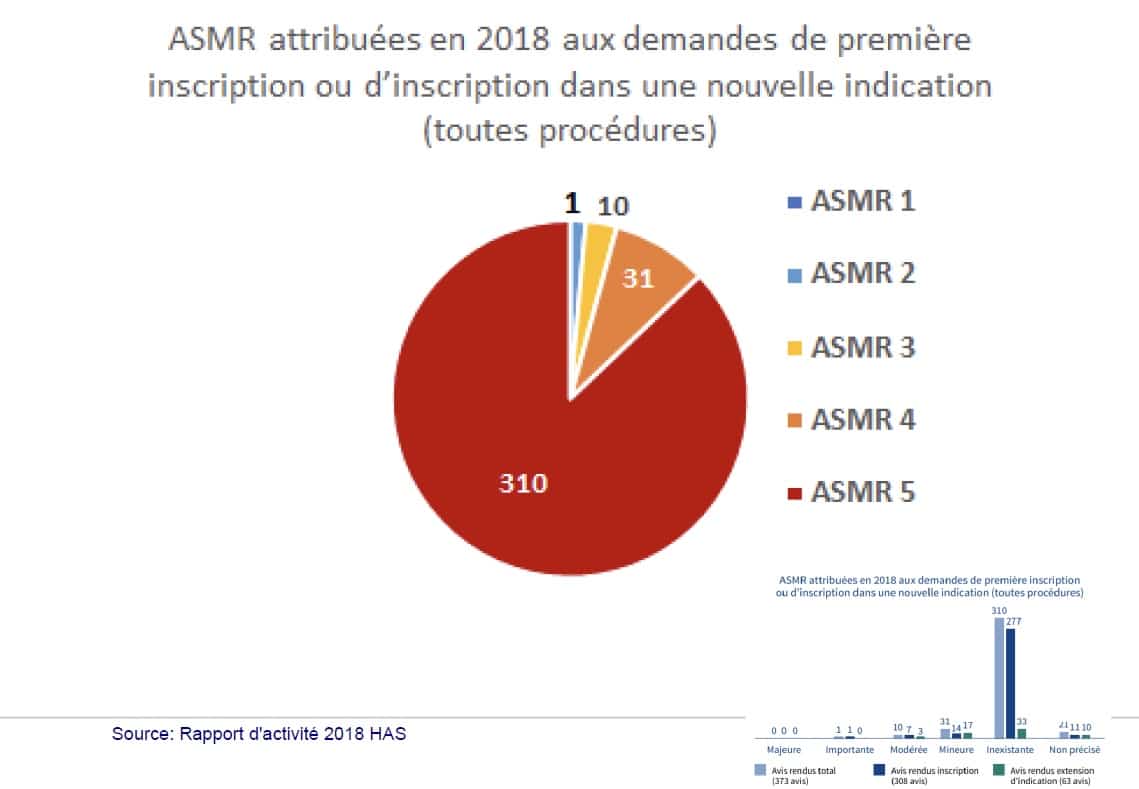
En janvier 2018, le Nalscue® obtient une AMMAMM Autorisation de Mise sur le Marché. Procédure administrative qui autorise un laboratoire pharmaceutique à commercialiser une molécule. Puis un avis favorable le 19 Février 2018 au remboursement de la Commission de transparence de la HAS avec une amélioration du service médical rendu plutôt favorable et assez rare par ces temps de régulation économique du médicament (ASMR IV) (voir Figure 1). La commission de Transparence précisant que NALSCUE «est susceptible d’avoir un impact sur la santé publique » et que « toutes les personnes à risque de surdosage aux opioïdes devraient bénéficier d’un kit de pulvérisation nasale de naloxone». Mais pas d’accord sur le prix trouvé avec le laboratoire Indivior. De 100€ dans le cadre de l’ATU (prix fixé par le laboratoire qui comprendrait le produit et le financement du dispositif ATU), il devait baisser, mais pas au-dessous de 35€. Les Caarud se plaignent de ne pouvoir distribuer le Nalscue®qu’à la condition d’avoir suivi une formation délivrée par un organisme agréé, une nouvelle complexité. Pourtant le Résumé des Caractéristiques du produit (RCP) mentionne seulement que «NALSCUE est un traitement d’urgence et il convient de s’assurer que le patient comprenne l’importance d’une prise en charge médicale après l’utilisation de ce médicament. Les patients à risque de faire un surdosage aux opioïdes et les personnes susceptibles d’administrer NALSCUE doivent recevoir des instructions claires quant aux circonstances et modalités d’administration de ce médicament». Alors que la feuille de route ministérielle prévoit un passage en ville, les négociations entre le laboratoire Indivior et le comité économique des produits de santé ont achoppé sur le prix, fin septembre. Et là, on n’y comprend plus rien…
Les labos en négo
En attendant, les acteurs bouillonnent : un médecin généraliste de Montluçon se plaint de ne pouvoir obtenir le produit, Catherine Duplessy, directrice de Safe, dit qu’elle a testé 180 pharmacies en France et qu’aucune ne s’est avérée capable de le commander. Pour Stéphane Robinet, du Csapa Pierre Nicole à Paris, il n’y a rien de plus facile. Alors qui bloque la naloxone: les pharmaciens, les CSAPA, les pouvoirs publics (HAS) ou le laboratoire? Quel prix pour la forme nasale en ville? 35 € ou plus?
Pour Mustapha Benslimane et Stéphane Robinet (cf. édito de la revue «le Flyer»): «On a du mal à croire qu’un kit contenant une dose de naloxone (…) puisse coûter plus d’une dizaine d’euros à fabriquer, emballer et distribuer ! On sait comment fonctionnent les firmes pour les négociations autour du médicament. Concernant les “nouvelles” formes de naloxone, on sait très bien qu’elles visent un prix “mondial” autour de 100€!» Affirmation contredite par Sophie Katz, directrice des Affaires publiques d’Indivior qui précise que le laboratoire était prêt à mettre sur le marché un lot de 30 000 kits spécialement fabriqué pour la France, seul pays à avoir donné l’AMM, au prix plancher de 35€ qui correspondrait au prix de production. Le lot sera périmé en décembre 2020!
En attendant que les choses se clarifient, l’association Safe est prête : elle a préparé 25 000 affiches, 15 000 brochures et presque autant de flyers pour informer sur les kits Nalscue®, leur intérêt et comment les utiliser. Elle a également conçu une formation en ligne pour tous, usagers, proches, ou soignants, certifiante pour les professionnels des Caarud.
Par ailleurs depuis juin, le Prenoxad®, forme injectable en intramusculaire, est disponible en officines au prix de 23,13€. La Commission de transparence de la HAS a considéré que PRENOXAD «n’apporte pas d’amélioration du service médical rendu (ASMR V) dans le traitement d’urgence, chez l’adulte, des surdosages aux opioïdes, caractérisés ou suspectés, se manifestant par une dépression respiratoire et/ou une dépression du système nerveux central, dans l’attente d’une prise en charge par une structure médicalisée».
