Efficacité de la stratégie de maintenance en administration tous les 6 mois avec du lénacapavir associé à 2 bNAbs dont un seul est testé sensible
D’après Eron JJ et al., abstr. 120 actualisé.
Après la preuve de concept démontrée pour un traitement de maintenance par lénacapavir (LEN) associé à 2bNAbs (TAB, teropavimab; ZAB, zinlirvimab) testés sensibles en administration tous les 6 mois (CROI 2023, abstr. 193), ce nouvel essai a pour objectif de définir le seuil optimal de sensibilité des bNAbs nécessaire pour atteindre l’efficacité.
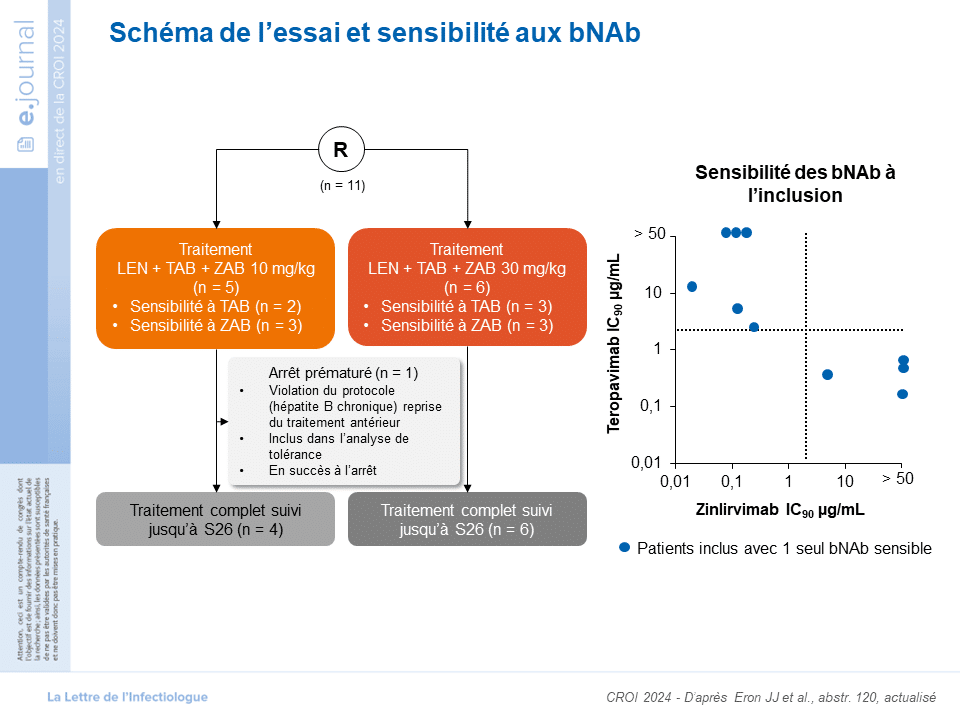
Ce nouvel essai clinique randomisé de phase Ib a évalué la tolérance et l’efficacité de l’association LEN + TAB + ZAB selon la dose de ZAB 10 mg/kg versus 30 mg/kg avec 1 seule administration et une évaluation de l’efficacité virologique à S26. Comme l’essai précédent, les patients inclus devaient avoir un contrôle de leur CV d’au moins 18 mois, un nadirNadir Chiffre indiquant la valeur minimale enregistrée de la charge virale ou des CD4. de CD4 ≥ 350/mm3, un taux de CD4 à l’inclusion ≥ 500/mm3 mais une sensibilité phénotypique à seulement un des 2 bNAbs. Dix patients ont été évalué jusqu’à S26.
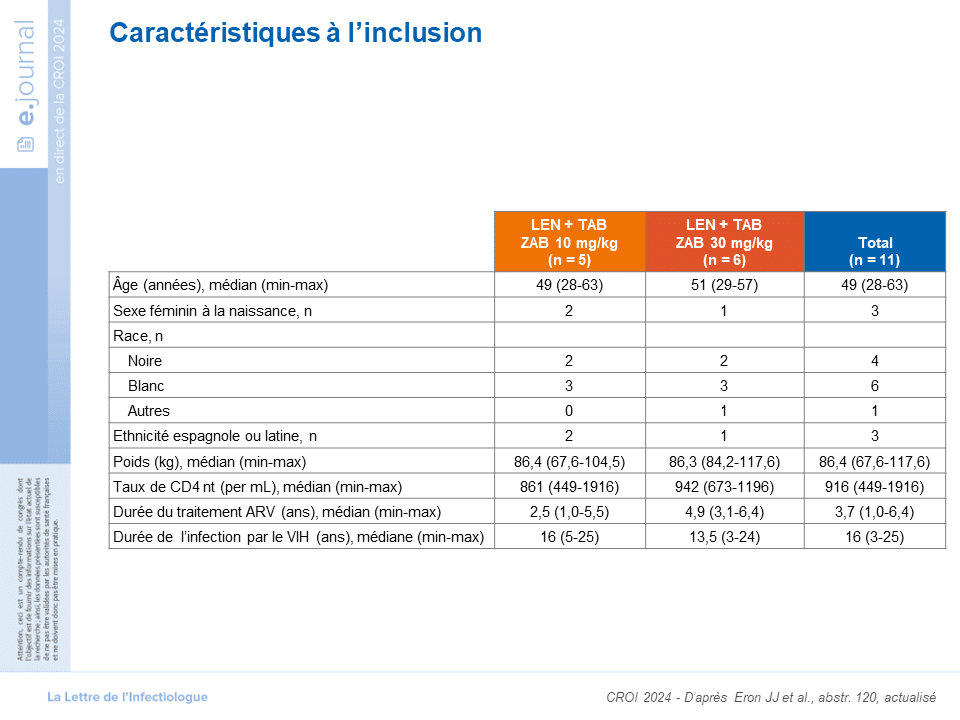
La suppression virologique (< 50 cp/mL) a été maintenue chez 8 des 10 patients 6 mois après l’administration. Tous les participants du bras ayant reçu la dose la plus élevée de ZAB (n = 6 ; ZAB 30 mg/kg) ont été contrôlés jusqu’à S26. Deux participants du bras ZAB 10 mg/kg ont présenté un rebond virologique (pour le premier : à 72 cp/mL à S26 ; pour le second : à 112 cp/mL à S20) malgré des concentrations satisfaisantes au LEN et aux 2 bNAbs. Il n’y a pas eu de sélection de résistance. La suppression virologique a été obtenue avec la reprise du traitement antirétroviral antérieur pour le 1er patient. Le second patient a continué à présenter une CV détectable de faible niveau après la reprise du traitement oral. D’autre part, cette association à longue durée d’action a été bien tolérée avec toujours les réactions au site d’injection de grade 1 liées au LEN.

L’anticorps neutralisant VRC07-523LS, un nouveau compagnon pour le cabotégravir dans la stratégie de maintenance en «long acting»
D’après Taiwo B et al., abstr. 119, actualisé.
Actuellement en stratégie de maintenance tous les 2 mois, il existe uniquement l’association en cabotégravir (CAB)+ rilpivirine (RPV) en injectable. L’objectif de cet essai clinique de phase II, à 1 seul bras (ACTG A5357) est d’évaluer l’association du VRC07-523LS, un bNAb ciblant le site de fixation du VIH-1 au CD4, et le cabotégravir à action prolongée (CAB LA) dans le cadre d’un traitement de maintenance.
Après une phase orale de 2 INTIINTI Les inhibiteurs nucléosidiques de la transcriptase inverse du VIH ou INTI, sont des composés de synthèse utilisés dans le traitement du VIH et des hépatites. + CAB pendant 1 mois, les patients recevaient le VRC07-523LS par voie i.v. (40 mg/kg) toutes les 8 semaines et le CAB LA par voie i.m. 400 mg toutes les 4 semaines après 600 mg de dose de charge.
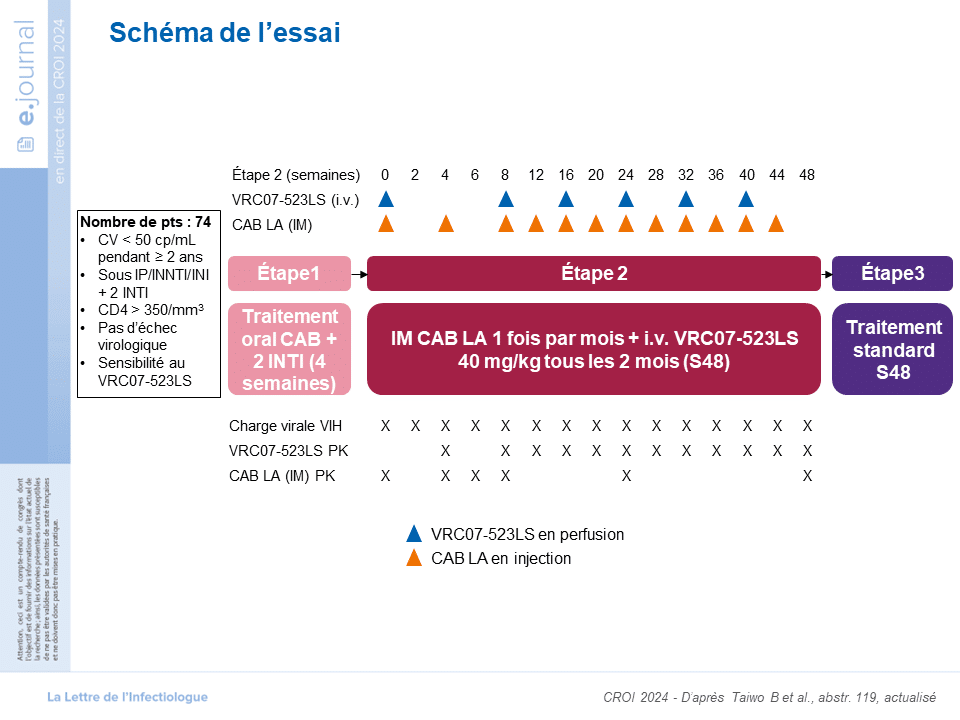
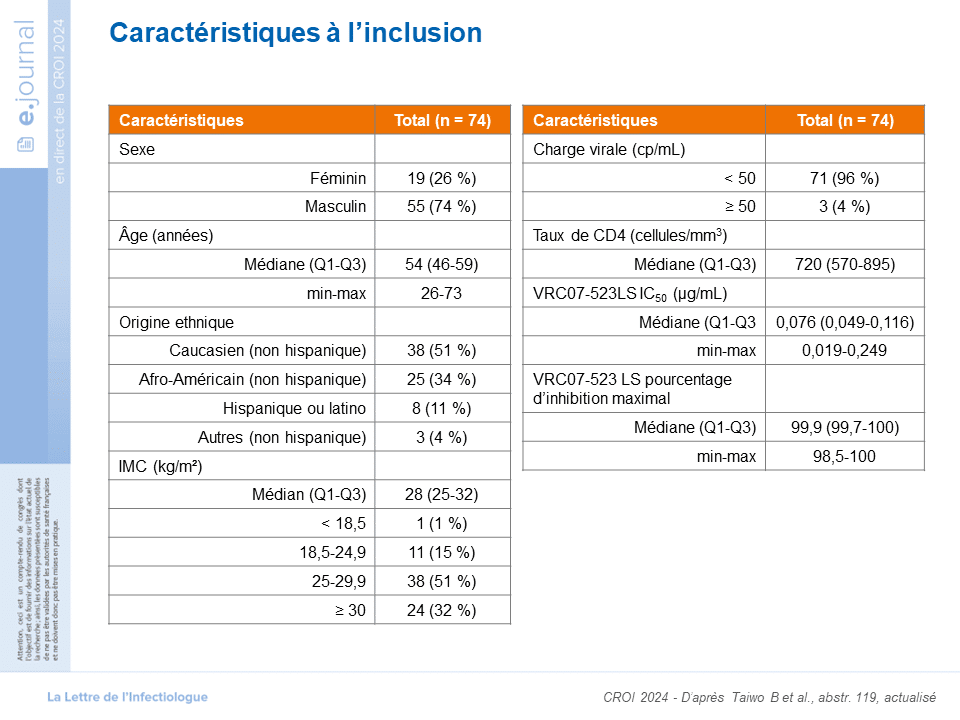
Les patients inclus avaient un taux de CD4 ≥350 cellules/mm3 et un virus testé sensible au VRC07-523LS (CI50≤ 0,25 μg/mL et un pourcentage maximal d’inhibition (MPI) >98 %). L’analyse a porté sur 74 patients avec un suivi jusqu’à S44. Les caractéristiques étaient les suivantes : un âge médian de 54 ans, un taux médian de CD4 de 720 cellules/mm3 et une CI50 médiane de 0,076 μg/mL.
Le risque cumulé d’échec virologique à S44 était de 7,3 % (IC95 : 3,2-16,0). Cinq patients ont présenté un échec virologique.
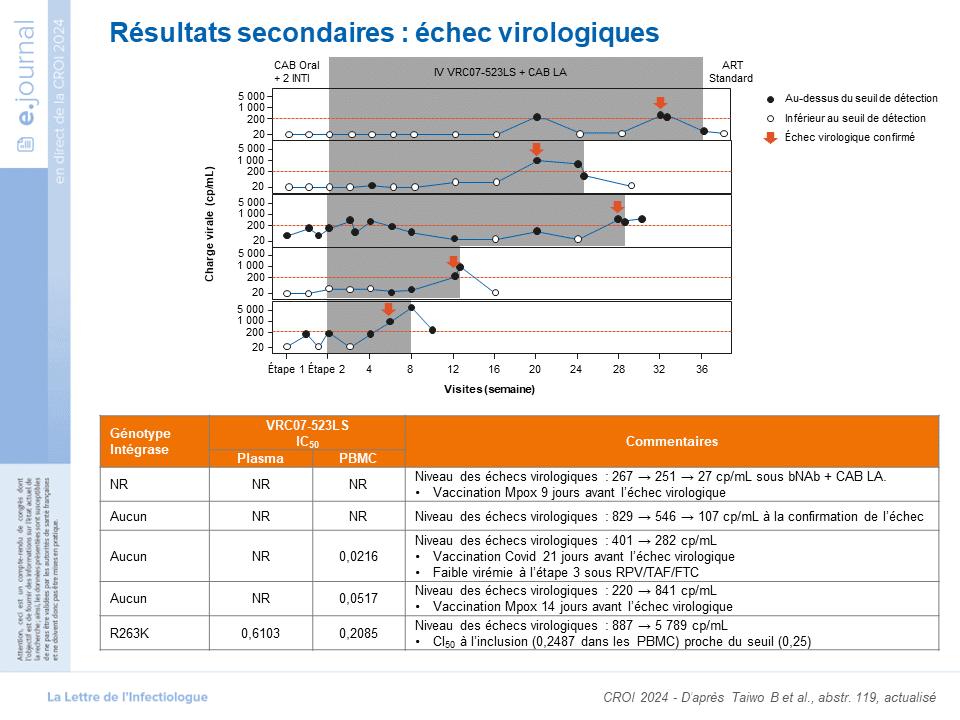
La sélection de la mutation R263K sur l’intégrase a été observée chez un patient dont la IC50 duVRC07-523LS était proche du seuil (0,25 μg/mL) laissant potentiellement le CAB en monothérapie. Douze patients (16,9 %) ont présenté un effet indésirable avec un arrêt de traitement pour un patient en raison d’une réaction liée à la perfusion. Pour les 11 autres patients (15 %), les effets de grade 3 (principalement des frissons, des myalgies, de la fatigue) n’ont pas entraîné l’arrêt du traitement.
Cette nouvelle option en LA pourrait être intéressante chez les patients présentant des résistances, notamment à la RPV. Cependant, son efficacité semble dépendante de la sensibilité virale à l’anticorps neutralisant.
Ces articles ont été publiés dans le e-journal de la Lettre de l’infectiologue consacré à la CROI 2024. Nous les reproduisons ici avec l’aimable autorisation d’Edimark.
